Полиорганосилоксаны получают методом гидролитической поликонденсации алкил (арил) хлорсиланов /?*С14-х и замещенных эфиров ортокремневой кислоты—алкил (арил) этоксисиланов Кх (ОС2Н5) 4—х, где х=1—3. Наиболее часто используются соединения, где И — СНз, С2Н5 или С6Н5.
Метод гидролитической поликонденсации основан на том, что многие функциональные группы, связанные с кремнием (преимущественно галоид и алкоксигруппы), способны легко гидролизоваться с образованием органосиланолов:
TOC o "1-5" h z И X
+2Н20 =*==* Рг2&(0Н)2-Ь 2НХ, (4.1>
И X
Где X — галоид или алкокси-группа.
Последующая конденсация органосиланолов приводит к образованию полиорганосилоксанов:
—а—ОН — ь НО—51— —О—в* Ь НаО. (4.2>
Из галоидсиланов используют хлорсиланы, которые легка гидролизуются в холодной воде. Процесс их гидролиза экзотер-
Мичен и сопровождается значительным выделением тепла. Ал — коксисиланы гидролизуются труднее, чем хлорсиланы, причем их склонность к гидролизу в значительной степени определяется характером алкоксидного заместителя: гидролиз алкокси- силанов замедляется при любом усложнении алкоксигруппы. Особенно способствуют понижению склонности к гидролизу разветвленные алкоксигруппы, что обусловлено в первую очередь пространственным эффектом заместителя. Константы скорости гидролиза различных алкоксисиланов в зависимости от характера алкоксидного заместителя резко снижаются в ряду:
|
|
|
ОС2Н5 |
![]() Увеличение электроотрицательности заместителей, связанных с атомами кремния или кислорода, способствует повышению склонности алкоксисиланов к гидролизу. Так, например, при гидролизе триэтоксифеноксисилана наиболее реакционноспособной является феноксигруппа:
Увеличение электроотрицательности заместителей, связанных с атомами кремния или кислорода, способствует повышению склонности алкоксисиланов к гидролизу. Так, например, при гидролизе триэтоксифеноксисилана наиболее реакционноспособной является феноксигруппа:
ОС8Нв
СгН60—Бі—ОСвН5 + НгО =*=а= С2Н50—Бі—ОН + СвН5ОН. (4.4)
|
ОС2Н6 |
![]() ОС2Нв
ОС2Нв
Реакция гидролиза алкоксисиланов подвержена кислотному и основному катализу, причем гидролиз некоторых алкоксисиланов с разветвленными алкоксидными заместителями протекает только в присутствии катализаторов.
Основно-каталитический гидролиз протекает по механизму 5^2—Бк
|
± — Зі—ОН +НОР+ ОН (4.5) |
![]() | _ ч /ОИ Н2о
| _ ч /ОИ Н2о
Д. пн —>- —к:’ ^——
Схему кислотного катализа можно представить следующим образом:
|
Н |
Наиболее быстро и полно гидролиз этоксисиланов протекает в присутствии таких катализаторов, как НС1, Н2504 и другие минеральные кислоты, кислые катионообменные смолы, сильные основания. Относительная активность кислотного и
основного катализа определяется строением заместителей у атома кремния. Так, например, гидролиз триалкилалкоксиси — ланов в кислой сред^ протекает в 1,5—2 раза быстрее, чем в основной. Для триалкилфеноксисиланов эффективнее основный катализ.
Гидролиз алкокси — и хлорсиланов можно проводить в присутствии органических растворителей. При использовании растворителей, хорошо смешивающихся с водой, гидролиз идет с большей скоростью за счет гомогенизации среды. Применение растворителей, не смешивающихся с водой, напротив, приводит к замедлению процесса. Вместе с тем такие растворители облегчают удаление побочного продукта (НС1).
Гидролиз в спиртах сопровождается частичной этерифика — цией алкилхлорсиланов или переэтерификацией исходных ал — коксисиланов спиртом-растворителем с образованием алкок — сипроизводных. Переэтерификация наблюдается в случае, когда образующееся алкоксипроизводное более стойко к гидролизу, чем исходное [см. ряд (4.3)]:
TOC o "1-5" h z И I*
К—Я—Х + И"ОН И—51—СЯГ +НХ, (4.7)
Я I*
где X—С1 или СЖ’.
В зависимости от структуры исходного мономера в результате гидролиза могут образовываться силаны с различным числом гидроксильных групп (от одной до четырех). В отличие от третичных спиртов (триалкилкарбинолов) триалкилсиланолы не способны к внутримолекулярной дегидратации и сравнительно легко подвергаются гомоконденсации с образованием соответствующих дисилоксанов:
КзЗЮН+НС^з + НаО. (4.8)
Соединения с двумя гидроксильными группами у атома углерода малостойки, в то время как известны многочисленные соединения кремния аналогичной структуры. В достаточной степени стабильными являются и трисиланолы 1^1 (ОН) з. Тет — расиланол — ортокремниевая кислота 5ЦОН)4 — может некоторое время существовать в мономерной форме при pH 2,7— 2,8 и быстро конденсируется в тетрамер.
Механизм конденсации в присутствии оснований может быть представлен схемой:
TOC o "1-5" h z I I
—51—ОН + "ОН ч=>: —8<—0’+ Н„С). (4.11)
+ но—в!- . * ^5|~он — ‘ —,ч;-о—+ он (1-^)
Лимитирующей стадией является взаимодействие аниона с силанолом — реакция (4.12).
Поскольку гидролиз хлор — и алкоксисиланов и конденсация силанолов представляют собой последовательно-параллельные реакции, стадия гидролиза не может быть отделена от основного процесса получения полимера (поликонденсации). Именно поэтому метод получения полисилоксанов называют гидролитической поликонденсацией.
Гидролитическую поликонденсацию обычно проводят в среде органических растворителей, причем природа растворителя оказывает влияние не только на скорость реакции, но и на структуру образующихся продуктов. Ускорение процесса в полярных растворителях обусловлено их сольватирующей способностью: чем прочнее комплекс силанола с растворителем, тем труднее проходит нуклеофильное замещение у атома кремния, т. е. конденсация.
Структура продуктов гидролитической поликонденсации определяется условиями проведения процесса и зависит от таких факторов, как функциональность исходных мономеров, структура заместителей при атоме кремния, pH среды, тип растворителя.
Монофункциональные триалкил(арил)силанолы независимо от условий конденсации образуют димеры, не содержащие свободных функциональных групп:
+2НгО —Н20
21^0 г^БЮН =8=±: 1^—О—аИз (4.13)
—2НС1
Сами по себе димеры не представляют большого интереса, однако монофункциональные соединения иногда используют в качестве регуляторов роста цепи, что позволяет при соконден — сации с ди — и трифункциональными алкил (арил) хлорсиланами получать полимеры с различной, заранее заданной длиной цепи:
+<п+1)Н20
ГЯз&а + пя2ж2 -( — > к35;—[—озд2—]п-о5ш3 (4.н)
—2(п+1)НС1
При гидролитической поликонденсации бифункциональных мономеров в зависимости от pH среды образуются линейные или циклические соединения:
9пн2о — [2{т+к)—1]Н20
ПГ^51(ОН)2 ■ НО—[——]т—Н 4*
—2пНС1
+ [1^0]* (4.15)
При pH>7 образуются в основном олигомеры линейного, а при рН<7 — циклического строения, преимущественно шести — и восьмичленные:
TOC o "1-5" h z И И
/ si-0-Si/
X «/| Iх»
К О О и или к О О
V1 К О I/
К О к /
Полимеризация образующихся органоциклосилоксанов приводит к полиорганосилоксанам линейного строения.
Скорость полимеризации зависит от природы групп, связанных с атомом кремния, и убывает в ряду: Н>СНз>С2Н5>
Поскольку силоксановая связь исключительно устойчива к гемолитическому расщеплению, возможность полимеризации циклосилоксанов под действием инициаторов радикальных реакций мало вероятна. Циклосилоксаны полимеризуются под действием сильных кислот и оснований (КОН, НС1, НгЭО«, А1С13, ИС14) по ионному механизму (соответственно анионному или катионному).
Схему процесса анионной полимеризации можно представить следующим образом:
|
К о Vч*’ /А о V / I? —51—0 I К |
|
Постоянно присутствующий в системе анион ——О — яв- I Ляется ответственным за полимеризацию. Катионная полимеризация протекает по схеме КОЯ КОЯ </ ,/ V / |
|
Т О я + н+ |
|
/А |
|
/ |
|
И 0-н+ |
|
V |
|
V Я» |
|
Г Я "1 —0£я— _ 4 _ При гидролитической поликонденсации трифункциональных мономеров могут образовываться полимеры с разветвленной (III), лестничной (силсесквиоксаны) (IV) или сшитой структурой молекул: |
|
Н— |
|
—оа+ А |
|
(4.18) |
|
■ и и —Б1—О— I _ К |
|
И —51—0- + I |
|
Но— |
 |
|
|
|
|
|
|
|
|
|
 |
|
ЯКЯ(ОН)а |
![]()
|
(4.19)^ |
![]() ИЯ51С1з+ЗлН80
ИЯ51С1з+ЗлН80
—ЗпНС!
~0 И О Я О Е? О — 1/ |/ 1/
А
I
О~
|
«Я5|(ОН)3 |
![]() О
О
Я
Й
/1 /1 /| ~о О О Я О о о~
* *
III
И о и I/ |
|
— И О И НО— ——О— —Н IV |
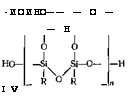 НО—Б! Я—ОН
НО—Б! Я—ОН
|
0,25 |
![]() 0,25п О О
0,25п О О
|
НО——ОН
|
Из изложенного очевидно, что стойкость силанолов резко снижается с увеличением числа гидроксильных групп у атома кремния, что проявляется во всех без исключения реакциях, в том числе и при поликонденсации.
Конденсация снланолов протекает уже в отсутствие катализаторов и в значительной степени ускоряется при воздействии кислот и оснований. При кислотном катализе в результате реакции силанола с кислотой образуются ионные пары, которые затем медленно реагируют с другой молекулой силанола; при этом получается силоксан и регенерируется катализатор.
Гидролитическая соконденсация би — и трифункциональных мономеров приводит к образованию полиорганосилоксанов циклолинейной структуры.
Как уже упоминалось, в кислой среде в составе, продуктов реакции преобладают циклические соединения типа I, образующиеся в результате внутримолекулярной дегидратации алкил — и арилтригидроксисиланов. Поликонденсация циклических соединений с продуктами гидролитической конденсации диорга — нодихлорсиланов, имеющих линейную структуру, приводит к образованию циклолинейных полимеров:
—10пНС1
2пЯгБ1аг+2пЯ’51С13+10пН90
(10п-1)Н*0
(4.21)
|
И |
 8 сентября, 2013
8 сентября, 2013  admin
admin 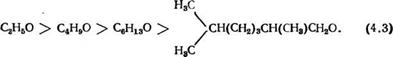
 Опубликовано в рубрике
Опубликовано в рубрике 