Термином «гидратная оболочка» мы будем обозначать пространство вокруг молекулы растворенного вещества в растворе, в котором физические свойства воды отличаются от свойств чистой воды.
Большое число публикаций посвящено определению количества молекул воды в гидратных оболочках органических и неорганических соединений в водных растворах. Для этой цели использовались самые разнообразные методы [143]. В большинстве работ число молекул воды рассчитывали на основании
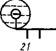
Рис. 3.1. Иллюстрация метода @
«молекулярного щупа».
При сближении двух атомиых групп на расстояние, когда гидратные оболочки перекрываются, гидрата — дионная характеристика изменяется
&
|
|
|
|
Измеренном характерне — тики (группы характери- стик) водного раствора исследуемого вещества в || рамках тех или иных по — сылок о свойствах гид-
Расстояние между гидратируемыми ерц^апи
Мер, при нахождении числа гидратации по сжимаемости раствора ряд авторов, вслед за А. Г. Пасынским [144, 145], принимали сжимаемость гидратной оболочки равной нулю. Другие исследователи принимали ее равной сжимаемости льда, как, например, в работах [146, 147]. Предположения такого рода носят достаточно произвольный характер и различаются от метода к методу, что значительно снижает достоверность получаемой информации даже в случае простых электролитов [148], а для органических соединений приводит к противоречивым результатам.
Наиболее прямое определение размеров гидратной оболочки органических соединений может быть сделано с помощью метода, который назовем условно методом «молекулярного щупа>
[149].
Метод основан на сравнении величин, характеризующих состояние воды в гидратной оболочке исследуемой атомной группы, входящей в состав различных молекул. Молекулы должны быть близки по строению, но расстояния между атомными группами для них должны быть различными. При этом гидратная оболочка как бы «прощупывается» другими атомными группами.
|
Ратной оболочки. Напри- |
Схематически сущность метода поясняет рис. 3.1. Метод не связан с какой-либо конкретной физической характеристикой раствора, поэтому с его помощью можно сравнивать данные, полученные разными физическими методами. Одним из факторов, ограничивающих применимость метода, является возможность взаимодействия между атомными группами не только посредством перекрывания гидратных оболочек, но и посредством смещения электронной плотности ковалентного остова молекулы, вследствие чего может изменяться характер взаимодействия исследуемых групп с водой. Однако даже в тех случаях, когда таким взаимодействием пренебречь нельзя, метод «молекулярного щупа» дает информацию о верхней границе размеров гидратной оболочки.
|
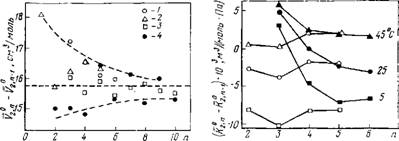
Рис. 3.2. Зависимость приращения парциального объема (У°) в гомологических рядах: ; —ОН(СН2)„ОН [151]; 2 — Н02С(СН2)„С0гН [153]; 3 — NH2(CH2)nNH2 [154]; 4 — NH3+(CH2)nC02- [155]. Выход на плато —при л<6 |
Рис. 3.3. Зависимость приращения парциальной адиабатической сжимаемости в гомологических рядах спиртов [152]:
; —Н(СН2)„ОН; 2 — НО(СН2)ПОН. Выход на плато — при п<5
Одной из разновидностей метода «молекулярного щупа» является анализ гомологических рядов. Для оценки размеров гидратной оболочки такой анализ впервые использовался в работе Эверта [150]. В качестве «щупа» здесь используется алифатический радикал, присоединенный к исследуемой атомной группе. Анализируемыми гидратационными характеристиками могут быть парциальный молярный объем, сжимаемость, теп-
|
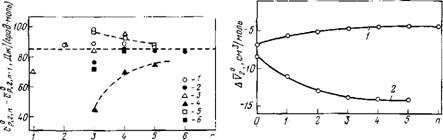
Рис. 3.4. Зависимость приращения парциальной теплоемкости (с°) в гомологических рядах [156—158]: О — монофункциональные ряды; • — бифункциональные ряды; 1 — Н(СН2)яОН; 2 — НО(СН,)яОН; 3 — Н(СН2)лС02Н; 4 — НООС(СН2)„СООН; 5 — H(CH2)„NH2; 6- HJN(CH2)„NH2. Выход на плато при л=5 |
Рис. 3.5. Зависимость объемного эффекта протоиирования аминогруппы (/) и ионизации карбоксильной группы (2) от длины алифатической цепи [159] 1: H(CHj)NNHs+H+-*-H(ch2)„nh3+; 2: Н(СН2)„СООН->-Н(СН2)лСОО—|-Н+. Выход иа плато при одной и той же длине цепн (/1—4)
Лоемкость, изменение этих величин при реакции протонирова — ния исследуемой атомной группы и ряд других. Зависимости: парциальных молярных характеристик от длины алифатического радикала выходят на линейный участок при таких длинах,, когда прекращается перекрывание гидратных оболочек концевых атомных групп. На рис. 3.2—3.5 приведены результаты исследований гомологических рядов [151—159]. Как следует из этих и ряда других [150,160—162] данных, перекрывание гидратных оболочек концевых атомных групп прекращается при таких расстояниях, когда между атомными группами может разместиться 2—4 молекулы воды. Это утверждение справедливо как для заряженных, так и для полярных и гидрофобных атомных групп. В целом анализ совокупности имеющихся данных по гомологическим рядам свидетельствует о том, что гидрат — ные оболочки атомных групп органических соединений состоят из одного или, как максимум, двух слоев молекул воды.
Другим примером использования метода «молекулярного щупа» является исследование гидратации фосфатной группы нуклеозидов и нуклеотидов [149, 163]. В качестве гидратацион — ной характеристики использовался эффект ионизации этой группы, наблюдаемый по скорости распространения, ультразвука в растворе (изменения скорости ультразвука отражают изменения объема и сжимаемости при ионизации молекулы). На рис. 3.6 представлены схематические изображения исследо-
✓ Tpoctpam натрия 5 — рийозосросфат 23
|
5-АІЇТ 5′-УМ<Р 5′-ЦМ? |
|
Т 21-22 |
АА, см3/мо/іь
З’-АМФ З’-УМ9 3′-ГМ9
Ф
2Р
|
/-AMP 2′-УМ9 2′-ГГі9
1Є-20 |
|
5і-АД9 5′-УД?
|
ЛА, см31моль
Рис. 3.6. Изменения концентрационного иикремента скорости ультразвука при ионизации фосфатной группы в составе различных соединений [149, 163J.
При приближении фосфатной группы к другим атомным группам вытесняется часть воды из гидратной оболочки и эффект ионизации уменьшается. Эффект ионизации выражен в см’/моль (относительное увеличение скорости ультразвука в растворе в пересчете на концентрацию 1 моль/см3). Фосфат натрия — ЫаНгРО«
Ванных соединений и значения эффекта ионизации
А-^ИОН= («ИОН ————————— «нейтр)/«нейтрС,
Гдеинейтр, «ион — скорости ультразвука в растворе молекул нейтральной формы и заряженной формы, С—молярная концентрация.
В работе [149] измерялись также объемные эффекты ионизации и изменения сжимаемости. Таким образом, взаимовлияние атомных групп нуклеотидов и нуклеозидов на гидратацию проявляется на расстояниях 0,6—0,8 нм между вандерваальсо — выми поверхностями групп, что соответствует двум-трем слоям молекул воды, т. е. менее чем двум слоям в гидратной оболочке.
Таким образом, из совокупности данных, полученных методом «молекулярного щупа», следует, что гидратационные изменения свойств воды вблизи атомных групп любой природы сосредоточены главным образом в первой гидратной сфере, и, возможно, частично захватывают вторую. Иначе говоря, гидра тационные возмущения структуры воды около молекул растворенного вещества локальны.
 24 октября, 2012
24 октября, 2012  admin
admin 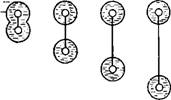
 Опубликовано в рубрике
Опубликовано в рубрике 