Коагуляция под влиянием электролитов является наиболее типичным случаем коагуляции и обычно применяется в технике, когда необходимо разрушить коллоидную систему. Однако очень часто коагуляция обусловливается и другими, чисто физическими факторами — механическим воздействием на коллоидную систему, нагреванием или замораживанием золя, разбавлением или концентрированием. Коагуляция может также происходить под влиянием видимого и ультрафиолетового света, рентгеновских лучей, радиоактивного излучения, при действии электрического разряда и ультразвука. Наконец, разрушение системы может наступить спонтанно при длительном хранении коллоидной системы. К сожалению, особенности и механизм безэлектролитной коагуляции до настоящего времени изучены недостаточно. Между тем для понимания явления коагуляции во всех его аспектах, для составления верного представления о его существе подобные исследования могли бы дать очень миого. Несомненно, что правильный взгляд на явление может быть установлен лишь при всестороннем его изучении, при подходе к нему с самых различных точек зрения.
Рассмотрим кратко те современные сведения, которые имеются о коагуляции золей, происходящей под влиянием наиболее важных физических факторов.
Спонтанная коагуляция. Самсгроизвольиая коагуляция при хранении коллоидных систем может происходить либо в результате медленно протекающих химических изменений в золе, либо вследствие того, что всегда имеется некоторая доля эффективных столкновений частиц, в конце концов приводящих к разрушению системы.
Самопроизвольное понижение устойчивости золя очень сильно зависит от условий, в которых хранится золь. Например, стабильность золя сульфида ртути сравнительно быстро понижается при хранении в открытом сосуде, что объясняется улетучиванием из раствора сероводорода, являющегося стабилизатором свежеприготовленного золя сульфида ртути. При хранении золя сульфида ртути в заполненном доверху и герметически закрытом сосуде золь не только не коагулирует, но становится при хранении даже более устойчивым к действию электролитов. Это можно объяснить тем, что при таких условиях в золе в результате хемосорбционного взаимодействия сероводорода и сульфида ртути вместо мицелл типа
{т [HgS] nSH~ • (я — х) Н*} *Н+
Постепенно образуются более устойчивые мицеллы типа {т [HgS] nHgSj" • 2 (п — х) Н+} 2хН*
Коагуляция в результате механического воздействия наблюдается при интенсивном перемешивании коллоидных систем, при перекачке их по трубопроводам и т. п. Причины коагуляции при механическом воздействии обусловлены, вероятно, временным нарушением адсорбционного баланса стабилизатора у поверхности коллоидных частиц. Такие астабилизованные частицы получают возможность сближаться на расстояние действия молекулярный сил и вследствие этого слипаются друг с другом. Доказательством такого механизма ко’агуляции служит тот факт, что в коагуляте, полученном в результате механической коагуляции, стабилизатора содержится всегда меньше, чем в коагуляте, получаемом при коагуляции электролитами.
Интересно, что системы, более стойкие к механическим воздействиям, обычно более стойки и к действию электролитов. Имеются данные, что механическая устойчивость коллоидных систем связана с их устойчивостью при старении. Связь между всеми этими факторами вполне понятна, так как механическая устойчивость, с одной стороны, и устойчивость лиозоля к электролитам и при хранении, с другой стороны, определяется одним и тем же фактором — свойствами двойного электрического слоя.
Коагуляция коллоидных систем может происходить и в результате вибрационных воздействий и влияния ультразвукового поля. Особенное значение вибрационная коагуляция имеет в технике при получении различных паст, бетонов и других систем. Например, виброобработка бетонной смеси вначале ведет к разрушению в ней коагуляционной структуры и в результате этого к увеличению текучести смеси, что облегчает заполнение смесью форм Однако при дальнейшей виброобработке образуется прочная кристаллизационная структура.
Коагуляцию коллоидных систем в ультразвуковом поле наблюдал еще Дарсинг (1908 г). В дальнейшем было установлено, что в докавитационной области облучение ультразвуком способствует коагуляции, однако с увеличением мощности поля начинает уже преобладать его диспергирующее действие. В ультразвуковых полях малой мощности малые частицы следуют за средой, в то бремя как крупные, обладающие большой инерцией, почти не увлекаются жидкостью. Таким образом, малые частицы как бы «про — шивают» среду и оказываются в поле действия молекулярных сил больших частиц, что приводит к коагуляции. Д. С. Лычников и Г. А. Мартынов установили, что преодоление энергетического барьера и коагуляция возможны лишь, когда амплитуда колебания частиц соизмерима с расстоянием между частицами. Ультра» звуковое поле как бы «перебрасывает» мелкие частицы из вторичного потенциального минимума в первичный, Если частицы нахо
дятся на больших расстояниях друг от друга, то устойчивость не нарушается и золь остается стабильным.
Не так давно было показано, что в осадках подвергнутых ультразвуковому облучению суспензий содержатся цепочки частиц, возникающие, по всей вероятности, в результате поляризационного взаимодействия между частицами. Таким образом, при образовании структур в дисперсных системах под влиянием ультразвукового поля важное значение имеет деформация двойного электрического слоя.
Коагуляция под влиянием электрического поля. Уже сравнительно давно обнаружено, что под действием переменного электрического поля в золях и суспензиях может наблюдаться как разрушение структур, так и образование цепочбк частиц. Особенно
Важно воздействие электрического поля на эмульсии, поскольку оно применяется для обезвоживания нефтяных эмульсий и очистки воды, содержащей примеси минеральных масел.
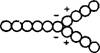
О. Г. Усьяров, И. С. Лавров и И. Ф. Ефремов исследовали влияние переменных и постоянных электрических полей на взаимодействие частиц синтетических каучуков, диспергированных в алифатических спиртах и гексане. Было найдено, что в полярных средах между частицами, находящимися в электрическом поле, возникает притяжение, которое заметно проявляется на расстоянии, в 2—3 раза превышающем размер частиц. В результате образуются линейные агрегаты — цепочки, что не наблюдается в случае неполярного гексана. Это привело к выводу об ответственности за процесс ориентированной агрегации неравновесных электроповерхностных сил, обусловленных деформацией и поляризацией двойного электрического слоя. При взаимодействии цепочек друг с другом по схеме, изображенной на рис. IX, 16, возникают вторичные дендритоподобные структуры. Снятие электрического поля при фиксации частиц в неглубоком потенциальном минимуме приводит к распаду агрегатов или структур; при фиксации частиц з глубокой потенциальной яме такого явления не происходит.
В более поздней работе И. С. Лавров показал, что наложение внешнего переменного поля сравнительно невысокой напряженности на водные суспензии полиакрилонитрила приводит к ориентированному вдоль силовых линий агрегированию частиц.
|
Оооо оэоооо -" |
|
Оооо + — — |
|
Рис. IX, 16. Схема взаимодействия днпольных частиц и образования цепочечных агрегатов. |
Коагуляция при разбавлении или концентрировании коллоидной системы. Наблюдающуюся в некоторых случаях коагуляцию при разбавлении гидрозолей водой можно объяснить десорбцией стабилизующего электролита с поверхности частиц в дисперсионную среду, что обусловливает падение заряда частицы. При этом, конечно, может происходить и гидролиз стабилизатора, вслед-
ствне которого золь может также терять устойчивость. В практике — при разбавлении коллоидной системы технической водой, содержащей электролиты, коагуляцию при разбавлении можМо объяснить и действием электролитов.
Гораздо труднее объяснить коагуляцию при концентрировании коллоидных систем. Правда, при концентрировании коллоидной системы путем выпаривания в ней повышается концентрация электролитов, всегда содержащихся в гидрозолях, что может действовать на систему астабилизующим образом. Однако опыт показал, что коагуляция гидрозоля происходит и в том случае, когда концентрирование проводится с помощью ультрафильтрации, т. е. когда состав дисперсионной среды не меняется.
Некоторые исследователи объясняют коагуляцию золя при концентрировании увеличением чйсла столкновений частиц друг с другом. Однако это объяснение мало соответствует тому факту, что золи проявляют способность к спонтанной коагуляции только тогда, когда их концентрация превышает определенное критическое значение. Можно полагать, что неустойчивость коллоидной системы выше определенной концентрации объясняется увеличением в единице объема содержания не только чужеродного электролита, но и самих коллоидных частиц,, которые должны рассматриваться как поливалентные ионы, а также и содержания соответствующих противоионов. Подобное допущение вполне вероятно. В самом деле, как показал еще Дюкло, коллоидные частицы вносят свою долю — в электропроводность системы, и поэтому есть все основания думать, что заряд этих частиц должен учитываться при вычислении ионной силы раствора.
Коагуляция при нагревании или охлаждении. Нагревание даже до кипения обычно сравнительно мало влияет на устойчивость гидрозолей. Наблюдающееся в отдельных случаях падение агрегатив — ной устойчивости при нагревании объясняется, вероятно, десорбцией стабилизатора с поверхности частицы и увеличением интенсивности броуновского движения. Оба эти фактора способствуют преодолению энергетического барьера при столкновении частиц.
Охлаждение гидрозолей до температур, выше температуры их замораживания, обычно также мало сказывается на устойчивости гидрозолей. Наоборот, охлаждение, сопровождающееся замораживанием гидрозоля, очень часто приводит к его коагуляции, причем коагуляция, как правило, бывает тем более полной, чем ниже температура, до которой охлаждался золь, и чем дольше он пребывал в замороженном состоянии.
По Лоттермозеру, на коагуляцию при замораживании влияет не столько температура, сколько степень превращения раствора в кристаллическую массу. Лоттермозер считает, что при замерзании вода образует между коллоидными частицами микроскопические кристаллы. Вследствие увеличения объема в замороженной системе могут развиваться большие давления. Частицы дисперсной фазы, спрессованные в результате этого между кристалликами, могут деформироваться, приходить друг с другом в контакт и слипаться. Так, в результате чисто механических воздействий, возникающих при замерзании коллоидной системы, может образовываться коагулят.
Иной позиции придерживался А. В. Думанский, считавший, чта при замораживании золя постепенно образуются кристаллики чистой воды, в результате чего в оставшейся незамерзшей части системы происходит концентрирование как золя, так и содержащихся в нем электролитов. Вследствие этого может возникнуть такая большая концентрация электролитов, что произойдет коагуляция. В доказательство правильности этой точки зрения А. В. Ду — манский приводил наблюдения Зигмонди, нашедшего, что коллоидная система при замораживании тем более стойка, чем она устойчивее к влиянию электролитов или удалению воды при высушивании.
Следует заметить, что в результате замораживания и последующего оттаивания. коагулятов гидратов окисей металлов в значительной степени меняются многие их свойства: уменьшается объем осадков,- понижается влажность и улучшаются фильтрующие свойства. Такое изменение свойств коагулятов ценно для аналитической химии, прейаративной радиохимии, химической технологии и для очистки вод, в том числе радиоактивных,
 1 ноября, 2012
1 ноября, 2012  admin
admin  Опубликовано в рубрике
Опубликовано в рубрике 