Предупредить коррозию теплообменной аппаратуры и трубопроводов можно, как уже отмечено, поддерживая такой режим контролируемого накипеобразования, который обеспечивает осаждение на теплообменной аппаратуре защитной пленки карбоната
кальция.
Уменьшить коррозию можно также обработкой воды гексаметафосфатом (ГМФ) или триполифосфатом натрия. Для этого рекомендуется охладительную систему заполнить водой, содержащей 100 г/м3 ГМФ в пересчете на Р2О5 и в течение 5—10 суток заставить ее циркулировать в системе. В дальнейшем концентрацию ГМФ в воде можно снизить до 7—10 г/м3 Р2О5. Сообщается также о возможности осуществления кислотно-фосфатной обработки, заключающейся в подкислении воды до pH=6,5-Н7,0 при одновременном увеличении концентрации гексаметафосфата до 15— 25 г/м3. Большие дозы полифосфатов рекомендуется применять для воды с малой жесткостью (до 2,5—3 мг-экв/л).
Агрессивные свойства воды можно также подавить полностью или резко снизить с помощью силиката натрия, хромата или бихромата калия, нитрита натрия, молибдатов, вольфраматов, аминов, четвертичных солей аммониевых оснований и т. д.
При защите металлов от коррозии силикатами. необходимо применять высокомодульные силикаты. Чем ниже модуль силиката, тем более щелочную среду он создает. Казалось бы, что они и должны быть более эффективными ингибиторами. Однако поскольку защита достигается в основном за счет кремнезема, а не подщелачивания раствора, лучшими защитными свойствами обладают высоко модульные силикаты. Силикаты с модулем меньше 2 малоэффективны, и их применять не следует. Наиболее эффективны силикаты с модулем от 2 до 3,5. При выборе силиката, естественно, существенное значение имеет состав электролита. Для кислых электролитов следует подбирать силикат с меньшим модулем, чем для нейтральных и щелочных.
Силикаты могут применяться как в твердом, так и в жидком виде. Для холодной воды целесообразно применять жидкие растворы силикатов, так как скорость растворения твердого силиката в холодной воде мала. Кроме того, следует учитывать, что растворение силикатов при нормальных температурах и давлениях происходит избирательно, что приводит к понижению модуля в растворе и обогащению кремнеземом нерастворенного осадка. Это связано с процессом растворения, сопровождающимся переходом в раствор основания и выделением аморфного кремнезема:
Na20 • nSi02 + Н20 = 2Na0H*nSi02( (8,41)
Отложение на поверхности аморфного кремнезема препятствует дальнейшему растворению силиката. По этой причине практически полностью растворить высокомодульные силикаты не удается.
Твердые силикаты следует применять только в системах с горячей водой, а растворение самого силиката производить по возможности в ограниченном объеме воды. Образующаяся в результате гидролиза щелочь способна пептизировать выделяющийся кремнезем, переводя его в раствор в виде силиката. Поэтому чем меньше воды будет взято для растворения силиката, тем концентрированнее получится образующаяся щелочь и тем сильнее она будет пептизировать кремнезем, повышая модуль растворенного силиката. Это необходимо учитывать при использовании твердых силикатов в качестве ингибиторов и конструировании системы питания. Питатели, наполненные твердым силикатом, служащие для ввода
силиката в раствор, следует конструировать таким образом, чтобы через них проходила лишь часть воды.
 Силикаты могут быть с успехом применены для защиты стальных трубопроводов в промышленном и коммунальном водоснабжении, а также для защиты отопительных систем, прачечных и др. В последних случаях можно не только уменьшить «ржавость» воды, но и добиться ее умягчения и понижения расхода моющих средств.
Силикаты могут быть с успехом применены для защиты стальных трубопроводов в промышленном и коммунальном водоснабжении, а также для защиты отопительных систем, прачечных и др. В последних случаях можно не только уменьшить «ржавость» воды, но и добиться ее умягчения и понижения расхода моющих средств.
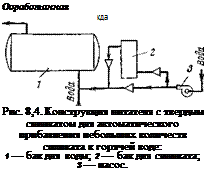
На рис. 8,4 приведена конструкция питателя с твердым силикатом для автоматического прибавления небольших количеств силиката к горячей воде. При большом расходе горячей воды целесообразно применить циркуляционный насос, соединив его с силикатным баком. Наличие в воде небольших количеств магниевых и кальциевых солей благоприятно сказывается на защитных свойствах силикатов. Большие концентрации этих солей, в пределах нескольких процентов, затрудняют растворение силиката в воде и уменьшают стабильность растворов. В воде, применяемой для бытовых нужд, например в прачечных, концентрацию силиката рекомендуется поддерживать на уровне 8н-10 мг/л, а в системах центрального водоснабжения — на уровне 3-4-4 мг/л.
В проточных системах концентрацию силиката следует поддерживать на уровне 154-20 мг/л. Высокомодульный силикат (Л4=3,3) рекомендуется применять для нейтральных и слабощелочных вод, более щелочные силикаты (Л"!=2,4) —для кислых вод (pH=6). Жидкие силикаты вводят с помощью специальных дозиметров ежедневно или через день.
В табл. 8,2 приведены минимальные концентрации силиката, обеспечивающие защиту стали от коррозии в обычной водопроводной воде. С течением времени концентрация силиката в воде может быть снижена до 4—8 мг/л.
|
Таблица 8,2. Минимальные концентрации силикатов (сМин), обеспечивающие защиту стальных водопроводных труб от коррозии
|
Обработку воды целесообразно проводить своевременно, так как коррозия труб, сопровождающаяся отложением продуктов коррозии, уменьшает пропускную способность линий и сокращает срок службы водопроводов.
Для достижения наилучшей защиты желательно, чтобы применяющаяся для охлаждения вода содержала солей не свыше 1004-150 мг/л. Добавление к воде небольших количеств (до 100 мг/л) кальциевых солей благоприятно сказывается на защитных свойствах силикатов.
Опыт показывает, что высокомодульные силикаты предотвращают явление обесцинкования латуней, наблюдающееся обычно в необработанной воде, а также хорошо предохраняют от коррозии оцинкованные трубы и резервуары, содержащие пресную воду.
Силикаты оказываются также эффективными и в циркуляционных системах. Добавление к воде, которая циркулирует при доступе воздуха в охлаждающих, башнях, 25 мг/л высокомодульного силиката достаточно для полного прекращения коррозии стали. Скорость теплопередачи при этом не ухудшается.
Свинцовые змеевики в циркуляционных системах также защищаются от коррозии силикатами при концентрации, равной 2504-500 мг/л. Защита достигается вследствие образования пленки из силиката свинца. Алюминиевые сплавы могут быть защищены от коррозии в проточных системах при концентрации силиката в воде, равной 1504-200 мг/л.
В замкнутых системах в зависимости от агрессивности среды концентрация силиката должна быть повышена в 4—5 раз. Обработка воды силикатами приостанавливает и коррозию стали, когда она находится в контакте с другими металлами. Силикаты дают определенный эффект при защите биметаллической системы из алюминия и меди; применение силикатов совместно с хроматами улучшает эту защиту. Оптимальной концентрацией считается 40 мг/л Na2Si03 и 500 мг/л ЫагСггО^ Добавки в электролит только силиката не прекращают коррозию. Добавки хромата в количестве 1000 мг/л также малоэффективны. Детали, покрытые оловом, судя по электрохимическим измерениям, должны также хорошо защищаться от коррозии силикатами [46].
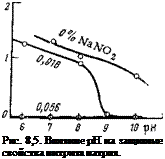
Защита стальных трубопроводов от коррозии в воде может быть также осуществлена с помощью нитрита натрия, являющегося, как было выше показано, хорошим пассиватором. Концентрация нитрита натрия зависит от содержания в воде агрессивных хлорид — и сульфат-ионов и pH воды. Ориентировочное соотношение между концентрацией ингибитора и содержанием хлоридов и сульфатов может быть определено по графику (рис. 5,206). С ростом температуры концентрация нитрита натрия повышается. Зависимость защитных свойств нитрита натрия от pH электролита может быть охарактеризована кривыми, представленными на рис. 8,5.
С понижением pH электролита требуются более высокие концентрации нитрита натрия для защиты системы от коррозии. Наи
более оптимальным значением pH яв — к, т/гвЗ ляется 8-4-9. В электролитах со значением pH <6 нитрит натрия плохо защищает сталь от коррозии, поскольку он восстанавливается при потенциале коррозии и становится сильным деполяризатором. Нитрит натрия хорошо защищает от коррозии сталь, находящуюся в контакте с нержавеющими аустенитными сталями, низколегированными сталями, никелированными и хромированными деталями, но вызывает потускнение меди и коррозию цинка и латуни. Поэтому аппаратуру, содержащую латунные или оцинкованные изделия, защищать нитритом натрия не рекомендуется. Хаммер [160] рекомендует воду обрабатывать нитритом натрия и хлораминами для предотвращения окисления нитрита натрия до нитрата. Концентрация нитрита натрия 200—250 мг/л, значение pH>7.
 Уменьшить агрессивные свойства воды можно также с помощью хроматов. Концентрация хромата или бихромата зависит от состава охлаждающих или передающих энергию жидкостей и их температуры. Для обыкновенной водопроводной воды добавка 0,2-—0,5% хромата вполне достаточна для прекращения коррозии стали при комнатной температуре. При большом содержании в воде хлоридов (от 100 до 1000 мг/л) концентрация хромата должна быть повышена до 2—5%. Хромат, обладающий более щелочными свойствами, имеет преимущество перед бихроматом. При необходимости применять бихромат целесообразно электролит подщелачивать до рН = 8ч-9, добавляя каустическую соду. Для воды с — высоким значением pH можно применять бихромат без дополнительного подщелачивания. С повышением температуры электролита защитные свойства хромата и бихромата значительно понижаются. При температурах 80—90°С концентрация хромата или бихромата в обычной водопроводной воде должна быть повышена до 1-2%.
Уменьшить агрессивные свойства воды можно также с помощью хроматов. Концентрация хромата или бихромата зависит от состава охлаждающих или передающих энергию жидкостей и их температуры. Для обыкновенной водопроводной воды добавка 0,2-—0,5% хромата вполне достаточна для прекращения коррозии стали при комнатной температуре. При большом содержании в воде хлоридов (от 100 до 1000 мг/л) концентрация хромата должна быть повышена до 2—5%. Хромат, обладающий более щелочными свойствами, имеет преимущество перед бихроматом. При необходимости применять бихромат целесообразно электролит подщелачивать до рН = 8ч-9, добавляя каустическую соду. Для воды с — высоким значением pH можно применять бихромат без дополнительного подщелачивания. С повышением температуры электролита защитные свойства хромата и бихромата значительно понижаются. При температурах 80—90°С концентрация хромата или бихромата в обычной водопроводной воде должна быть повышена до 1-2%.
Защита сложных конструкций, содержащих несколько металлов, требует учета электрохимического поведения отдельных электродов в многоэлектродной системе. В таких случаях требуется применять ингибиторы, отличающиеся универсальными защитными свойствами (хроматы, нитробензоаты), или смеси ингибиторов.
В качестве примера рассмотрим электрохимическое поведение конструкции, состоящей из алюминия, стали и меди. В обыкновенной водопроводной воде (содержащей 30 мг/л хлоридов) эта трехэлектродная система работает таким образом, что анодом служит сталь, которая корродирует, а катодами — алюминий и медь. Наблюдающаяся часто на практике сильная коррозия железных ру
башек цилиндров у моторов с водяным охлаждением подтверждает это. При введении в воду 0,2% бихромата калия коррозии подвергаются железо и алюминиевый сплав, а катодом служит латунь. Полное устранение коррозии охладительной системы достигается введением в воду 0,3% бихромата калия. Если вода содержит более высокую концентрацию хлоридов, то рекомендуется увеличить концентрацию бихромата до 2%. Хорошие результаты можно также получить, если добавить в воду наряду с хроматами высокомодульный силикат. В присутствии этих ингибиторов конструкции, состоящие из стали, меди и алюминия, защищаются от коррозии даже при температуре 80—100 °С.
Кроме хромитов и бихроматов калия или натрия можно для этих же целей рекомендовать труднорастворимые хроматы стронция и цинка. В последнем случае часть воды, применяемой для охлаждения системы, направляют в бак, содержащий труднорастворимый хромат стронция или цинка. Вода постепенно насыщается хромат-ионами и при смешивании ее с основной массой ингибирует воду.
В системах, содержащих алюминий, опасным является наличие в воде солей меди. Вторичное их осаждение на алюминиевом сплаве вызывает сильную местную коррозию. Однако имеются сообщения, что в обычной водопроводной воде коррозию можно и в этом случае прекратить при добавлении 0,5—1% хромата калия.
Коррозия алюминия может быть также значительно снижена с помощью хроматов и в щелочных растворах. Введение в электролит 1—5% ЫагСгС>4 практически прекращает коррозию алюминия в 0,1—1%-,ном растворе NaOH.
Хроматы и бихроматы оказываются весьма полезными также при защите от коррозии магниевых сплавов. Введение в воду с малым содержанием хлоридов 1—2% хромата или бихромата калия полностью прекращает коррозию обычно применяемых магниевых сплавов при нормальных температурах. Для защиты сплавов, легированных благородными компонентами, в особенности при высоких температурах (60—80°С), требуются более высокие концентрации хроматов (до 5%).
Серьезной проблемой является защита систем с ватерлинией (резервуары, баки, газгольдеры с гидравлическими затворами) в связи с уменьшением со временем концентрации ингибитора в зоне мениска и развитием коррозии по механизму щелевой. Одними ингибиторами защитить аналогичные системы, как правило, не удается, если только не применять слишком высокие концентрации ингибиторов (до 10—15%).
Подобные системы хорошо защищать от коррозии комбинированным методом защиты при совместном применении ингибиторов и протекторов [46]. Сущность метода заключается в том, что металл на уровне предполагаемой ватерлинии покрывается способом металлизации слоем цинка 0,2—0,3 мм, а в электролит вводится в зависимости от его состава 1—5 г/л бихромата калия.
Минимальное количество бихромата рекомендуется для воды, содержащей не более 30 мг/л хлоридов.
В работах Яковлева [161], посвященных защите систем оборотного водоснабжения, содержатся рекомендации для ингибирования воды: при силикатной обработке для обессоленной воды и вод, содержащих 1,5 мг-экв/л НСОз и 20 мг/л C1-+S04-, рекомендуется вводить 10—20 мг/л силиката в расчете на S1O2; при более высоком содержании бикарбонат-ионов (1,5 мг-экв/л), хлор — и сульфат-ионов (35—550 мг/л) концентрацию силиката необходимо увеличивать до 30—80 мг/л, при 3 мг-экв/л НСОз и 400—650 мг/л (C1-+SOJ") концентрацию силиката следует доводить до 60— 100 мг/л.
Подтверждается эффективность применения смесей ингибиторов, в частности хроматов с фосфатами, а также фосфатов с сульфатом цинка: р_екомендуется при содержании в воде 3—
3,5 мг-экв/л НСОз и 400—600 мг/л (CI-+SO4-) добавлять к воде 15—20 мг/л бихромата калия и 2—4 мг/л сульфата цинка. Для вод, содержащих 3 мг-экв/л НСОз и 400—600 мг/л (CH+SO]") и склонных к осаждению на теплообменной аппаратуре карбонатных осадков, рекомендуют вводить 20 мг/л динатрийфосфата и 20 мг/л бихромата калия или 8 мг/л динатрийфосфата, 12 мг/л бихромата калия и 4 мг/л сернокислого цинка. Последняя смесь, по мнению авторов, дает лучший защитный эффект.
В тех случаях, когда накипеобразование не играет существенной роли, а основная задача заключается в защите системы от коррозии, концентрация полифосфата может изменяться в довольно широких пределах. Обычно это бывает тогда, когда содержание кальция и железа в воде невелико. Концентрации полифосфатов, которые обеспечивают защиту от коррозии, зависят от скорости течения воды, ее состава и температуры. В размешиваемых электролитах, где ингибитор все время подводится к металлической поверхности, резкое замедление коррозии наступает при введении в электролит от 25 до 200 мг/л гексаметафосфата.
В системах, где вода течет с большой скоростью (0,5—2,0 м/с), для прекращения коррозии металла обычно достаточно введения 20—25 мг/л гексаметафосфата натрия. В циркуляционных системах с относительно небольшой скоростью течения воды (до 0,5 м/с) концентрация полифосфата должна быть увеличена в 5—10 раз.
Сталь, находящаяся в контакте с другими металлами, также хорошо защищается от коррозии гексаметафосфатом, при условии усиленного подвода ингибитора к поверхности металла: 25—
50 мг/л полифосфата оказывается достаточным для того, чтобы полностью прекратить коррозию стали, находящуюся в контакте с латунью и медью, в усиленно размешиваемой водопроводной воде.
С повышением температуры воды увеличивается необходимое количество полифосфата. Однако до 100 °С защита всегда достигается при концентрации гексаметафосфата, равной 50—100 мг/л, и при усиленном размешивании электролита.
Наряду с полифосфатами в циркуляционных системах для борьбы с коррозией можно применять и фосфаты. Выбор фосфата зависит от состава воды. Для жестких вод тринатрийфосфат мало эффективен. Монофосфат, по мнению Эванса, дает лучший эффект.
В ряде работ рекомендуется в циркуляционных системах охлаждающую воду обрабатывать смесью гексаметафосфата и хромата [40—50 мг/л (NaPOa)6+20—30 мг/л ЫагСгС^ или
ЫагСггСЬ]. Такая обработка, по мнению авторов, способствует отложению различных кристаллических пленок и предотвращает появление язвенной коррозии. Значение pH следует поддерживать на уровне 6,5н-7.
В работе [162] было показано, что в системах водоснабжения значительного снижения коррозии можно достигнуть посредством обработки воды азотнокислым кальцием, бурой и гексаметафосфатом натрия (табл. 8,3).
Эти результаты представляют интерес в связи с тем, что значительное снижение коррозии достигнуто в относительно концентрированных растворах хлоридов, в которых подавить коррозию небольшими концентрациями ингибиторов довольно трудно. Положительные результаты, несомненно, связаны с осаждением защитных пленок, содержащих кальций.
Роль полифосфатов еще не совсем ясна. Однако предполагают, что они образуют на поверхности металла тонкие фосфатные слои, в состав которых входят ионы защищенного металла, а также ионы кальция. Полифосфаты более эффективны при размешивании электролита, что связывают с постоянным подводом ингибитора и ускорением катодного процесса, который облегчает в связи с за-
|
Та блица 8,3. Скорости коррозии различных металлов в 5%-ной морской воде в присутствии смеси ингибиторов (200 мг/л гексаметафосфата натрия, 100 мг/л кальция, 100 мг/л буры)* (t=20 сут)
* Электролит получали разбавлением синтетической Na2S04 — 4 г/л; MgCl2-6H20 — 20 г/л; СаС12 — 1,2 г/л. морской воды (NaCl — 23 г/л; |
щелачиванием приэлектродного слоя осаждение карбоната кальция.
Многие исследователи обращают внимание на возможность усиления коррозии при применении концентрированных растворов полифосфатов в связи с образованием растворимых комплексов. Кроме того, в воде, которая имеет щелочную реакцию, при полифосфатной обработке иногда обнаруживаются питтинги. Поэтому при фосфатной обработке воды pH рекомендуют поддерживать на уровне 7 или даже несколько ниже.
Исследованием ингибиторов в системах автономного горячего водоснабжения занимались Венцел и Вранглен [163]. В нагревательную систему в здании обычно входят бойлер, в котором вода нагревается и циркулирует через радиаторы, благодаря термической конвекции или с помощью специальных водяных помп. Холодная вода поступает в медный змеевик, вмонтированный в специальную обогреваемую емкость, и после нагрева идет на дальнейшее водоснабжение. Ввиду того что циркуляционная система сообщается с атмосферой, вода обогащается кислородом, который окисляет Fe^ до Fe3* участвующий в процессе катодной деполяризации. Наличие контакта между двумя разнородными в электрохимическом отношении металлами (Fe—Си) приводит к сильной коррозии. Положение еще осложняется тем, что продукты коррозии осаждаются на медном змеевике и сильно ухудшают теплопередачу, что приводит к чрезмерному расходу энергии. Некоторые конструктивные изменения в системе — уменьшение подсоса воздуха, электрическое разъединение стальной емкости от медного змеевика, в котором нагревается вода, — могут быть полезны, однако они не решают полностью проблему, поскольку осаждение продуктов коррозии на змеевике не прекращается. В связи с этим придается большое значение применению ингибиторов коррозии.
Авторы проводили опыты на установке, имитирующей бытовое водоснабжение. Некоторые результаты, полученные авторами, представлены в табл. 8,4. В змеевик поступала холодная вода (жесткость по немецкой шкале 4,5, что соответствует 45 мг СаО на литр), затем нагревалась до 80°С. Концентрация ингибиторов — 1 г/л. В двухкомпонентных смесях ингибиторов (0,5+ +0,5 г/л) сталь более чувствительна к ингибиторам, нежели медь, ее коррозия резко замедляется. Наилучшим ингибитором является нитрит натрия, который к тому же сильно уменьшает отложение осадков на медных змеевиках. Одновременную защиту стали и меди обеспечивает смесь бензоата натрия и нитрита натрия. Хорошие результаты были получены и с помощью одного бензоата натрия, тринатрийфосфата калия, цинк-хромата, [К2СЮ4Х X3ZnCr04-Zn(0H)2], а также смесей двух последних ингибиторов с силикатом натрия. Силикат натрия, а также двойные смеси, содержащие этот ингибитор, уменьшая общую коррозию, склонны, однако, по мнению авторов, вызывать локальную коррозию.
Хотя и обнаружено определенное соответствие между концентрацией продуктов коррозии в воде и скоростью коррозии стали, отложение этих продуктов на меди зависит от специфических свойств самих ингибиторов коррозии. Относительно большие отложения наблюдаются в присутствии гексаметафосфата натрия, силиката, гидразина и смеси силиката с гидразином. Несомненно, что некоторые из этих ингибиторов включаются непосредственно в осадки.
Особый интерес, по мнению авторов, в качестве ингибитора представляет смешанный хромат калия и цинка. Его растворимость равна примерно 1 г/л. Этого количества может оказаться недостаточно для полной защиты от коррозии. Поэтому в начальный момент следует применять более растворимый хромат, а потом подпитывать систему водой, которая пропускается через патрон, содержащий слабо растворимый хромат.
Таким образом, решить вопрос о защите металлов от коррозионного воздействия агрессивной воды или осаждения на теплообменной аппаратуре карбонатных отложений нетрудно. Гораздо
|
Таблица 8,4. Влияние ингибиторов на скорость коррозии малоуглеродистой стали и меди в бытовых нагревательных системах (сИнг=1 г/л)
|
сложее решить задачу, когда требуется, чтобы вода не оказывала коррозионного воздействия на металлы и не была склонна при нагреве к накипи.
![]()
![]()
![]()
 Защита от коррозии и образования накипи
Защита от коррозии и образования накипи
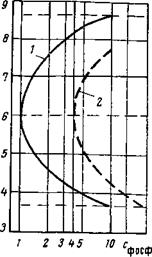
Для того чтобы защитить аппаратуру одновременно от коррозии и накипеобразования, применяют обычно полифосфаты, характеризующиеся общей формулой Na^PxOte+i. Наибольшее применение находят гексаметафосфат натрия (ЫаРОз)б, трипо — лифосфат натрия Ыа5РзОю, три — фосфат натрия МазРО4-10Н2О и дифосфат натрия Na2HP04- 12Н20 Для определения концентрации г е к с а ‘.и е т а ф о с ф а т а натрия в воде рекомендуется пользоваться диаграммой, приведенной на рис.
8,6. По оси ординат откладывается так называемый «индекс стабильности» (2рНнас — pH), по которому можно определить, является ли вода опасной в коррозионном отношении или склонной к накипеобразованию, а по оси абсцисс — количество полифосфата, которое необходимо ввести в воду [153]. При индексе стабильности, равном 6, вода не склонна ни к накипеобразованию, ни к коррозии, и количество полифосфата, которое необходимо ввести в такую воду, ничтожно. При индексе стабильности, большем 6, вода вызывает коррозию; при индексе стабильности, меньшем 6, она становится склонной к отложениям. В обоих случаях концентрация полифосфата в воде должна быть увеличена. Количество полифосфата, подлежащее добавке, определяется по кривым диаграммы. Сплошная кривая соответствует оптимальной концентрации полифосфата, пунктирная — максимально допустимой. На практике наилучшие результаты дает оптимальная концентрация.
Значение pH нас определяется по содержанию кальция в рае — творе, общей щелочности, содержанию солей и температуре воды. Если эти данные известны, то величина рНнас рассчитывается по следующей формуле:
Для природных вод, содержащих меньше 500 мг/л минеральных солей, можно принять, что ц=0,000025 от общего содержания минеральных солей.
![]()
![]()

 Значение pH в выражении для индекса стабильности соответствует концентрации водородных ионов при t—20 °С. Наивысшие концентрации полифосфата, обычно применяемые на практике, составляют б—10 мг/л. Более высокие концентрации полифосфатов применять не рекомендуется, так как они часто приводят преимущественно к карбонатным отложениям.
Значение pH в выражении для индекса стабильности соответствует концентрации водородных ионов при t—20 °С. Наивысшие концентрации полифосфата, обычно применяемые на практике, составляют б—10 мг/л. Более высокие концентрации полифосфатов применять не рекомендуется, так как они часто приводят преимущественно к карбонатным отложениям.
Воду целесообразно предварительно обработать таким образом, чтобы индекс стабильности был близок к теоретическому значению, равному 6. Если состав воды такой, что она может вызвать коррозию, ее целесообразно обработать также другими ингибиторами (щелочи, силикаты), чтобы индекс стабильности привести к 6. Иными словами, рекомендуется применять полифосфаты в комбинации с другими ингибиторами. Смеси фосфатов с силикатами дают очень хорошие результаты. Добавки в воду некоторых органических соединений также уменьшают коррозию металлов и склонность воды к накипеобразованию. Поэтому смеси органических веществ с полифосфатами в настоящее время применяются на практике.
С увеличением температуры воды кривые оптимальных концентраций сближаются с максимально возможными. В таких случаях следует проводить особо тщательный контроль за количеством вводимого полифосфата. С увеличением содержания железа в растворе количество полифосфата должно увеличиваться. Диаграмма рис. 8,6 построена для воды в статическом состоянии, содержащей меньше 2 мг/л железа. Поэтому кривые следует рассматривать в качестве ориентировочных, нуждающихся в корректировании для каждого конкретного случая движения жидкости.
При обработке горячей воды, пригодной для питья, в полевых условиях наиболее эффективным среди всех ингибиторов оказался гептаметафосфат натрия Na9P7032. Концентрация этого вещества, равная 7,9 мг/л, полностью защищала железо от коррозии и исключала накипеобразование.
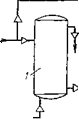
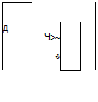
На рис. 8,7 представлена установка, выпускаемая заводами ЧКД «Дукла» в ЧССР, для обработки хозяйственной теплой воды полифосфатами с целью уменьшения коррозии и накипеобразования. Она включает раскисляющий фильтр /, заполненный полуобожженным доломитом, для доведения концентрации СОг до
равновесной концентрации (pH =7,6—8,4), а также удаления взвешенных частиц; магнитный прибор для. магнитной обработки воды 2 с целью ограничения первичной накипи и дозатор ингибитора кислородной коррозии 3, наполненный «атрий-кальциевым полифосфатом, обеспечивающим поддержание концентрации фосфата в воде на уровне 1—4 мг/л.
Вода, обработанная в таких установках, удовлетворяет требованиям чехословацких стандартов (CSN830611 и 830616) на питьевую и теплую хозяйственную воду. Срок службы систем водоснабжения увеличивается при этом в среднем в 3 раза (обычный срок службы стальных труб в теплой хозяйственной воде, не обработанной полифосфатами, — 5—7 лет, а оцинкованных — 7—9 лет).
Установки для обработки воды полифосфатами выпускаются различной производительности: от 13 м3 воды/сут до 380 м3/сут. Число подключаемых бытовых помещений может меняться от 50 до 1440.
 7 сентября, 2015
7 сентября, 2015  admin
admin  Опубликовано в рубрике
Опубликовано в рубрике 