Известно, что многие ингибиторы катионного типа, и в частности амины, являются слабыми ингибиторами коррозии в чистой кислоте. Однако при наличии сероводорода защитный эффект этих же соединений возрастет во много раз (табл. 9,9).
Как видно из данных табл. 9,9, в присутствии сероводорода проявляется синергетический эффект. Таким образом мы встречаемся со своеобразной ситуацией, когда H2S, усиливающий обычно коррозию и водородное охрупчивание стали, облегчает защиту ингибиторами. Аналогичная картина наблюдалась авторами работы [59]. Карбамид, тиокарбамид и их производные не проявляли особых защитных свойств по отношению к стали в 0,1 н. НС1, но в присутствии H2S эти соединения показывали исключительно высокий ингибирующий эффект. Защитный эффект у некоторых производных карбамида и тиокарбамида в HCI+H2S приведен ниже:
 КПИ-2 КПИ-4 ДММ
КПИ-2 КПИ-4 ДММ
4,71•10~я 3,6-10"3 4,16-10_3
220 264 20,9
342 500 500
263 552 1730
Механизм действия этих соединений объясняют возникновением в электролите формальдегида (или тиокарбамида), который вступает во взаимодействие с сероводородом и образует тиоформ — альдегид, полимеризующийся на поверхности металла. Считают, что многие органические добавки способны вступать в химическое взаимодействие с сероводородом, образуя на поверхности металла нерастворимые соединения, представляющие своеобразный фазовый барьер. В частности, подобными добавками являются альдегиды, которые в кислой среде образуют с сероводородом нерастворимые соединения типа тритиона. Эффективными ингибиторами могут быть также соединения, которые не вступают в химические реакции с сероводородом, но способны вытеснять молекулы и ионы сероводорода с поверхности металла. Очевидно, с последними механизмами следует считаться, поскольку теория Иофа и Ле Буше не в состоянии полностью объяснить механизм торможения ингибиторами анодной реакции ионизации металла.
Синергетический эффект H2S обычно объясняют тем, что адсорбированные на железе анионы HS- выполняют роль анионных мостиков, облегчающих адсорбцию ингибиторов катионного типа R+. К последним принадлежат и амины, которые за счет реакции протонизации превращаются в органические катионы. В результате взаимодействия промежуточного комплекса Fe(HS-) с органическими катионами R+ на поверхности металла возникает относительно прочное поверхностное соединение Fe(H—S—R), которое, с одной стороны, не способно служить поставщиком протонов для катодного процесса, а с другой — затрудняет анодную реакцию ионизации металла. Кроме того, адсорбированные катионы ингибитора смещают фі-потенциал в положительную сторону, что также способствует замедлению реакции разряда ионов водорода.
|
Таблица 9,9. Защитный эффект у аминов в присутствии сероводорода
|
Как уже отмечалось, основные неприятности сероводородные среды доставляют не столько из-за коррозии, сколько из-за наво — дороживанию стали, приводящего в конечном счете к охрупчиванию металла и коррозионному растрескиванию оборудования нефтяных и газовых скважин. В принципе, с общей коррозией можно было бы еще мириться или свести ее до минимума. Однако это не спасает положение, ибо уже небольшие скорости коррозии с водородной деполяризацией приводят часто в присутствии сероводорода к сильному охрупчиванию металла. Объясняется это тем, что гидросульфидные ионы сильно замедляют процесс рекомбинации разрядившихся атомов водорода, поэтому их концентрация на поверхности возрастает и проникновение водорода в металл усиливается.
Исследованием влияния H2S на диффузию водорода в металлы занимались Смяловски с сотр. [201], Шрейдер с сотр. [202] и другие. Смяловски изучал проникновение через железную мембрану водорода из газовой фазы, в которой содержалась смесь молекулярного, атомного и ионизированного водорода. Показано, что при высокой разности потенциалов между электродами ионы водорода проникают значительно быстрее, чем атомы водорода. Проникновение водорода усиливается, если к смеси добавить сероводород. Последний оказался промотором и в газовой фазе и ускорял скорость проникновения водорода в 5—7 раз ([H2S] =0,5%).
С увеличением концентрации сероводорода скорость проникновения водорода через металл возрастает и при некоторой концентрации достигается насыщение. На основании этих фактов был сделан вывод, что промотирующее действие H2S носит адсорбционный характер. Поскольку в данном случае через мембрану преимущественно проникали ионы водорода, действие сероводорода, по-видимому, связано не только с тем, что он замедляет процесс рекомбинации йтомов водорода. При адсорбции на поверхности H2S оказывает каталитическое действие и в тех случаях, когда имеется поток ионов водорода к поверхности металла. Заметим, кстати, когда наводороживание происходит в электролитах, не исключено, что в металл диффундируют не агомы водорода, а ионы. Исходя из этих позиций, промотирование сероводородом процесса наводороживания нельзя уже объяснить замедлением процесса рекомбинации. В связи с этим Смяловский для объяснения механизма сульфидного охрупчивания использует представления об адсорбции ионов HS~. При адсорбции ионов HS- ослабляется связь между поверхностными атомами, а это должно облегчить проникновение водорода в металл.
Для борьбы с сульфидным охрупчиванием ингибиторы оказываются исключительно эффективными. Однако здесь также надо проявлять известную осторожность, имея в виду, что не каждый ингибитор, который уменьшает коррозию, уменьшает и наводороживание. Более того, как показал Каваларо с сотр. [203], некото-
зоо
рые ингибиторы, и в частности производные тиокарбамида, хотя и являются ингибиторами коррозии в кислых средах, сильно стимулируют процесс наводороживания. В связи с этим автор предложил считать ингибиторами в данном случае лишь те соединения, которые одновременно тормозят коррозию и предотвращают проникновение водорода в металл.
Предложено много способов борьбы с сульфидным охрупчиванием сталей: они включают как методы изменения состава и структуры сталей, так и обработку среды ингибиторами. Специальной термической обработкой и соответствующим подбором состава стали можно резко снизить наводороживание. Определенные результаты дают и методы поверхностной обработки металла (создание окисных, карбидных и нитридных слоев), которые препятствуют проникновению водорода в металл. Однако применение каждого метода в отдельности не решает полностью проблему. Коррозия и сульфидное охрупчивание сталей лучше всего исключаются при совместном применении сталей определенного состава, подвергнутых специальной термической обработке, и ингибиторов коррозии. В качестве ингибиторов сероводородной коррозии применяют амины жирного и ароматических рядов, а также азот — и серусодержа — щие соединения. Предложено также вводить аммиак с воздухом, которые переводят сероводород в полисульфиды аммония.
В нефтяных скважинах, содержащих сероводород, сама нефть может ингибировать процесс наводороживания. Чем выше содержание нефти в системе, тем меньше наводороживание. Сильная сульфидная хрупкость наблюдается лишь в сильнообводненных скважинах. В малообводненных скважинах даже при большой концентрации сероводорода (500—600 мг/л) коррозионного растрескивания оборудования из-за сульфидной хрупкости почти не наблюдается. Объясняется это тем, что нефть смачивает поверхность металла и предотвращает воздействие на металл водной фазы.
По данным Негреева с сотр. [186], эффективно уменьшают наводороживание стали в двухфазной системе нефть — 3% NaCl (1 : 15) при содержании сероводорода в водной фазе 500—600 мг/л углеводородорастворимый ингибитор диаминдиолеат (высокомолекулярный алифатический диамин с радикалом R, содержащим 10—16 атомов углерода, нейтрализованный олеиновой кислотой) и водорастворимый ингибитор катапин А (параалкилбензилпири — динийхлорид). Углеводородорастворимые ингибиторы содержат активную группу, которая связывает молекулы ингибитора с поверхностью защищаемого металла, и радикалы, которые стабилизируют пленку, включающую и углеводородную фазу (нефть, углеводородный конденсат). В потоке движущейся двухфазной жидкости нефть — 3% NaCl (1:10), насыщенной сероводородом (650 мг/л), наводороживание стали уменьшали катапин А и АПН-2 (смесь солей алифатических аминов).
В наших исследованиях особое внимание было уделено изысканию ингибиторов применительно к газоконденсатным скважинам,
Р, °/о содержащим высокую
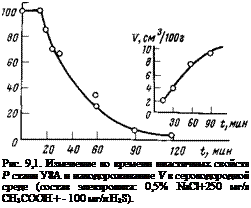 концентрацию сероводорода в добываемом газе. В качестве модельной коррозионной среды выбрали 0,5%-ный NaCl, подкисленный уксусной кислотой (250 мг/л) до pH = 3,5; концентр ация сероводорода 1000—1200 мг/л. Влияние сероводорода на сульфидное охрупчивание определялось на холоднокатаной стали У8А (С —0,79; Si — 0,23; Мп—0,28; Si—0,019; Р— 0,014; Сг—0,22; Ni—0,12 и Си—0,12%) по изменению исходной пластичности стали и по количеству абсорбированного водорода. Содержание водорода в стали определялось — методом вакуумной экстракции. Метод заключается в следующем: образец помещается в предварительно вакуумированный до остаточного давления 10-6 мм рт. ст. сосуд и нагревается до 400 °С. Количество газов, выделившихся из стали при нагреве в вакууме, оценивается по изменению давления с помощью манометрической лампы ПМТ-2 и манометра Мак-Леода. После установления постоянного давления (15—30 мин) выделившиеся газы просасывают через палладиевый фильтр, нагретый до 600 °С, для отделения водорода от примесных газов. По разности давлений судят о концентрации водорода в стали (см3/100 г). Пластичность образцов (ленты) определяли на машине НГ-1-ЗМ.
концентрацию сероводорода в добываемом газе. В качестве модельной коррозионной среды выбрали 0,5%-ный NaCl, подкисленный уксусной кислотой (250 мг/л) до pH = 3,5; концентр ация сероводорода 1000—1200 мг/л. Влияние сероводорода на сульфидное охрупчивание определялось на холоднокатаной стали У8А (С —0,79; Si — 0,23; Мп—0,28; Si—0,019; Р— 0,014; Сг—0,22; Ni—0,12 и Си—0,12%) по изменению исходной пластичности стали и по количеству абсорбированного водорода. Содержание водорода в стали определялось — методом вакуумной экстракции. Метод заключается в следующем: образец помещается в предварительно вакуумированный до остаточного давления 10-6 мм рт. ст. сосуд и нагревается до 400 °С. Количество газов, выделившихся из стали при нагреве в вакууме, оценивается по изменению давления с помощью манометрической лампы ПМТ-2 и манометра Мак-Леода. После установления постоянного давления (15—30 мин) выделившиеся газы просасывают через палладиевый фильтр, нагретый до 600 °С, для отделения водорода от примесных газов. По разности давлений судят о концентрации водорода в стали (см3/100 г). Пластичность образцов (ленты) определяли на машине НГ-1-ЗМ.
В качестве ингибиторов коррозии были исследованы алифатические амины (первичные, вторичные, третичные), гетероциклические амины, соли аминов, производные гексаметиленимина, технические продукты.
Исследования показали, что при концентрации сероводорода 1000—1200 мг/л сталь У8А уже через 2 ч практически теряет пластичные свойства, а количество абсорбированного водорода достигает ~10 см3/100 г (рис. 9,1). Но достаточно ввести в коррозионную среду 30 мг/л хлорида алкилтриметиламмония (ЛБ-4) или диалкиламина (ЛБ-67), чтобы количество абсорбированного водорода упало до 0,25 см3/100 г, а пластичность стали восстановилась до исходного значения (рис. 9,2). Аналогичные результаты можно получить и с помощью хлорида алкилдиметилбензиламмония (ЛБ-3): при концентрации последнего 70 мг/л количество абсорбированного водорода падает до 0,3 см3/100 г, а пластичность сохраняется на уровне 87%. Из солей аминов самым эффективным ингибитором сероводородной коррозии оказался алкилбисокси-
|
Рис. 9,2. Влияние ингибиторов на наводороживание V и пластичные свойства Р стали У8А в сероводородной среде (состав электролита — см. рис. 9,1): 1 — алкилтриметиламмонийхлорид (ЛБ-4); 2 — диалкиламинхлорид (ЛБ-67). |
Рис. 9,3. Влияние смесей ингибиторов на пластичные свойства стали У8А в серо-
водородной среде (состав электролита —см. рис. 9,1):
/ — ИФХАН-1; 2 — ЛБ-64; 3 — смесь 1:2.
этилметиламмонийхлорид (ЛБ-56); при концентрации его всего 7 мг/л пластичность образцов сохраняется на уровне 83%, а количество абсорбированного водорода падает до 0,3 см3/100 г. О защитных свойствах алифатических аминов и солей аминов можно судить по данным, приведенным в табл. 9,10 и 9,11.
Таким образом, четвертичные аммониевые основания и третичные амины, имеющие в своей молекуле длинные углеводородные цепи, являются исключительно эффективными ингибиторами наво — дороживания в присутствии сероводорода.
Был обнаружен также эффект синергизма, заключающийся в том, что смесь двух ингибиторов, например алкилированного амина (ИФХАН-1) и оксиэтилированного амина (ЛБ-64) в соотно-
|
Таблица 9,10. Влияние алифатических аминов на пластичные свойства стали У8А (% от исходного значения) в присутствии сероводорода (1000—1200 мг/л). (Состав электролита: 0,5% NaCl+250 мг/л СН3СООН; pH = 3,6; / = 2 ч.)
|
|
Таблица 9,11. Влияние солей аминов на пластичные свойства стали У8А (условия те же, что в табл. 9,10)
|
шении 1 : 2, оказывается при одинаковых концентрациях намного эффективнее, чем каждый из компонентов смеси в отдельности (рис. 9,3). Аналогичный эффект дает и смесь других ингибиторов (табл. 9,12).
Очень серьезной проблемой является защита оборудования, применяющегося для очистки газа от сероводорода. Оно подвергается часто коррозионному растрескиванию. В настоящее время разработан весьма эффективный ингибитор ИФХАНГАЗ-1, который предотвращает коррозию, коррозионное растрескивание и вспенивание абсорбента (моноэтаноламина), нарушающее технологический процесс. Промышленные испытания этого ингибитора подтвердили его исключительно высокие защитные и технологические свойства. Он рекомендуется к промышленному применению.
В процессах сероочистки следовало бы проверить возможность использования сталей, плакированных алюминием, а там, где не требуется высокой прочности, алюминиевые сплавы. При этом возможно удастся использовать ингибирующие свойства H2S. Извест-
|
Таблица 9,12. Влияние смесей ингибиторов на количество абсорбированного водорода (состав электролита: 0,5% NaCl+250 мг/л СН3СООН; pH = 3,6; сhos = 1200 мг/л; сталь У8А)
|
но, что алюминиевые сплавы очень сильно корродируют в растворе моноэтаноламина (в 15%-ном растворе скорость коррозии достигает 20 мм/ год), однако в присутствии 5 г/л H2S она уменьшается до 0,15 мм/год.
 9 сентября, 2015
9 сентября, 2015  admin
admin 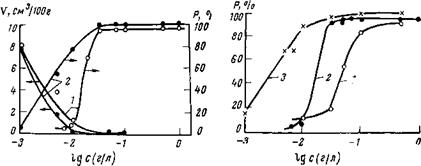
 Опубликовано в рубрике
Опубликовано в рубрике 