Зависимо от наружных критерий может быть три агрегатных состояния вещества, каждое отличается нравом движения частиц, который, в свою очередь, находится в зависимости от типа связи их вместе. По степени распространенности посреди жестких тел выделяется кристаллическое состояние, кое характеризуется строго определенной ориентацией частиц друг относительно друга. Это, в свою очередь, обуславливает и внешнюю форму тела в виде какого-нибудь многоугольника – кристалла. В эталоне кристалл ограничен плоскими гранями, сходящимися в точечных верхушках и прямолинейных ребрах. Такие монокристаллы время от времени встречаются в природе, можно также получить их искусственно. Но большая часть узнаваемых кристаллических тел являются поликристаллическими, т.е. сростками огромного количества маленьких кристаллов, имеют некорректную внешнюю форму но правильное внутреннее строение.
Получение кристаллов из смесей именуют кристаллизацией. Процесс кристаллизации содержит в себе:
1. Образование сверхнасыщенных смесей
2. Появление эмбрионов кристаллизации
3. Рост кристалла
4. Перекристаллизация (сочетание процессов растворения и кристаллизации)
Одним из методов получения сверхнасыщенных смесей является хим взаимодействие веществ. Если в итоге хим реакции появляется малорастворимое вещество, то с течением времени его концентрация становится выше растворимости и раствор по отношению к нему становится сверхнасыщенным.
Кристаллизация включает два процесса:
1. Рост уже имеющихся центров кристаллизации за счет отложения новых молекулярных слоев
2. Появление центров кристаллизации
Зависимо от критерий эти процессы идут с различными скоростями. Если скорость первого процесса существенно больше скорости второго, то образуются большие кристаллы, если напротив – бесформенный осадок, если скорости примерно равны, то появляется полидисперсная кристаллическая система.
Массовому появлению центров кристаллизации содействует резвое смешение прохладных смесей, при неспешном смешении жарких смесей образуются большие кристаллы. Если в сосуде находятся полидисперсные кристаллы 1-го и такого же вещества, то с течением времени будет равномерно происходить рост больших кристаллов за счет растворения маленьких. Это разъясняется тем, что из-за большей удельной поверхности маленьких частиц раствор по отношению к ним является ненасыщенным и напротив. На теоретическом уровне, этот процесс закончится образованием 1-го большого кристалла. Разная скорость роста отдельных граней кристалла обуславливает обилие форм. Исследованием формы кристаллов занимается кристаллография.
Фазовое состояние твердого тела, характеризующееся правильной повторяющейся повторяемостью в пространстве расположения структурных частей именуется кристаллическим состоянием. Все неорганические и органические пигменты являются кристаллическими субстанциями, и большая часть их физических и технических параметров определяется конкретно кристаллическим состоянием.
Зависимо от вида структурных частей и преобладающего нрава связи меж ними кристаллы разделяются на атомные (ковалентная связь), ионные (ионная связь), молекулярные (силы межмолекулярного притяжения) и железные (железная связь). Посреди пигментоввстречаются кристаллы со всеми видами связи, но не всегда можно довольно строго отнести кристалл к тому либо другому виду. В большинстве случаев связи в кристаллах пигментов, по собственной природе являющихся солями либо оксидами, имеют ковалентный либо ионно-ковалентный нрав. Молекулярные кристаллы более свойственны для органических пигментов. Преобладающий нрав связи определяет многие характеристики кристаллов — твердость, температуру плавления, электронные характеристики и др.
То либо другое конкретное размещение структурных частей вещества в пространстве носит заглавие кристаллической структуры. Определенный отрезок, при переносе на который в каком-либо направлении вся кристаллическая структура совмещается сама с собой, именуется трансляцией. Совокупа трансляций образует кристаллическую
решетку.
Важным признаком кристаллов является их симметрия, характеризуемая элементами симметрии (плоскости, оси и центры симметрии). Для кристаллов вероятны 32 разных набора частей симметрии. Это — так именуемые классы симметрии. Параллелепипед, построенный из кратчайших трансляций, которые ориентированы по координатным осям, подходящим симметрии кристалла, именуется простой ячейкой. Углы при ее верхушке и длины трансляций, являющихся ее ребрами, именуются
параметрами решетки. Зависимо от направления координатных осей и соотношения размеров трансляций, из которых образована элементарная ячейка, все классы симметрии, которые вероятны для кристаллических решеток, делятся на 6 систем, именуемых сингониями: кубическая, тетрагональная, гексагональная, ромбическая, моноклинная и триклинная. Кубическая сингония относится к высшей категории симметрии, тетрагональная и гексагональная — к средней, ромбическая, моноклинная и триклинная — к низшей.
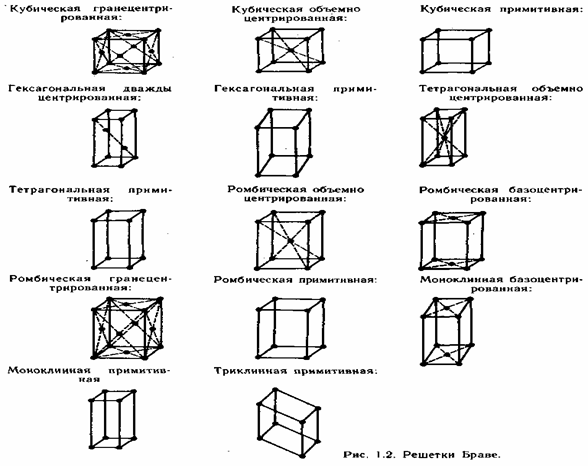
Если простые ячейки, надлежащие 6 сингониям, дополнить, по мере способности, кратчайшими трансляциями, не совпадающими с осями координат, то в простых ячейках появятся дополнительные узлы кристаллической решетки. Эти узлы будут размещаться в пространстве меж верхушками параллелепипеда, представляющего из себя простую ячейку. Они могут размещаться в центрах всех граней,— такая решетка носит заглавие гранецентрированной; в центрах пары обратных граней — базоцентрированная решетка; в центре ячейки — объемноцентрированная решетка. Если в ячейке нет узлов, не считая узлов в верхушках, то ячейка именуется примитивной. Таким макаром, по виду центровки решетки кубической сингонии разделяются на гранецентрированные, объемноцентрированные и примитивные; решетки гексагональной сингонии — на два раза центрированные (два узла на большей большой диагонали) и примитивные; решетки ромбической сингонии — на объемноцентрированные, базоцентрированные, гранецентрированные и примитивные; решетки моноклинной сингонии — на базоцентрированные и примитивные,_Решетка—триклинной сингонии
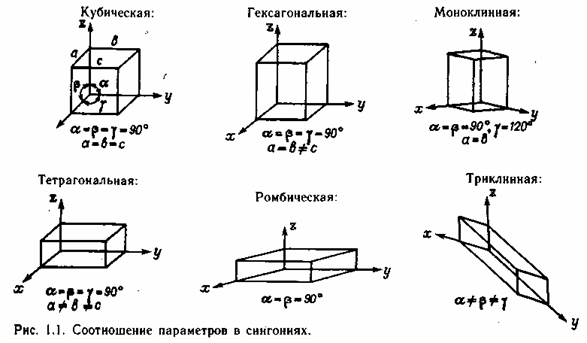
может быть только примитивной. Эти 14 видов кристаллических решеток именуются решетками Браве.
Для кристаллического состояния очень типично явление полиморфизма. Полиморфизм — это способность 1-го и такого же хим вещества существовать в виде 2-ух либо нескольких кристаллических структур (модификаций). Переход из одной кристаллической модификации в другую именуется полиморфным перевоплощением. Кристаллические модификации 1-го и такого же вещества обозначаются знаками греческого алфавита в порядке увеличения температуры размеренного состояния данной модификации. Но в химии пигментов для обозначения тех либо других модификаций нередко пользуются исторически сложившимися наименованиями. Любая кристаллическая модификация размеренна в определенном температурном интервале. Переход из одной модификации в другую сопровождается термическим эффектом. Переход высокотемпературной модификации в низкотемпературную сопровождается выделением теплоты, оборотный переход — поглощением теплоты. Переход одной кристаллической модификации в другую характеризуется обычно очень высочайшим значением энергии активации. В случае перегрева поблизости температуры полиморфного перевоплощения, а при переохлаждении даже при очень большенном удалении от нее, число структурных частей, владеющих достаточной энергией для перестройки в пространстве, невелико, тем паче, что поглощенная жестким телом энергия, даже сравнимо большая, распределяется меж колоссальным числом
структурных частей. Потому возможность полиморфного перевоплощения малозначительна. Таким макаром, при данных критериях могут существовать метастабильные кристаллические модификации, т. е. модификации относительно устойчивые, но термодинамически неравновесные.
Познание и внедрение вероятных полиморфных перевоплощений того либо другого хим соединения, используемого в качестве пигмента, позволяет направленно регулировать его физико-химические характеристики, которые у различных модификаций могут очень различаться. Поближе по свойствам кристаллы в этом случае, если они относятся к одной категории симметрии, и тем паче к одной сингонии. Переход от низшей категории симметрии к средней вызывает в данном случае резкое расширение полосы поглощения света в длинноволновую область, что вызывает существенное изменение расцветки пигмента.
Модификации, относящиеся к одной сингонии, могут достаточно существенно различаться по ряду физико-химических параметров — по плотности, показателю преломления, твердости и прочности кристаллов. К примеру диоксид титана анатазной модификации имеет плотность 3840 кг/м3 и показатель преломления 2,3, а рутильной модификации — 4200 кг/м3 и 2,6 соответственно. Рутил характеризуется большей твердостью, чем анатаз, и большей склонностью к явлению фототропии (обратимому изменению расцветки под действием света в присутствии маленьких количеств примесей), тогда как анатаз проявляет огромную фотохимическую активность, ежели рутил.
Получая в итоге синтеза ту либо иную кристаллическую модификацию либо смесь модификаций, можно в достаточно широких границах разнообразить многие характеристики пигмента.
Некие соединения, близкие по хим составу, могут создавать однообразные кристаллические структуры. Это явление именуется изоструктурностью. Если надлежащие структурные единицы изоструктурных соединений способны к образованию близких по нраву связей и не достаточно отличаются по объему, то эти соединения могут создавать смешанные кристаллы. Такие хим соединения именуют изоморфными.
Явления изоструктурности и изоморфизма обширно употребляют при синтезе пигментов для управления процессами кристаллизации и увеличения стойкости метастабильных кристаллических модификаций (к примеру, при синтезе лимонового свинцового крона для стабилизации ромбической модификации хромата свинца его соосаждают с изоморфным ему более устойчивым сульфатом свинца).
Многие характеристики реальных кристаллических веществ, в отличие от безупречных кристаллов, в большой степени зависят от изъянов кристаллической структуры. Различают точечные, линейные, поверхностные и большие недостатки. Точечным недостатком может являться вакансия, т. е. отсутствие атома либо иона в узле кристаллической решетки, либо атом либо ион (принесенный либо свой), размещающийся меж узлами. Линейные недостатки, либо дислокации,—
это нарушение периодичности расположения атомов либо ионов повдоль какой-нибудь полосы. Длина дислокации соизмерима с размерами кристалла, а ширина не превосходит нескольких межатомных расстояний. Поверхностные недостатки — это нарушение периодичности кристаллической решетки, распространяющееся в 2-ух направлениях. Толщина поверхностных изъянов не превосходит нескольких межатомных расстояний. Большие недостатки —
это макродефекты, представляющие из себя включения в кристалл частиц другой фазы, микрополости, поры. Недостатки появляются как в процессе процесса кристаллизации, так и в следующих процессах термообработки и механического измельчения, вызывающего деформацию кристаллов.
Все виды изъянов кристаллической решетки оказывают существенное воздействие на характеристики пигментов. Точечные недостатки оказывают влияние на цвет кристаллов, показатель преломления, плотность, электронную проводимость, магнитные характеристики. Наличие в кристаллической решетке сторонних атомов, даже в очень малых количествах, может вызывать явление фототропии — обратимого конфигурации параметров кристалла под действием света. Так, диоксид титана анатазной модификации, содержащий малозначительное количество примесей железа, хрома и никеля, под действием света приобретает коричневую расцветку, исчезающую в мгле.
Поверхностные недостатки делят кристаллы на отдельные блоки различной формы и размеров, разориентированные друг относительно друга на некий угол, что присваивает кристаллам мозаичное строение. Выходящие на поверхность кристаллов поверхностные недостатки и дислокации вызывают ее микронеоднородность. Нарушение упорядоченности расположения атомов либо ионов на поверхности по местам выхода линейных либо поверхностных изъянов можно рассматривать как микрообласти с бесформенным состоянием, характеризующимся завышенным припасом поверхностной энергии.
От больших изъянов зависит крепкость кристаллов, что играет важную роль в процессах механического измельчения и диспергирования пигментов.
Точечные недостатки вызывает нестехиометричность соединения как в объеме кристалла, так и на его поверхности. А именно, такая нестехиометричность свойственна для диоксида титана: из-за наличия вакансий содержание кислорода в кристаллической решетке может быть меньше стехиометрического на 0,1 моль. Нестехиометричность свойственна для оксида цинка, в каком содержание кислорода может превосходить стехиометрическое. Отклонение от стехиометрии, вызванное наличием в кристаллической решетке точечных изъянов, наблюдается и у других, оксидных пигментов (оксидов железа, свинца и др.).
Присутствие в кристаллической решетке сторонних ионов влияет на поверхностные характеристики пигментов. Если сторонний ион имеет однообразный заряд с ионом кристаллической решетки и отличается от последнего ионным радиусом, наблюдается деформация решетки. Такие недостатки в приповерхностном слое вызывают возникновение участков с завышенной поверхностной энергией, что оказывает влияние на адсорбционные характеристики поверхности.
 19 октября, 2014
19 октября, 2014  Meneger
Meneger  Опубликовано в рубрике
Опубликовано в рубрике  Метки:
Метки: 