Прежде всего рассмотрим отличия в структуре граничных слоев, обнаруживаемые для воды вблизи гидрофильных и гидрофобных поверхностей. Методами численного эксперимента показано, что в прослойках, ограниченных гидрофобными стенками, возникает характерная картина ориентации диполей во-
Рис. 1.1. Зависимость средней вязкости воды (т)) в тонких кварцевых капиллярах от их радиуса (г) при 21 °С:
Г)о — вязкость объемной воды
Ды параллельно поверхности [2—10]. При этом эффект упорядоченной ориентации распространяется на
О 0,2 0,4 о, б о, В 1,0 значительное расстояние, г>мт т. е. является дальнодейст-
Вующим. Такое расположение молекул воды приводит к снижению плотности вблизи стенок и повышает подвижность молекул в тангенциальном направлении, что можно интерпретировать как снижение вязкости граничных слоев. Макроскопически этот эффект может проявляться как скольжение воды по гидрофобной подложке.
Этот вывод хорошо согласуется с результатами прямых измерений [11]. Количественно исследовать эффект скольжения воды удалось благодаря применению микронных кварцевых капилляров с молекулярно гладкой гидрофобизованной (метилированной) поверхностью. На основании таких опытов были получены средние значения коэффициента скольжения воды по гидрофобной поверхности, равные 30 см3/(Н-с). Этому значению отвечает падение вязкости в тонком пристенном слое воды примерно на порядок.
В случае прослоек, ограниченных гидрофильными поверхностями, ситуация меняется. Так, вблизи поверхности ионного кристалла NaCl диполи воды ориентируются нормально к поверхности — главным образом за счет электростатического притяжения между ионами Na+ и отрицательно заряженными атомами кислорода воды [5]. Аналогичный вывод следует также из других численных экспериментов [6, 8]. В отличие от гидрофобных стенок, здесь имеет место некоторое повышение плотности воды и снижение тангенциальной подвижности ее молекул в слоях толщиной в несколько нанометров, что должно проявляться макроскопически как рост вязкости граничных слоев воды.
|
|
Этот теоретический вывод также находит экспериментальное подтверждение. На рис. 1.1 показаны результаты прямых измерений вязкости воды в тонких гидрофильных кварцевых капиллярах и тонкопористых стеклах [12]. С уменьшением радиуса капилляров средняя вязкость воды растет. При интерпретации результатов измерений следует, однако, учитывать возможное влияние встречного электроосмотического потока под действием потенциала течения (электровязкость). Пунктирной
кривой показаны результаты расчетов электровязкости по теории С. С. Духина с сотр. [13], использующей нелинеаризован — ное уравнение Пуассона — Больцмана. Для расчетов использованы значения потенциала поверхности кварца г|зі=—150 мВ, измеренные в таких же капиллярах [14]. Максимум влияния электровязкости, как видно из рис. 1.1, должен был бы приходиться на радиус капилляров ~0,3 мкм. Отсутствие влияния электровязкости в опытах с капиллярами связано с тем, что измерения велись при практически постоянной длине столбика жидкости. Смещение мениска при проведении измерений не превышало 100 — 200 мкм. Объем вытекающей и втекающей жидкости составлял при этом всего Ю-11—Ю-12 см3, что было недостаточно для формирования сколько-нибудь заметного потенциала течения.
Результаты измерений вязкости в пористом стекле (г= = 10 нм) показаны точкой а на рис. 1.1. В этом случае влияние электровязкости было мало в связи с сильным перекрытием двойных электрических слоев (ДЭС). Теория дает в этом случае электровязкостную поправку, не превышающую долей процента [13].
Повышение вязкости тонких прослоек воды между гидрофильными поверхностями кварца — хорошо установленный экспериментальный факт, следующий не только из этих измерений, но и из более ранних экспериментов [15], а также измерений на глинах [16], на силикагелях [17], экспериментов с ядерными фильтрами [18] и пористыми стеклянными мембранами [19—21].
Другим характерным свойством связанной воды — воды граничных слоев вблизи гидрофильных поверхностей, по современной терминологии, — является ее пониженная, по сравнению с объемной водой, растворяющая способность. Это также является следствием измененной структуры воды. Как известно, под действием внешнего давления и температуры меняется растворяющая способность и объемной воды. Пониженную растворяющую способность граничных слоев воды использовали, в частности, для количественных оценок содержания связанной воды в дисперсных системах. При этом в качестве индикаторов, слабо проникающих в связанную воду, брали электролиты и сахарозу [1].
Теория нерастворяющего объема, развитая Б. В. Дерягиным на основе представления Г. Баккера об анизотропии давления в граничном слое [22], позволила объяснить и количественно описать этот эффект, положенный в настоящее время в основу методов обратноосмотического разделения растворов на тонкопористых мембранах. Из теории следует, в частности, что повышение концентрации должно приводить к постепенному уменьшению толщины граничного слоя, разрушению особой
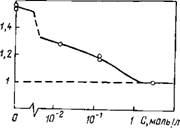
Рис. 1.2. Зависимость вязкости воды в гоиких порах (г=10 нм) стеклянной мембраны от концентрации электролита
Структуры. Это связано с повышением разности между осмотическим давлением в объемной части и в граничном слое раствора. На рис. 1.2 приводятся результаты измерений вязкости во — и водных растворов различной концентрации в порах стеклянной неселективной мембраны (г = 10 нм). Вязкость рассчитывали по изменению скоростей фильтрации через пористое стекло, причем в качестве эталонной жидкости брали неполярный ССЦ, вязкость которого практически не меняется в порах такого радиуса. При повышении концентрации электролита, как видно из рис. 1.2, постепенно уменьшается разница между вязкостью раствора в тонких порах (г]) и в объеме (г)0). При концентрации выше 0,1 моль/л вязкость раствора в порах такая же, как в объеме, т. е. граничные слои заметной протяженности отсутствуют.
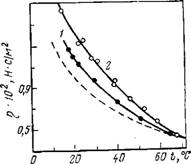
Разрушение граничных слоев воды происходит также и при повышении температуры, когда тепловое движение размывает упорядоченную под влиянием гидрофильной поверхности сетку водородных связей. На рис. 1.3 показана температурная зависимость вязкости воды в тонких гидрофильных капиллярах (кривые 1 и 2) в сравнении с температурной зависимостью вязкости объемной воды (пунктир). При повышении температуры до 65—70 °С отличия вязкости от объемных значений перестают ощущаться, что означает резкое уменьшение толщины граничных слоев. Как было показано ранее, при этом прекращается также термоосмос воды в тонких порах [23] и заметно растет (из-за снижения вязкости) скорость фильтрации воды в пористых телах и мембранах [18, 20].
Влияние температуры на структурные эффекты хорошо прослеживается и в опытах с пленками воды на поверхности кварца. При повышении температуры, как было показано ранее [30], постепенно уменьшается толщина полимолекулярных адсорбционных пленок, что обусловлено утончением граничных слоев воды. При 65—70 °С толщина пленок падает до монослоя, что хорошо согласуется с результатами других обсуждавшихся выше экспериментов.
|
|
Тепловое разрушение граничных слоев воды проявляется и в снижении устойчивости гидрофильных коллоидных систем— таких, как золи кварца и алмаза [24, 25]. Стабилизация коллоидных систем за счет адсорбции неионогенных ПАВ свя
зана с образованием граничных слоев воды вблизи полярных групп молекул ПАВ [26]. Повышение температуры ведет и в этом случае к потере устойчивости золей [27] и мицеллярных растворов [28, 29].
Если при повышении температуры граничные слои разрушаются, то ее понижение должно, напротив, приводить к усилению структурных эффектов. Это проявляется, в частности, в граничном плавлении льда. Этот известный эффект можно наблюдать в строго цилиндрических тонких капиллярах с молекулярно гладкой поверхностью [31]. При приближении температуры к точке плавления столбики льда становятся легко подвижными в связи с образованием у поверхности лед — кварц незамерзающей водной прослойки, обладающей свойствами вязкой ньютоновской жидкости. При понижении температуры скорость сдвига столбиков льда падает в связи с уменьшением толщины незамерзающих прослоек и ростом их вязкости.
Учет особенностей незамерзающих прослоек позволил получить (на основе термодинамики необратимых процессов и теории расклинивающего давления) уравнения течения, связывающие скорость переноса влаги в мерзлых грунтах и пористых телах с теплотой фазового перехода лед — вода [32]. Более подробно эти вопросы рассматриваются в разделе 6 этой же главы.
Кроме вязкости и растворяющей способности меняется также и плотность воды в граничных слоях. Однако эти изменения количественно выражены слабее, что связано с особенностями структуры объемной воды. Так, при повышении температуры от 20 до 55 °С вязкость объемной воды падает вдвое, в то время как плотность снижается всего на 1%. В этом смысле вязкость является более структурно-чувствительным свойством, что и позволило посредством относительно более простых измерений вязкости изучить ряд структурных особенностей граничных слоев воды.
|
|
Получить надежные оценки плотности граничных слоев воды далеко не просто. Ранее для таких измерений использовались методы дилатометрии. Основную трудность здесь представляет выбор эталонной жидкости, кото-
Рис. 1.3. Зависимость средней вязкости воды (гі) в капиллярах от температуры:
Г=0,17 мкм (/) и 0,05 мкм (2)
рая должна заполнять тот же объем в пористом теле, что и исследуемая жидкость, и не изменять свою плотность заметным образом вблизи межфазной поверхности. Применение этого метода к гидрофильным коллоидам давало, как теперь становится ясным, сильно завышенные значения плотности «связанной» воды, доходившие до 1,3—2,5 мг/см3 [1].
Не зависят от выбора эталонной жидкости методы, основанные на измерении теплового расширения воды, заполняющей тонкие поры [33]. Для исследований брали высокодисперсные порошки белой сажи и рутила с низким коэффициентом теплового расширения. Порошок запрессовывали для получения плотной упаковки и малых пор под давлением около 108 Па в сосуд из инвара — сплава также с очень низким коэффициентом теплового расширения («Ю-6 град-1). Пористость упакованного порошка составляла около 0,5, что отвечало среднему радиусу пор г=5 нм. Порошок заполняли под вакуумом предварительно обезгаженной водой. Контроль за отсутствием остаточного воздуха в порошке проводили путем проверки сжимаемости системы.
|
|
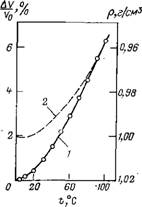
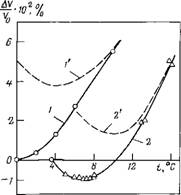
Определенное положение мениска в мерном капилляре устанавливали путем испарения части жидкости. После этого следили за смещением мениска, изменяя температуру термостата, в котором находился прибор. На рис. 1.4 показана зависимость относительного изменения объема жидкости в порах AV/Vо (где Vo — объем жидкости при Т=273 К) от температуры Т. Полученные зависимости (кривые 1 и 2) качественно отлича-
|
Рис. 1.4. Тепловое расширение воды в тонких порах: 1 — Н20; 2 — D20; /’, 2′ — ход теплового расширения объемной жидкости |
Рис. 1.5. Совмещение графиков теплового расширения воды в тонких порах (/) и объемной воды (2) в области температур выше 80 °С
Ются от объемных (пунктирная линия), что свидетельствует об измененной структуре как Н20, так и D2O в тонких порах. Так, НгО в тонких порах не обнаруживает максимума плотности при 4°С, а максимум плотности D20 сдвинут на 4 градуса в низкотемпературную сторону. Эффекты не связаны с влиянием растворенных веществ, так как извлеченная из пор вода восстанавливала свои объемные свойства.
Эти эксперименты, хотя и демонстрировали отличие свойств воды от объемных, еще не. позволяли определить плотность воды в тонких порах. Для этого необходимо было иметь хотя бы одну реперную точку на кривой AV/Vo(T), для которой плотность была бы известна. Исходя из обсуждавшихся выше данных, можно было ожидать, что при температуре выше 70— 80 °С вода в тонких порах примет структуру объемной воды.
На рис. 1.5 показаны результаты экспериментов [34], выполненных в более широком, чем ранее, интервале температур: от 0 до 90 °С. Это позволяет совместить кривые теплового расширения воды в тонких порах (./) и объемной воды (2) в области температур 80—90 °С. Теперь, зная плотность объемной воды, можно было построить шкалу плотностей р. В результате оказалось, что средняя плотность воды в тонких (г = 5 нм) порах вблизи гидрофильной поверхности кварца при 20 °С была выше примерно на 1,5%. При повышении температуры отличия плотности уменьшаются, составляя около 1% при 35 °С.
В еще более тонких порах этот эффект может быть, вероятно, еще более значительным. Однако достижение плотной упаковки частиц более высокодисперсных порошков представляет значительные трудности. Эту трудность удалось преодолеть недавно, используя метод послойного вибропрессования [35]. В этой работе исследовали высокодисперсные порошки аэросила, частицы которого не обладают, в отличие от исследованных ранее образцов [33, 34], внутренней пористостью. Это позволяет отнести полученный результат только к воде в промежутках между частицами аэросила. Средний радиус пор при пористости 0,5, достигнутой вибрационной упаковкой порошка, составлял около 5 нм. Полученная зависимость AV/Vo От Т для аэросила совпадает с кривой 1 на рис. 1.4, что указывает также и на малый вклад в обнаруживаемые эффекты внутренней пористости частиц.
Ориентирующее действие на дипольные молекулы воды гидрофильных подложек должно приводить к анизотропии прослоек и, как следствие, к их двойному лучепреломлению (ДЛ). Измерения ДЛ были выполнены для тонких прослоек воды, содержащихся в осмотически набухших пластинчатых частицах глины (Na-монтмориллонит) [36]. Среднюю толщину водных прослоек h, изменявшуюся при приведении образца в контакт с растворами NaCl различной концентрации, определяли методом рентгеновской дифракции. Используя данные для ДЛ твердой фазы частиц монтмориллонита, получили значения разности показателей преломления для обыкновенного и необыкновенного лучей (D-линия натрия) An = 0,004ч-0,003, мало зависящие от толщины прослойки h. Большим значениям Да отвечали меньшие значения толщины (h = 4,5 нм), а меньшим An — большие h (12 нм). Из-за возможной неточности в значении ДЛ для частиц глины могли снизиться полученные значения An, ио не более чем до Ап=0,002 — для всех значений H. Поправка на поляризацию воды в поле двойного электрического слоя не превосходила 10% наблюдаемого эффекта.
Заметим, что для тонких водных прослоек между частицами монтмориллонита характерно повышение вязкости при уменьшении h [16] и понижение диэлектрической проницаемости ео. В работе [37] получены значения ео = 23-^-25 для прослоек толщиной h = 5-ь8 нм. Хэкстра и Дойл [38] получили ео = 35—40 для А= 1,5-5-1,8 нм и е0 = Зч-4 для А = 0,5-ь0,6 нм. Несмотря на некоторые количественные различия полученных оценок, они явно указывают на ограничение вращательной подвижности молекул воды в тонких прослойках. Повышение температуры, как и следовало ожидать, приводило к росту измеренных значений ео, приближая их к объемному значению для воды (е0 = 80).
Понижение диэлектрической проницаемости граничных слоев воды следует также из молекулярно-динамических оценок изменений вращательной подвижности диполей воды [4] и подтверждается исследованиями структуры воды в тонких прослойках методом неупругого рассеяния нейтронов и ЯМР. Так, для дисперсий кремнезема времена релаксации молекул воды в граничном слое 1 нм в 5—10 раз превышают объемные значения [39]. Методом электронного спинового резонанса показано, что подвижность спиновой метки снижается с уменьшением радиуса пор силикагеля от 5 до 2 нм [40].
Анизотропия тонких прослоек воды между гидрофильными поверхностями следует и из результатов исследований другими, независимыми методами. Так, для граничных слоев воды вблизи поверхности сферических частиц кремнезема радиусом от 10 до 80 нм методом спиновой релаксации ядер 170 и 2Н обнаружено снижение трансляционной подвижности молекул воды в тангенциальном направлении на порядок, а в направлении по нормали к поверхности — на два порядка по сравнению с объемной водой [39].
• Структурные изменения граничных слоев воды ведут к изменению их температуропроводности [41]. Отклонения температуропроводности от объемных значений в сторону снижения начинают обнаруживаться при толщине водной прослойки между сферической (с радиусом кривизны около 1 м) и плоской пластинами плавленого кварца менее 1 мкм. При наименьшей в проведенных опытах толщине прослойки А = 0,03 мкм температуропроводность снижалась примерно на 30%. Этот эффект был объяснен усилением энергии межмолекулярных связей в граничных слоях воды, что подтверждается и исследованиями ИК-спектров воды в тонких прослойках и пленках.
 24 октября, 2012
24 октября, 2012  admin
admin 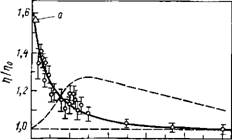
 Опубликовано в рубрике
Опубликовано в рубрике 