Сиккативы — это соли монокарбоновых кислот (мыла). Они служат катализаторами процесса аутоокнслнтельной полимеризации растительных масел, продуктов их обработки и модификации, а также маслосодержащих пленкообразующих веществ, катализаторами отверждения ненасыщенных полиэфиров, полиуретанов и других олигомеров.
Свойства применяемого сиккатива оказывают значительное влияние на механизм аутоокислительного превращения маслосодержащих материалов. В свою очередь свойства самих сиккативов сильно зависят от применяемых для их получения материалов, а также от способов их синтеза.
Сиккативы классифицируют по химическому составу, по способу получения и механизму действия. По химическому составу сиккативы различают в зависимости от содержания в них металла и солеобразующей кислоты. Наиболее распространены сиккативы, содержащие свинец, марганец, кобальт, и менее — содержащие кальций, цинк, железо, стронций и др. Соответственно различают свинцовые, марганцевые, кобальтовые и другие сиккативы.
Сиккативы могут содержать один активный металл (монометаллические) или несколько металлов (полиметаллические). Примерами полиметаллических сиккативов являются свинцово- марганцевые, свинцово-марганцево-кобальтовые, свинцово-мар — ганцево-кальциевые и т. п.
В зависимости от входящей в состав сиккативов органической кислоты различают нафтенаты — соли нафтеновых кислот, Линолеаты — соли жирных кислот льняного масла, резинаты — ■соли смоляных кислот канифоли (в основном абиетиновой), Таллаты — соли жирных кислот таллового масла, октаты — •соли 2-этилгексановой (октановой) кислоты.
По способу получения сиккативы разделяют на плавленые и осажденные.
По механизму действия сиккативы делят на две группы: первичные (истинные) сиккативы и вспомогательные (промоторы).
К первичным сиккативам относятся соли металлов переменной валентности (Со, Мп, Pb, Fe и др.), у которых состояние высшей валентности менее устойчиво, чем низшей.
При контакте маслосодержащих пленкообразователей с кислородом воз — Духа образуются гидропероксидные соединения, которые под действием иона металла распадаются на свободный радикал и ион:
ROOH + Co2+ ^ RO + Co3++OH7
Образовавшийся ион Со3+ может также разрушать гидропероксидные соединения:
ROOH + Со3+ —» ROO + Со2+ + Н + и взаимодействовать с а-метиленовыми группами жирных кислот:
••• — Сн2-сн = СН — ■• +Со3+ — .. — СН-СН = СН—- f
+ Со2+ + Н+.
В присутствии ионов разных металлов реакции образования пероксидов и их распад ускоряются, но в различной степени. Так, ионы кобальта в большей степени ускоряют процесс образования пероксида, а марганец более эффективно его разрушает; свинец ускоряет образование гидропероксидов, но не влияет на процесс их распада. Поэтому, сочетая в определенных соотношениях сиккативы на основе разных металлов, можно более эффективно влиять на скорость отверждения покрытия. Так, в присутствии марганцевого сиккатива льняное масло высыхает за 12, в присутствии свинцового — за 26, а при введении в это же масло их смеси — за 7 ч. Следует отметить, что в присутствии антиоксидантов и сернистых соединений, содержащихся в некоторых растворителях, активность сиккатива может снизиться.
Количество вводимого в масло сиккатива влияет на процесс отверждения покрытия. При увеличении концентрации сиккатива ускоряется высыхание до определенного предела, выше которого активность снижается. Для каждого сиккатива существует некоторая оптимальная концентрация (в пересчете на металл). Например, для кобальтовых, марганцевых сиккативов она составляет в зависимости от вида пленкообразующего вещества примерно 0,025—0,1%.
Активность кобальтовых, марганцевых и свинцовых сиккативов повышается при добавлении к ним промоторов (вспомогательных сиккативов). К ним относятся соли карбоновых кислот и металлов с постоянной валентностью: кальция, бария, цинка и отчасти свинца. Эти соединения, не ускоряя процесс взаимодействия масла с кислородом, оказывают активирующее действие на первичные сиккативы. Вторичные сиккативы способствуют более равномерному высыханию покрытия по толщине и повышению стабильности первичного сиккатива.
Сиккативы в маслосодержащих пленкообразующих веществах не должны терять растворимость длительное время.
Качество лакокрасочного материала и покрытия во многом зависит от совместимости сиккатива с пленкообразующими веществами. В связи с этим очень важно, чтобы сиккатив хорошо растворялся в маслах и растворителях.
Нафтенаты, линолеаты и резинаты свинца, марганца, кобальта и указанных металлов в различных сочетаниях легко растворяются в маслах при нагревании (например, резинат марганца при 120—150°С), а также в растворителях.
Осажденные нафтенаты имеют более светлый цвет и отличаются более постоянным содержанием активного металла по сравнению с плавлеными сиккативами. Линолеатные сиккативы сообщают маслосодержащим пленкообразующим веществам более высокую эластичность, но меньший глянец, чем резинатные сиккативы. Наибольшее распространение получили сиккативы на основе свинца, марганца и кобальта. В последнее время разработаны сиккативы на основе синтетических жирных кислот, содержащих от семи до девяти атомов углерода (С7—С9). Такие сиккативы имеют более светлый цвет, чем линолеаты, и лучше растворяются в пленкообразующих веществах. Использование синтетических жирных кислот для получения сиккативов представляет интерес с точки зрения расширения сырьевой базы и замены растительных масел.
Сиккативы получают двумя способами: сплавлением и осаждением из раствора. Преимуществом способа сплавления является его простота.
Сиккатив образуется в результате взаимодействия соответствующей кислоты и соединения, содержащего активный металл (оксиды, гидроксиды, различные соли) при нагревании:
2R — СООН + РЬО — (RCOO)2Pb + Н20.
Сиккатив получается в виде вязкой массы; при этом не удается ввести в него металл в стехиометрическом соотношении. Возможно также протекание побочных реакций, приводящих к образованию основных солей, растворимость которых отличается от растворимости сиккатива.
Наиболее распространенным способом является получение сиккативов в растворе. По этому способу реакцию между кис-
|
Рис. 3.2. Технологическая схема получения осажденного нафтената кобальта: 1 — реактор; 2, 3, 4 — мерники; 5— реактор для осаждения; 6 — конденсатор; 7 — разделительный сосуд; 8 — фильтр; 9 — промежуточная емкость; 10 — насос |
Лотой и соединением металла проводят в среде растворителя, и сиккатив выпускается в виде раствора с определенной концентрацией активного металла.
На рис. 3.2 приведена технологическая схема процесса получения осажденного нафтената кобальта по реакции:
2RCOONa + CoS04-7H20 —(RCOO)2Co + Na2S04 + 7H20.
Технологический процесс включает следующие основные операции: нейтрализацию нафтеновых кислот; осаждение сиккатива; осушку раствора сиккатива; фильтрацию раствора сиккатива; фасовку готового продукта в тару.
Нейтрализацию нафтеновых кислот проводят в реакторе 1 при 85— 90 °С в течение 2—3 ч при перемешивании. Осаждение сиккатива осуществляют в реакторе 5, в который загружают раствор нафтената натрия из реактора 1. После нагрева этого раствора до 80 °С загружают при перемешивании толуол и раствор сульфата кобальта из мерника 4 и проводят осаждение сиккатива.
По окончании процесса реакционной массе дают отстояться. Нижний водный слой (маточник) сливают через нижний штуцер реактора, а раствор сиккатива промывают водой от водорастворимых солей. Затем проводят отгонку воды азеотропным методом при 100—110 °С. Полученный сухой раствор сиккатива фильтруют на фильтре 8; очищенный готовый сиккатив собирают в емкости 9, откуда его фасуют в тару или перекачивают в цеха-потребители этого же завода.
 1 ноября, 2012
1 ноября, 2012  admin
admin 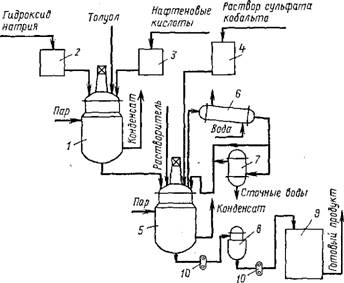
 Опубликовано в рубрике
Опубликовано в рубрике 