Результаты хроматографического разделения смеси веществ регистрируются в виде хроматограммы, которая показывает последовательное расположение компонентов вдоль неподвижной фазы и на выходе из нее, а также их количества. Получение хроматограммы целесообразно рассмотреть на примере газовой хроматографии. Газовые хроматографы выпускаются промышленностью серийно для газохроматографического контроля. Принципиальная схема такого прибора показана на рис. 111.27. Проба анализируемого вещества подается в хроматографичес — кую колонку 2 с помощью дозатора У, через который пропускают газ-носитель (элюент); обычно пробу вводят в поток газа — носителя шприцем. В колонке 2 компоненты пробы распределяются вдоль слоя сорбента, детектор 3 фиксирует концентрации выходящих из колонки компонентов в потоке газа-носителя. Сигнал детектора регистрируется самописцом 4.
Детектирование может быть интегральным и дифференциальным. При интегральном детектировании фиксируется общее количество компонентов, например, их общий объем. Вследствие малой чувствительности и инерционности интегральные детекторы применяют крайне редко. Дифференциальное детектирование (более чувствительное) позволяет фиксировать концентрацию компонентов. В качестве детекторов наиболее часто используются катарометры (регистрируют изменение теплопроводности газов по изменению электрического сопротивления проводника), ионизационные детекторы (регистрация по току ионизации молекул газа под воздействием пламени или радиоактивного излучения), детекторы плотности, или плотномеры (по плотности
|
АХ |
|
С — Ас |
|
АА± Ні— |
![]()
|
Газ — Носитель |
Рис. III.27. Принципиальная схема газового хроматографа:
/—дозатор; 2— хроматографическаи колонка; 3 — детектор: 4— регистрирующее yctpoiV
Рис. III.28. К выводу основного уравнения равновесной хроматографии.
Газа), пламенные детекторы (по температуре пламени, в котором сгорает элюент) и другие.
Самописец хроматографа записывает хроматограмму в виде отдельных хроматографических зон, отвечающих соответствующим компонентам, которые движутся с разной скоростью по хроматографической колонке>и поочередно выходят из нес.
Описание движения компонентов разделяемой смеси вдоль неподвижной фазы является основной задачей теории хроматографии. Это движение происходит с определенной скоростью, и поэтому равновесие между фазами ие достигается. Однако при соответствующих условиях хроматографические процессы могут приближаться к равновесным. Анализ равновесного процесса позволяет связать скорость перемещения компонента вдоль неподвижной фазы со скоростью потока элюента и изменением величины сорбции.
Представим себе хроматографическую колонку с сечением, равным единице площади, в которой достигается равновесное распределение вещества между подвижной и неподвижной фазами (рис. 111.28). Составим уравнение материального баланса по распределяющемуся веществу (продольную диффузию в неподвижной фазе ие будем принимать во внимание). Обозначим объемную скорость потока подвижной фазы через и, а через Дт — время прохождения участка Ах тогда за это время пройдет объем подвижной фазы шАт. При адсорбции концентрация компонента в подвижной фазе уменьшается на Ас, а общее количество вещества, ушедшего из подвижной фазы, равно wAtAc. Если q—количество сорбента, приходящееся на единицу длины колонки, то на участке A. v его количество составит qАх. В результате адсорбции концентрация вещества в сорбенте возрастает на АЛ, а общее его количество, перешедшее в сорбент на участке Ах, станет равным QAxAA. Запишем уравнение материального баланса:
(оЛтДс = <?Дх. М і ПІ.162)
Переходя к бесконечно малым величинам и записывая соотношение (III.162) относительно линейной скорости перемещения вещества и вдоль колонки, получим:
Dx Ю
Уравнение(ІІІ. ІбЗ) является основным уравнением идеальной равновесной хроматографии.
Из уравнения (III. 163) следует, что линейная скорость передвижения вещества в общем случае зависит от вида изотеруы адсорбции, т. е. от производной dAjdc. Принципиально различают три вида изотерм сорбции (рис. III.29а). Если адсорбция
|
Рис. Ill.29. Виды изотерм сорбции (а) и соответствующие им формы хро — матографических зон (б): 1—4 — см. текст. Стрелкой показано направление движения подвижной фазы |
Следует закону Генри, то производная равна константе Геири (изотермы 1 и 2 (см. рис. 111.29а) и уравнение (III.163) принимает следующий вид:
U = w/{qKrl (III.164)
Таким образом, скорость движения вещества не зависит от йго концентрации. Форма хроматографической зоны на хромато — грамме также не меняется в ходе перемещения вещества, так как элементы объема с любой концентрацией вещества передвигаются с одинаковой скоростью. Если бы отсутствовала продольная диффузия, концентрация вещества вдоль потока не менялась бы и форма хроматографической зоны напоминала вид, показанный на рис. III.296 (кривая /). Однако в реальных условиях имеет место продольная диффузия, и вследствие этого распределение концентрации вещества вдоль потока несколько изменяется, соответственно размывается и хроматографическая зона. Ее форма напоминает кривую распределения Гаусса (кривая 2 на рис. III.296).
С увеличением концентрации перестает соблюдаться закон Генри. Если изотерма имеет вид выпуклой кривой (кривая 3 на рис. III.296), то производная dA/dc уменьшается с увеличением концентрации, а скорость движения вещества возрастает. В результате наблюдается преимущественное размывание (кривая 3 на рис. III.296) задней части зоны (тыла зоны), которая движется медленнее, так как концентрация в ней меньше (вследствие диффузии). При вогнутой изотерме сорбции (кривая 4 на рис. Ш.296) производная dA/dc увеличивается с ростом концентрации и соответственно скорость движения вещества уменьшается. Это приводит к преимущественному размыванию передней части зоны (ее фронта), чему способствует возрастание скорости движения вещества при уменьшении концентрации (кривая 4 на рис. 111.296).
Так как при нелинейных изотермах сорбции происходит размывание хроматографических зон, что ухудшает качество раз
деления, то, очевидно, для лучшего разделения необходимо стремиться проводить исследования в области концентрации, при которых соблюдается закон Генри.
 2 ноября, 2012
2 ноября, 2012  admin
admin 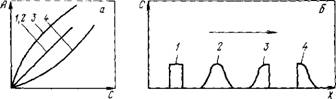
 Опубликовано в рубрике
Опубликовано в рубрике 