Процесс разрушения лакокрасочных покрытий под воздействием органических растворителей можно рассматривать следующим образом. Молекулы растворителя в результате диффузии проникают в покрытие и происходит набухание полимерного связующего. Набухание может быть ограниченным или неограниченным, т. е. переходящим в растворение. Это зависит от термического сродства растворителя к полимеру и структуры и строения полимера, т. е. наличия поперечных сшивок, разветвленности, кристалличности. Наличие поперечных сшивок или кристалличности является причиной ограниченного набухания полимера даже в термодинамически хорошем растворителе.
Растворитель, достигнув поверхности металлической подложки, на которой находится лакокрасочное покрытие, замещает адсорбированные молекулы полимера, в результате чего происходит разрушение адгезионной связи и отслаивание покрытия. Для лакокрасочных покрытий на основе термопластичных полимеров этот процесс завершается растворением. Покрытия на основе термореактивных полимеров набухают и отслаиваются от подложки [30, с. 140].
Диффузионные процессы, протекающие при воздействии растворителей на лакокрасочные покрытия, подчиняются ‘законам Фика [31, с. 6]. В случае постоянного градиента концентрации растворителя в пленке и стационарности потока процесс диффузии описывается 1-м законом Фика:
|
где Q — количество продиффунднровавшего растворителя за время т через попе- Q = — D^St, dx
трации; С — концентрация растворителя в пленке; х г— толщина пленки. |
Обычно при проникновении растворителя в пленку градиент концентрации изменяется во времени, поэтому процесс диффузии подчиняется 2-му закону Фика:
![]() dC _ D d2C
dC _ D d2C
Коэффициенты диффузии растворителей можно рассчитать, используя данные по адсорбции растворителей и по изменению [2]
|
Рис. 8. Сорбционные кривые растворителей в пленку на основе смолы ЭД-20: і — метиленхлорид; 2 — тетра хлорметан (четыреххлористый углерод); 3 — 1,3-дихлорэтан; 4 — ацетон; 5 — метилэтилкетон; 6 — этилацетат; 7 — этиловый спирт; S — бутиловый спирт |
адгезионной прочности покрытий при воздействии растворителей [32, с. 5]. Так, на основании данных по набуханию эпоксидных пленок (рис. 8) рассчитаны коэффициенты диффузии растворителей Ds по формуле:
Qt/^o=4 /1Т, т/Ь /л,
где Q„ Qgo — количество растворителя в пленке толщиной 6 в момент времени т и в состоянии равновесия.
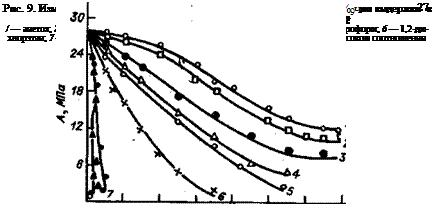
На основании результатов измерения адгезионной прочности эпоксидных пленок до и после воздействия на них растворителей (рис. 9) [33] были рассчитаны эффективные коэффициенты диффузии П9фф по формуле: гдеЛт и А^ — адгезионная прочность в момент времени и в состоянии равновесия.
Ниже приведены значения коэффициентов диффузии растворителей Ds и /),фф в эпоксидные пленки:
|
D., и!/с |
А. ф, м!/с |
|
|
Метиленхлорид |
4,86- 1(Г12 |
8,91-10-‘2 |
|
1,2-Дихлорэтан |
1,25-КГ12 |
0,9-10-‘2 |
|
Хлороформ |
0,7 ■ 10~12 |
0,97-10-12 |
|
Трихлорэтилен |
0,5-10~12 |
0,9-10“12 |
|
Тетра хлорметан |
1,ыо-12 |
2,88-10-12 |
|
Тетрахлорэтилен |
0,08-10-‘2 |
0,19-10-12 |
|
Ацетон |
1,47 •’10-и |
2,65-10-" |
|
Метилэтил кетон |
1,86.10-" |
12-10-14 |
|
Этилацетат |
2,35-10~" |
1,05-10-" |
|
Бутилацетат |
0,52.10-" |
0,08-10-" |
|
Метиловый спирт |
0,88-10-12 |
0,4-10-‘2 |
|
Этиловый спирт |
0,85-10-" |
6,27-Ю-" |
|
Бутиловый спирт |
0,4- ИГ14 |
0,2-10-14 |
Из рис. 8 видно, что при диффузии спиртов, кетонов, сложных эфиров форма сорбционных кривых имеет Г-образный характер, т. е. подчиняется 2-му закону Фика. В случае диффузии хлорированных углеводородов кинетические кривые имеют S-обраэный характер, что свидетельствует об отклонении от 2-го закона Фика. Это связано с изменением подвижности структурных элементов полимера в результате взаимодействия его с молекулами растворителя.
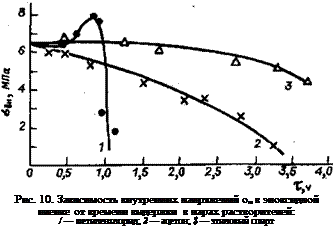
При воздействии активных растворителей на покрытия на основе термореактивних полимеров высокой степени сшивания, к которым относятся, например, эпоксидные пленки, полученные в результате отверждения с помощью полиэтиленполиамина при 200 °С в течение 2 ч, происходит неравномерное распределение растворителя в пленке. Это приводит к возникновению высоких внутренних напряжений в пленке и к ее растрескиванию (рис. 10). В случае паров высокоактивного метиленхлорид а внутренние напряжения резко возрастают, достигают максимума и падают вследствие образования трещин в пленке. При действии этилового спирта и ацетона происходит монотонное снижение внутренних напряжений, так как эти растворители оказывают пластифицирующее действие на покрытие.
|
4* |
Диффузия в твердых телах определяется наличием разрывов непрерывности в молекулярной упаковке, т. е. «дырок», по Френкелю, образующихся в результате теплового движения. Совокупность «дырок» представляет собой свободный для диффузии объем. В полимерах основными подвижными элементами являются сегменты, поэтому скорость диффузии растворителя зависит от их подвижности [28]. Подвижность сегментов в гибкоцепных поли-.
 |
мерах гораздо выше, чем в стеклообразных полимерах с плотной упаковкой макромолекул.
Введение пластификаторов увеличивает подвижность макромолекул и их сегментов и тем самым облегчает диффузию растворителей. Таким образом, пленки пластифицированных полимеров более подвержены действию растворителей по сравнению с пленками непластифицированных полимеров. При этом разные пластификаторы неодинаково влияют на процессы диффузии растворителей в пленки. Содержание пластификатора также сказывается на диффузии растворителей. Большое количество пластификатора приводит к разрыхлению пленки, что способствует диффузии растворителей.
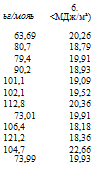 |
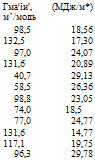 |
 |
 |
Термодинамическое взаимодействие в системе полимер-растворитель можно приближенно оценить по изменению энтальпии системы, применяя концепцию параметров растворимости [30, с. 8—14]. Ниже приведены значения молярных объемом VUOJt и общих параметров растворимости 6 для ряда наиболее распространенных органических растворителей:
![]()
|
ма/моль |
б* ./2 (МДж/м*)1’* |
Л, м • юв. м*/моль |
6, (МДж/м*) |
||
|
Метилэтил кетон |
90,16 |
18,91 |
Пропиленгликоль |
73,6 |
30,19 |
|
Метилиэобутил кетон |
125,8 |
17,48 |
Пиридин |
80,4 |
21,64 |
|
1,4-Диоксан |
85,7 |
20,4 |
Анилин |
91,1 |
22,52 |
|
Циклогексанон |
104,0 |
20,16 |
Циклогексиламин |
115,2 |
18,46 |
О действии растворителей на лакокрасочные покрытия на полимерной основе можно судить по данным табл. 4. Неактивные растворители используют в качестве сорастворителей в смеси с активными растворителями, относительно активные растворители в разных случаях могут_служить как в качестве активных растворителей, так и в качестве сорастворителей.
|
Таблица 4. Действие растворителей на лакокрасочные покрытия на основе различных полимерных пленкообразователей при температуре 20 °С в — активный растворитель; о — относительно активный растворитель; с — неактивный растворитель (сорастворитель)
|
 29 августа, 2015
29 августа, 2015  admin
admin 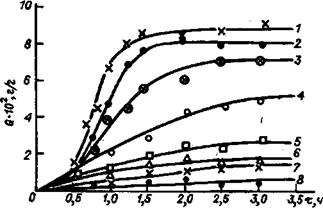
 Опубликовано в рубрике
Опубликовано в рубрике 