К высокомолекулярным веществам [31] относятся вещества, состоящие из больших молекул (макромолекул) с молекулярным весом не менее 10 000—15 000. Нередко молекулярный вес природных высокомолекулярных соединений достигает нескольких миллионов. Размер макромолекул весьма велик по сравнению с размерами обычных молекул. Например, если длина молекулы этана равна всего нескольким ангстремам, то длина линейных молекул каучука и целлюлозы достигает 4000—8000 А (при поперечном размере 3—7,5 А). Моделью подобных молекул могут служить нити длиной от 800 до 1600 мм и диаметром 1 мм.
Высокомолекулярные вещества вследствие их большого молекулярного веса нелетучи и не способны перегоняться. По той же причине высокомолекулярные вещества весьма чувствительны к воздействию различных внешних факторов. Макромолекулы легко распадаются под действием самых незначительных количеств кислорода и других деструктирующих агентов. Причина различия в чувствительности к химическим воздействиям низко — и высокомолекулярных веществ становится понятной из следующего примера. Допустим, что для расщепления одной молекулы вещества на две достаточно одной молекулы кислорода. Тогда для низкомолекулярного вещества с молекулярным весом, равным, например 100, количество кислорода, необходимое для такого расщепления, должно составлять 32% от его массы. Если же молекулярный вес окисляемого вещества 100 000, то кислорода для той же цели потребуется лишь 0,032% от его массы, что на 1 г вещества составит всего 32-Ю-5 г кислорода, т. е. количество, которое с трудом может быть обнаружено даже с помощью самых точных аналитических весов. Большинство высокомолекулярных веществ при повышении температуры размягчается постепенно и не имеет определенной температуры плавления. Температура разложения этих веществ ниже температуры кипения. Следовательно, высокомолекулярные вещества могут находиться только в конденсированном состоянии.
Свойства высокомолекулярных веществ зависят не только от размера, но и от формы молекул.
Высокомолекулярные соединения с изодиаметрическими молекулами (например, гемоглобин, печеночный крахмал — гликоген) обычно представляют собой порошкообразные вещества. При растворении они почти не набухают, а растворы этих веществ не обладают высокой вязкостью даже при сравнительно больших концентрациях и подчиняются закону вязкости Пуазейля, закону диффузии Эйнштейна и закону осмотического давления Вант-Гоффа.
Высокомолекулярные соединения с сильно асимметрическими вытянутыми молекулами (например, желатин, целлюлоза и ее производные, натуральный и синтетические каучуки) при растворении очень сильно набухают и образуют высоковязкие растворы, не подчиняющиеся закономерностям, приложимым к растворам низкомолекулярных веществ.
Характерной особенностью высокомолекулярных веществ с линейными молекулами является волокнистая структура, обусловливающая анизотропию свойств и высокую механическую прочность. Поэтому такие вещества обладают способностью образовывать волокна и пленки. Некоторые полимеры обладают ценнейшим свойством — высокой эластичностью.
Природные высокомолекулярные вещества
К природным высокомолекулярным веществам относятся такие важнейшие для биологии и техники органические вещества, как белки, высшие полисахариды, натуральный каучук.
Белки (протеины) представляют собой сложнейшие высокомолекулярные соединения. Это основное вещество, которое входит в состав протоплазмы клеток мышц, хрящей, сухожилий и кожи животных и человека. Они содержатся также в шелке, молоке (казеин) и растениях, особенно в зернах пшеницы, семенах бобовых (растительные белки). Все известные энзимы, многие гормоны и вирусы также состоят из белков. К белкам, применяемым в технике, следует отнести желатин, казеин, янчный альбумин.
Молекулы белков состоят из аминокислот, содержат ионогенные группы (—СООН, —NH3OH) и обладают амфотерными свойствами. Белки растворимы в растворах щелочей, некоторые из них растворимы в воде и разбавленных растворах солей и кислот. Растворы белков очень нестойки к действию температур: при нагревании происходит денатурация многих белков и переход их в нерастворимую форму. Белки осаждаются из растворов электролитами, спиртом и ацетоном. До сих пор многие белки из-за сложности строения не получены синтетическим путем.
Высшие полисахариды. К этим веществам относятся крахмал и целлюлоза.
Крахмал, макромолекула которого состоит из звеньев глюкозы, представляет собой не индивидуальное вещество, а смесь полисахаридов, отличающихся не только размером макромолекул, но й строением. Крахмал является одним из важнейших продуктов фотосинтеза, образующихся в зеленых частях растений, и составляет основную часть питательного вещества хлеба, картофеля и различных круп. В воде при определенной температуре крахмал набухает и клейсте-‘ ризуется, образуя внешне однородную густую жидкость — крахмальный клейстер, который широко применяют в технике в качестве клея, для шлихтования и отделки тканей, для проклеивания бумаги и т. д. Путем гидролиза из крахмала получают декстрин, патоку и глюкозу.
Целлюлоза является главной составной частью организма растений, она придает ему прочность и эластичность. Целлюлоза также состоит из длинных цепочек, составленных из остатков глюкозы, но соединенных друг с другом несколько иначе, чем в молекуле крахмала. Попытки синтезировать целлюлозу еще не привели к Положительным результатам, и поэтому ее получают из древесины, соломы и других растительных материалов путем горячей обработки растворами веществ, растворяющих содержащиеся в этих материалах лигнин и другие примеси. Целлюлозу широко используют для получения бумаги. Хлопок и другие виды растительного волокна, представляющие собой почти чистую целлюлозу, применяют в текстильном производстве для получения тканей. Производные целлюлозы — нитрат целлюлозы, ацетат целлюлозы и другие простые и сложные эфиры целлюлозы — применяют для получения кинофотопленок и искусственного волокна
Натуральный каучук — чрезвычайно ценный материал, обладающий высокой эластичностью Его добывают из млечного сока (латекса) некоторых растений (каучуконосов). По своей природе — это углеводород, причем его макромолекулы состоят из изопентеновых (изопреновых) остатков. Растворим в углеводородах, обладает пластичностью, особенно заметно проявляющейся при повышении температуры При нагревании с небольшим количеством серы каучук вулканизуется — молекулы его химически связываются друг с другом посредством МОСТИКОВ из серы. Вулканизованный каучук (резина) теряет способность растворяться и размягчаться при нагревании, но сохраняет при этом эластические свойства. При нагревании с большим количеством серы в результате образования большого числа поперечных связей между его молекулами каучук теряет эластичность и образует твердый вулканизат, называемый эбонитом.
Синтетические высокомолекулярные вещества
Помимо природных высокомолекулярных веществ в настоящее время в технике и быту применяют ряд синтетических высокомолекулярных продуктов. Сюда следует отнести синтетические каучуки и различные синтетические полимеры. Эти продукты, чрезвычайно разнообразные по химическому строению и свойствам, не только являются полноценными заменителями природных высокомолекулярных веществ, но и получают часто совершенно новое применение. Так, их используют для получения разнообразных пластмасс, в виде органического стекла, в качестве ионообменных материалов (ионитов) для очистки воды и выделения индивидуальных веществ из смесей, для изготовления деталей самолетов и автомобилей и даже корпусов малотоннажных судов. Показательно, что производство синтетических высокомолекулярных веществ значительно превысило производство не только традиционных конструктивных материалов, но и таких сравнительно новых материалов, как алюминиевые и магниевые сплавы.
К достоинствам синтетических высокомолекулярных веществ относится то, что их можно получать с заданными свойствами — прочностью, эластичность1о, химической стойкостью, диэлектрической проницаемостью, подбирая подходящие исходные материалы и регулируя технологический процесс. Кроме того, из синтетических высокомолекулярных веществ можно получать изделия методом непосредственного формования без потери материала в виде стружки и без необходимости последующей обработки изделий. • Широкое применение синтетических высокомолекулярных веществ объясняется также и неограниченными ресурсами сырья,
необходимого для’ их получения. Для синтеза высокомолекулярных веществ используются простейшие продукты переработки нефти и угля, ацетилен, а также отходы ряда отраслей промышленности.
Синтетические каучуки. К синтетическим каучукам относятся изготовляемые в промышленных масштабах полибутадиен, полихлоропрен, бутадиен-стирольные и бутадиен-нитрильные сополимеры и ряд других продуктов. Строение молекул этих веществ рассматривается во всех курсах органической химии.
Помимо собственно синтетических каучуков, которые благодаря наличию в их макромолекулах двойной связи способны вулканизоваться так же, как и натуральный каучук, известен ряд синтетических полимеров, лишенных этой способности, но обладающих высокой эластичностью. Сюда бтносится, например, продукт низкотемпературной полимеризации изобутилена—полиизобутилен. Пленки из иолиизобутилена газонепроницаемы и не изменяются под действием воздуха и озона, вследствие чего полиизобутилен широко применяют для изготовления оболочек аэростатов, шаров-пилотов и т. д. При сополимеризации изобутилена с небольшим количеством (2—3%) диена, например изопрена, получаются продукты, уже содержащие в молекуле небольшое число двойных связей. Эти продукты, способные вулканизоваться, получили название бутилкаучуков.
Полисилоксаны. Это весьма интересные новые высокомолекулярные продукты, применяемые в качестве материала для термостойкой электроизоляции. Полисилоксаны, как и каучуки, обладают высокой эластичностью, но благодаря тому, что основная цепь полисилоксана состоит из атомов кремния и кислорода, эти соединения весьма прочны и более стойки к температурным воздействиям.
Синтетические полимеры. К синтетическим полимерам, в обычных условиях не обладающим высокой эластичностью, относятся полиэтилен, поливинилхлорид, поливинилиденхлорид, поливинилацетат, полиметилакрилат, полиметилметакри — лат, полистирол и ряд других широко известных Продуктов, идущих для изготовления изделий из пластмасс, пленок и т. д. Этн вещества являются термопластичными, поскольку они могут размягчаться и формоваться при нагревании. К синтетическим полимерам относятся также термореактивиые смолы, текучие в исходном состоянии и способные при нагревании в результате химических реакций необратимо отвердевать. К таким смолам следует отнести феноло-форм — альдегидные и мочевино-формальдегидные смолы, применяемые в технике уже несколько десятилетий.
Из сравнительно новых полимеров назовем лишь полиамиды и политетрафторэтилен.
Полиамиды получают при поликонденсации диаминов с дикарбоновыми кислотами, например при конденсации гексаметилендиамина и адипиновой кислоты, полимеризацией со-аминокислот и другими методами. В результате этих реакций получается полигексаметиленадипамид. Из полигексаметиленадипамида в США изготовляют искусственное волокно найлон. Это волокно по свойствам близко к шерстяному и шелковому волокнам, а по некоторым свойствам даже превосходит их. Исключительно высокое сопротивление разрыву иайлонового волокна, достигающее 4000—4500 кгс/см2, объясняется полярностью молекулы полигексаметиленадипамида, возможностью образования водородной связи между отдельными молекулярными цепочками и тем, что в вытянутом волокне полиамид находится главным образом в ориентированном, кристаллическом состоянии. Близко по свойствам к найлону полиамидное волокно капрон, получаемое в Советском Союзе путем полимеризации капролактама.
Быстрому развитию химии соединений фтора обязано производство политетрафторэтилена. Молекулы этого полимера вследствие того, что сильно электроотрицательные атомы фтора расположены в них симметрично, неполярны. Благодаря правильной линейной структуре молекул политетрафторэтилен сравнительно легко кристаллизуется.
Политетрафторэтилен является одним из наиболее высокоплавких кристал^ лических полимеров. Вместе с тем температура, при которой он становится хрупким. очень низка. В результате этого изделия из политетрафторэтилена могут
работать в очень широком интервале температур. По термостабильности, химической стойкости и диэлектрическим свойствам политетрафторэтилен превосходит все известные до сих пор полимеры.
Неорганические высокомолекулярные вещества
Помимо органических, хорошо изученных высокомолекулярных соединений существуют также и неорганические высокомолекулярные вещества. К сожалению, строение их молекул, равно как и свойства их растворов, еще недостаточно изучены.
К высокомолекулярным неорганическим веществам с цепйым строением молекулы можно отнести, например, одну из модификаций серы («пластическая» сера), получаемую быстрым охлаждением расплава серы, нагретого выше 300 °С. Благодаря цепному строению молекулы высокомолекулярная сера обладает каучуколодобной эластичностью.
|
Рис. XIV, 1. Строение графита и алмаза: а — плоскостные решетки графита; 6 — трехмерная структура алмаза. |
|
А |
Неорганическим высокомолекулярным веществом является также полифос — фонитрилхлорид.
Примером двухмерных высокомолекулярных неорганических веществ служит обыкновенная слюда, молекулы которой имеют форму пластинок. Сюда же следует отнести и алюмосиликаты, из которых состоят глины, и графит, кристаллы которого построены из углеродных шестиугольников, расположенных друг под другом в виде отдельных плоскостей. Благодаря сравнительно большому расстоянию между отдельными сйоями и непрочности связи между ними можно считать, что в графите молекулой является каждая отдельная плоскость.
Примером трехмерного неорганического высокомолекулярного соединения может служить алмаз, состоящий из атомов углерода. В кристалле алмаза каждый атом углерода связан с четырьмя другими ближайшими атомами углерода. Кристалл алмаза можно считать одной гигантской молекулой, лишенной ряда свойств, типичных для обычных молекул. Вследствие такого строения алмаз не способен набухать, не растворяется ни в одном из растворителей и обладает очень большой твердостью. Структура графита и алмаза показана на рис. XIV, 1.
Особо следует отметить вещества промежуточного типа, растворы которых, в зависимости от условий их получения, могут проявлять свойства как типичных золей, так и растворов высокомолекулярных соединений. К таким веществам относятся окиси и гидроокиси элементов, образующих слабокислые или амфотер — ные соединения, например гидроокись кремния,
Свежеприготовленные растворы этих окисей и гидроокисей во многом сходны с растворами высокомолекулярных соединений. Эти вещества осаждаются из растворов при введении электролита, но осадок легко вновь переходит в коллоидный раствор, если коагулятор удалить. Такое осаждение и диспергирование, напри-мер двуокиси олова, может быть произведено сколь угодно большое число раз. Действие электролитов на растворы таких веществ и влияние валентности иона, вызывающего понижение ^-потенциала частиц, далеко не столь значительны, как для типичных коллоидных систем, например металлических золей и золей сульфидов металлов. Относительная вязкость растворов подобных веществ значительно выше, чем обычных золей. Наконец, растворы их обладают способностью давать студни, очень сходные по свойствам со студнями высокомолекулярных веществ.
Все приведенное выше позволяет считать, что такие растворы содержат макромолекулы. Например, можно предположить, что в свежеприготовленном растворе ортокремневой кислоты ее молекула имеет следующее строение:
(HO)3SiO— [Si(OH)2—0]„—Si(OH)3
Вероятно, таким же образом можно представить и строение молекул в проявляющих коллоидные свойства растворах гидроокиси железа, гидроокиси алюминия и др. Однако известно, что подобные растворы при стоянии или при добавлении электролитов могут приобретать типичные свойства обычных коллоидных систем. Для жидкого стекла это явление можно объяснить наличием у молекул ортокремневой кислоты гидроксильных групп, благодаря чему при добавлении, например, кислоты происходит сшивание молекул поперечными химическими связями. Если растворы достаточно разбавлены, то вследствие сшивания участков одной и той же гибкой макромолекулы могут образоваться отдельные мицеллы, причем роль стабилизатора играет сама кремневая кислота.
Если растворы достаточно концентрированы, то вследствие поперечного сшивания макромолекул образуется трехмерная сетка и раствор переводится в необратимый студень. Такого рода явление очень близко к тем процессам конденсации, которые происходят при отвердении феноло-формальдегидных смол. Отличие заключается в том, что студни кремневой кислоты после высушивания и прокаливания способны обнаруживать кристаллическую структуру (в результате образования кристалликов).
Промежуточные системы, стоящие между растворами высокомолекулярных соединений и типичными коллоидными растворами или же способные переходить из одного класса растворов в другой, не следует смешивать с растворами коллоидных поверхностно — активных веществ, отличающимися тем, что в одних условиях они проявляют свойства истинных растворов, а в других — типичные свойства золей.
 1 ноября, 2012
1 ноября, 2012  admin
admin 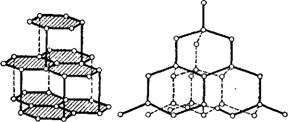
 Опубликовано в рубрике
Опубликовано в рубрике 