Коллоидные системы с газовой дисперсионной средой обычно называют аэрозолями, хотя большей частью их дисперсность ниже коллоидной, и поэтому правильнее называть их аэродисперсными системами.
Отличие аэрозолей от лиозолей обусловлено прежде всего разреженностью и меньшей вязкостью дисперсионной газовой среды. Поэтому броуновское движение в аэрозолях происходит гораздо более интенсивно, а седиментация частиц идет значительно быстрее, чем в лиозолях. Другое существенное отличие аэрозолей от лиозолей заключается в том, что в газовой среде не может происходить электролитическая диссоциация и, следовательно, невозможно образование двойного электрического слоя из ионов вокруг частиц. В связи с этими особенностями учение об аэрозолях развивалось в значительной мере самостоятельно, своими собственными путями.
Классификация аэрозолей. Аэрозоли классифицируют по агрегатному состоянию Дисперсной фазы, по дисперсности и по методам получения.
Исходя из первого принципа, аэрозоли делят на туманы — системы с жидкой дисперсной фазой и дымы — системы с твердыми частицами. К дымам следует отнести по этой классификации и пыли — системы с твердыми, но более крупными частицами.
Следует иметь в виду, что часто в практике «дым» означает аэродисперсную систему, возникающую при сгорании топлива и содержащую как твердые частицы сажи и золы, так и жидкие частицы продуктов перегонки топлива и капли воды, образовав
шиеся в результате конденсации водяного пара. Дымы, в которых частицы дисперсной фазы адсорбировали значительное количество влаги из атмосферы, очевидно, являются одновременно и дымами, и туманами. Такие системы, особенно часто образующиеся при большом содержании влаги в задымленной атмосфере над большими промышленными городами, называются особым английским термином «смог» [smog = smoke (дым)+ fog (туман)].
По дисперсности аэрозоли с твердой дисперсной фазой разделяют на дымы с частицами от J0-7 до Ю-3 см и на пыли, размер частиц которых обычно больше Ю-3 см. Туманы, как правило, имеют довольно крупные капельки размером от Ю-5 до 10-3 см.
По происхождению системы с газовой дисперсионной средой разделяют, как и все дисперсные системы,*на диспергацион — ные и конденсационные аэрозоли. Диспергационные аэрозоли, образующиеся при измельчении твердых тел или распылении жидкостей, как и лиозоли, полученные путем диспергирования, имеют довольно крупные частицы и, как правило, полидисперсны. Аэрозоли, полученные методом конденсации из пересыщенных паров или в результате химических реакций, наоборот, обычно являются высокодисперсными системами с более однородными по- размеру частицами
Размер и форма частиц. Ниже приведены размеры частиц (в см) некоторых типичных аэрозолей:
Туман (Н20)
Слоистые облака Дождевые облака H2S04 (туман) . . ZnO (дым) . . . Табачный дым. . Топочный дым. . Р206 (дым) . . .
Кривая распределения частиц в аэрозоле, т. е. содержание в нем частиц различных радиусов, зависит от происхождения аэрозоля и процессов, происходящих в аэрозоле после его получения (агрегация, коалесценция, изотермическая перегонка).
Форма частиц аэрозолей зависит от агрегатного состояния ве-в щества дисперсной фазы. В туманах капельки жидкости шарообразны. В дымах они могут иметь самую разнообразную форму, например, игольчатую, пластинчатую, звездообразную. В дымах частицы могут представлять собой и сложные агрегаты, тогда как в туманах столкновение капелек обычно приводит к коалесценции и образованию капелек большего размера.
В результате рыхлости (пористости) частиц аэрозоля кажущаяся плотность этих частиц, определенная обычно принятыми способами, часто значительно меньше плотности вещества, из которого они состоят. Это можно видеть по значениям плотностей частиц некоторых дымов, полученных различными методами (табл. XI, 1),
Таблица XI, 1. Плотность частиц в дымах
Плотность, г/смэ
|
Вещество |
Метод получения дь, ма
Истинная кажущаяся
19,3 0,2—8,0 Испарение в вольтовой дуге
10.5 0,64—4,22 То же
13.6 0,07—10,8 Нагревание в лодочке
3,6 0,24—3,48 Сжигание металлического магния
5.4 0,62—4,3 Нагревание в лодочке
|
Золото Серебро Ртуть Окись магния Хлорид ртути Окись кадмия |
6.5 0,17—2,7 Испарение в вольтовой дуге
Размер и форму частиц аэрозолей определяют с помощью обычной микроскопии, ультрамикроскопии и электронной микроскопии. Для счета частиц в аэрозолях особенно удобен поточный микроскоп Б. В. Дерягина и Г. Я. Власенко, о котором уже упоминалось в гл. II.
Концентрацию трудно доступных для исследования аэрозолей, например концентрацию воды в облаке, можно определять с помощью радиолокаторов. «Прощупывающий» пространство направленный радиолуч испускается источником в виде импульсов через определенные промежутки времени и регистрируется на экране осциллографа. С помощью осциллографа регистрируется и излучение, возвратившееся обратно в результате рассеяния объектом (облаком). По интервалу времени, прошедшему от подачи" радиосигнала до приема рассеянного луча, можно определить расстояние до объекта, а по интенсивности отраженного луча можно судить о концентрации дисперсной фазы в объекте, так как рассеяние радиолучей малыми частицами описывается уравнением, в общем аналогичным уравнению Рэлея.
Оптические свойства. Оптические свойства аэрозолей подчиняются в общем тем же законам, что и оптические свойства лиозолей. Следует, однако, помнить, что вследствие большой разницы в плотностях, а значит, и в показателях преломления дисперсной и газовой фаз оптические свойства аэрозолей и прежде всего светорассеяние проявляются весьма ярко. Благодаря большой способности рассеивать свет аэрозоли широко применяются для создания дымовых завес. Из всех дымов наибольшей способностью рассеивать и отражать свет обладает дым Р2О5; его маскирующая способность обычно принимается за единицу.
Молекулярно-кинетические свойства. Аэрозоли — сравнительно сильно разреженные системы, обладающие малым коэффициентом внутреннего трения дисперсионной среды. Этим и определяются особенности их молекулярно-кинетических свойств.
|
(XI, 1) |
Движение взвешенных в вязкой жидкости (рассматриваемой как непрерывная среда) сферических частиц, размеры которых значительно превышают размеры молекул среды, описывается известным уравнением Стокса:
F = блцги
Где F — сила трения частицы; г| — вязкость среды, г — радиус частицы, и — скорость движения частицы
|
(XI, 2> |
Введя коэффициент сопротивления частицы В = F/U, получим
В — бяіу
Для описания движения частиц, взвешенных в газовой среде, это гидродинамическое уравнение пригодно только в том случае, если размер частиц значительно больше среднего свободного пробега молекул газа Так как при атмосферном давлении эта величина для воздуха составляет приблизительно Ю-5 см,, то очевидно, уравнение Стокса применимо лишь для грубодисперсных аэрозолей,, радиус частиц которых превышает Ю-4 см При меньших давлениях и, следовательно, при большем свободном пробеге граница применимости уравнения Стокса для аэрозолей смещается в сторону еще меньшей дисперсности
Для высоко дисперсных аэрозолей, радиус частиц которых меньше Ю-8 см, движение частиц описывается другим уравнением’
|
" (XI, 3> (XI, 4> |
|
Или |
F = 6яг|лги/(0,3502 • 4,5Л) В = 6іщг2/(0,3502 .4,5Я)
Где X— средний свободный пробег молекул газа
Это уравнение выводится на основе представлений, аналогичных применяемым в кинетической теории газов, так как для малых частиц (или для низких давлений), когда отношение Х/г 1, движение частиц аэрозоля происходит подобно движению молекул газа
|
Или |
Для описания поведения аэрозолей с промежуточным размером частиц. (10_б—10~4 см) используются переходные формулы; одной из таких формул является уравнение Кеннингема.
|
|
(XI, 5>
Где А — коэффициент, близкий к единице, значение которого определяется экспериментально
Как можно видеть, для больших значений Х/R (когда АХ/г » 1) в уравнении (XI,3) сила сопротивления F пропорциональна квадрату радиуса частицы, а для малых значений Х/R (когда АХ/г <. 1) уравнение Кеннингема переходит в уравнение Стокса
Все сказанное относилось к простейшему случаю — движению сферических, частиц Зависимость скорости движения частицы от действующей силы для ие — сферических частиц гораздо сложнее ‘
Рассмотрим кратко особенности броуновского движения в дисперсных системах с газовой средой На броуновском движении частиц в аэрозолях весьма сильно сказывается седиментация вследствие малой вязкости и малой плотности газовой среды В ранних исследованиях это не было учтено, и поэтому значение средних смещений в горизонтальном и вертикальном направлениях не совпадали. Кроме того, благодаря малой вязкости аэрозолей в них легко возникают конвекционные токи, что также весьма затрудняло изучение броуновского движения в этих системах Однако позже благодаря применению усовершенствованных методов исследования все эти трудности были преодолены и было установлено, что броуновское движение в аэрозолях подчиняется тем же закономерностям, что и в лнозолях В настоящее время броуновское движение в аэрозолях изучают путем микроскопического наблюдения за седиментирующими частицами, которым придают тем или иным способом электрический заряд Благодаря за — ряду частицы, опустившиеся на некоторое расстояние вследствие седиментации, можно возвратить в исходное положение при наложении соответственно направленного электрического поля и таким образом проводить множество изме-
-рений с помощью одной и той же частицы, что обеспечивает получение точных результатов.
Если бы частица аэрозоля не находилась в броуновском движении, то время ее оседания % на расстояние H было строго постоянным. Однако из-за броуновского движения к ее перемещению добавляется вертикальная составляющая. Время, необходимое для прохождения частицей расстояния Л, может быть больше (если броуновское смещение за время падения направлено снизу вверх) или меньше (если броуновское смещение направлено вниз) времени седиментации. Полученное при таких измерениях большое число значений Xit т2, Тз.. 1 Для продолжительности падения на одно и то же расстояние H можно обработать с помощью теории броуновского движения. Не входя в подробности этих расчетов, укажем, что коэффициент диффузии, вычисленный по полученным таким образом результатам с учетом поправки на седиментацию, для капелек масляного тумана, как показал Флетчер, прекрасно совпадает с коэффициентом диффузии, найденным для этой системы другими способами.
Весьма существенно учитывать одновременно идущие диффузию и седиментацию при исследовании поведения аэрозоля, заключенного в небольшое пространство Это особенно важно для понимания процесса фильтрации.
Допустим для упрощения, что аэрозоль заключен в сферическое пространство с радиусом R. При этом уменьшение численной концентрации аэрозоля может идти двумя путями:
1) частицы, находящиеся в броуновском движении, достигают стенок сосуда и прилипают к ним (вследствие того, что частицы аэрозоля обычно лишены какого-либо фактора устойчивости, можно считать, что каждая частица, ударившаяся о стенку, остается на ней);
2) частицы седиментируют и оседают на дно сосуда.
Время тд, необходимое для того, чтобы частица, находящаяся в центре сосуда и максимально удаленная от стенки, продиффундировала к ней, очевидно, можно найти, исходя из формулы Эйнштейна — Смолуховского (см. гл. III, разд 2), путем замены Д2 на R2
Тд = R2/(2D) — R2B/(2kT) (XI, 7)
Время тс, необходимое для седиментации максимально удаленной частицы на дно, определяется, очевидно, уравнением
Тс = 2 RB/(Mg) (XI,8)
Где т — масса частицы; G — ускорение свободного падения (при этом принимается, что седиментация частицы происходит с постоянной скоростью 2R/Rc).
Так как для малых частиц коэффициент сопротивления частицы В пропорционален квадрату радиуса, а масса частиц пропорциональна кубу радиуса, то тд ~ г2, а 1с ~ I/г. Отсюда следует, что средние значения *гд и тс, необходимые для прилипания частиц к стенкам сосуда и для оседания на дно, по-разному зависят от размера частиц.
Если частицы малы, то диффузия происходит быстрее, чем седиментация, и разрушение аэрозоля в основном будет вызвано прилипанием частиц к стен — •кам, а не оседанием на дно Если частицы крупные, наблюдается обратное явление, т. е. разрушение аэрозолей обусловлено в основном седиментацией.
Из изложенного также следует, что из аэрозоля быстро исчезают как очень мелкие, так и очень крупные частицы, первые вследствие прилипания к стенкам, вторые — в результате оседания на дно. Наоборот, частицы промежуточных размеров дольше пребывают в аэрозоле Частицы, для которых тд = т0, очевидно, обладают максимальной устойчивостью. Приравнивая уравнения (XI, 7) и (XI, 8), легко найти формулу, по которой можно вычислить массу частиц, дольше всего остающихся в аэрозоле:
M0 = 4kT/(gR) (XI, 9)
Все сказанное о разрушении аэрозоля, находящегося в ограниченном объеме, • относится к разрушению систем с газовой дисперсионной средой при прохождении нх через пористые фильтрующие материалы. Развитые выше соображения, вероятно, объясняют также и то обстоятельство, что у людей, больных силикозом, в легких находят главным образом частицы кварца размером, отвечающим массе Ото — Можно предполагать, что кристаллы больших и меньших размеров остаются почти целиком в дыхательных путях человека и не доходят до легких.
Рассмотрим кратко явления термофореза, фотофореза и термопреципитации, связанные с кинетическими свойствами и характерные для коллоидных систем с газовой средой.
Явление термофореза заключается в движении частиц аэрозоля в направлении снижения температуры. При соблюдении условия 1, т. е когда частицы малы, термофорез возникает вследствие того, что на более нагретую сторону частицы молекулы газа налетают с большей скоростью, чем на менее нагретую, и, следовательно, сообщают частице импульс в направлении понижения температуры. Если Х/г •< 1, причина возникновения термофореза несколько более сложная. Однако можно показать, что и при Х/г •< 1 движение частицы в поле температурного градиента должно также происходить в сторону понижения температуры.
Строгая количественная теория термофореза для малых и больших частиц разработана Б. В. Дерягиным, С. П. Бакаевым и Ю. И. Яламовым.
Фотофоре з, заключающийся в передвижении частиц аэрозоля при одностороннем их освещении, является частным случаем термофореза. Объяснение фотофореза более сложно, чем термофореза, поскольку распределение температуры внутри освещенной частицы зависит от ее размера, формы, прозрачности и коэффициента преломления и, следовательно, может быть весьма различным. Для непрозрачных частиц обычно наблюдается положительный фотофорез, т. е. движение частиц в направлении светового луча. Для прозрачных частиц может наблюдаться и отрицательный фотофорез в связи с тем, что задняя сторона частицы может быть нагрета преломившимися в частице лучами сильнее, чем передняя, обращенная к источнику света. Известны случаи, когда малые частицы некоторых веществ обнаруживают отрицательный фотофорез, а большие— положительный. Такое явление можно объяснить тем, что по мере увеличения размера частицы свет, прошедший через частицу, ослабляется в большей степени, а значит, задняя сторона частицы нагревается меньше.
Термофорез и фотофорез имеют большое значение в движении атмосферных аэрозолей, например при образовании облаков. Термофорез .водяных капелек, взвешенных в воздухе, возникает при соприкосновении холодных и теплых воздушных масс, а фотофорез происходит вследствие освещения облаков солнечными лучами. Следует вообще заметить, что кинетическая устойчивость атмосферных аэрозолей весьма своеобразна. Благодаря небольшому размеру капелек и малой скорости оседания (0,05—0,7 см/с) они как бы взвешены в атмосфере, и поднимающихся от земли сравнительно слабых токов теплого воздуха достаточно для того, чтобы облака продолжали свой путь над землей, двигаясь при этом как одно целое. И только, когда в результате коалесцеиции или конденсации капельки облаков или туманов становятся больше критического размера, они выпадают в виде дождя
Под термопреципитацией подразумевают осаждение частиц аэрозоля иа холодных поверхностях, поскольку при соприкосновении с такими поверхностями частицы теряют кинетическую энергию. Именно термопрецнпита — цией объясняется осаждение пыли иа стенах и потолке возле печей, радиаторов, ламп, а также в трубах.
Электрические свойства. Как уже указывалось, вокруг частиц в системах с газовой дисперсионной средой не могут возникать Двойные электрические слои. Тем не менее частицы аэрозолей в определенных условиях могут быть заряженными, хотя заряд их обычно невелик. Электрический заряд на частицах в аэрозолях возникает либо в результате образования и последующего нарушения контакта частиц друг с другом или с какой-нибудь поверх — тюстью, либо, чаще всего, вследствие адсорбции на поверхности частиц ионов газов.
В отличие от коллоидных растворов, где величина заряда частицы обычно обуславливается избирательной адсорбцией ионов электролита и отвечает равновесию между частицей и окружающей средой,- у аэрозолей заряд частицы в известной мере случаен и целиком зависит от причин, его вызывающих. По тем же причинам у аэрозолей не существует строгой зависимости между дисперсностью и величиной заряда. Однако в общем все же можно полагать, что заряд частицы аэрозоля тем больше, чем больше ее размеры. Из практики также установлено, что частицы аэрозолей металлов и их окислов обычно несут отрицательный заряд, например Fe203, MgO, Zn, ZnO, и, наоборот, частицы аэрозолей неметаллов и их окислов заряжены, как правило, положительно (Si02, Р2О5). Положительно заряжены также частицы NaCl, угля, крахмала; частицы муки несут отрицательный заряд. —
Рассмотрим подробнее причины возникновения электрических зарядов на частицах аэрозоля.
Допустим, что частица аэрозоля вначале не имеет заряда п адсорбция на ней ионов, всегда присутствующих в газовой фазе в результате ионизация газов под действием космических или ультрафиолетовых лучей, неспецифична. Такая частица, сталкиваясь с ионом, адсорбирует его и приобретает заряд. Так как концентрация ионов в газе невелика, то эти столкновения редки — интервал времени от одной встречи до другой может измеряться минутами. При новом столкновении адсорбировавшей частицы с ионом заряд. частицы может увеличиться или уменьшиться в зависимости от знака заряда и валентности иоиа, с которым она столкнулась. В результате подобных встреч частица может даже изменить знак заряда или стать нейтральной. Конечно, одновременно происходит и десорбция ионов, захваченных частицей. Таким образом, частица время от времени меняет заряд, но колебания заряда в общем должны происходить около среднего нейтрального состояния. Нетрудно видеть, что колебания заряда частиц аэрозоля имеют характер флуктуаций и являются отражением молекуляр — но-кинетического движения ионов и частиц. При таких условиях вероятность W приобретения частицей какого-либо заряда определяется выражением:
W~exp( — A/kT) (XI, 10)
Где А — работа, необходимая для осуществления флуктуации.
Расчеты, подтвержденные опытом, показывают, что заряд частиц аэрозоля — обычно очень мал и редко превышает элементарный электрический заряд более чем в І0 раз. Это позволило установить дискретный характер заряда ионов и измерить абсолютную величину заряда электрона, что и было выполнено Милли- кеном.
Рассмотренная картина значительно усложняется, когда частицы способны избирательно адсорбировать ионы какого-нибудь определенного вида, иными словами, когда проявляется действие адсорбционного потенциала. Кроме того, на межфазной границе обычно существует скачок потенциала. А. Н. Фрумкин показал, что на межфазной границе аэрозолей воды или снега благодаря большому дипольному моменту молекул Н20 и их ориентации существует положительный электрический потенциал порядка 250 мВ. Скачок потенциала на межфазной границе может возникать и вследствие так называемой баллоэлектризации — электризации частиц аэрозоля при получении его методом диспергирования.
В результате способности дисперсной фазы к специфической адсорбции ионов и наличия скачка потенциала у межфазной границы частицы аэрозоля неодинаково адсорбируют различные ионы и средний их заряд отличен от нуля.
Заряд частиц обусловливает явления, происходящие в больших объемах аэрозоля, например в облаках. Опытным путем установлено, что заряд капелек воды в облаках в общем близок к величине, соответствующей потенциалу порядка 250 мВ. В больших объемах атмосферного аэрозоля происходит разделение: частиц по размеру, а следовательно, и по электрическому заряду, вследствие того, что частицы различных радиусов седиментируют с разной скоростью. В результате этого электронейтральность облака нарушается и в нем возникают мощные электрические поля. При этом нижняя часть облака приобретает обычно отрицательный заряд, а верхняя часть остается положительно заряженной. Расчеты показывают, что в таких условиях напряженность поля Н в облаке составляет, в среднем 100 В/см. Однако при значительной полидисперсностн капелек облака, а также при конвекционных токах, обусловленных ветром, в облаке могут возникать и гораздо большие напряжения, служащие причиной грозовых явлений.
Заряд частиц аэрозолей обычно определяют с помощью приемов, аналогичных методам, используемым для изучения броуновского движения в этих системах. С большой точностью измеряют скорость свободной седиментации частицы аэрозоля. После этого определяют скорость падения или поднятия частицы в наложенном на нее электрическом поле н вычисляют заряд частицы Q, пользуясь уравнением:
U = uc±u3 = ~(mg± QH) (Х1,11>
Где ис — скорость свободной седиментации частицы; и3—скорость движения ча — N стицы в электрическом поле; т —масса частицы; G — ускорение свободного падения; Н — напряженность электрического поля.
Ионизируя дисперсионную среду аэрозоля, можно изменять заряд частиц на величину &Q. Весьма существенно, что изменение AQ всегда оказывается кратным величине элементарного заряда е = 4,8-10~10 эл.-ст. ед. Заряд частицы можно найти, не зная коэффициента В, применив поле с напряжением Но, при котором подъемная сила полностью компенсирует вес частицы. В этом случае, очевидно, «с = «э. Заменив «с на Mg/B и и» на QHo/B, получим уравнение:
Mg= QH0 (XI, 12>
Из которого легко найти Q.
Агрегативная устойчивость. Электрический заряд частиц аэрозолей, возникающий обычно в результате адсорбции ионов, как правило, весьма невелик, а иногда практически равен нулю. Встает вопрос, могут ли возникать на поверхности частиц аэрозоля молекулярные адсорбционные слои и способны ли такие слои обусловливать агрегативную устойчивость аэрозолей.
В ранних работах имеются указания, что при достаточно больших давлениях на поверхности ч’астиц аэрозоля возникает полимолекулярный диффузный слой газа, удерживаемый адсорбционными силами. Наличием газовой оболочки, в частности, объясняли неслеживаемость порошков при хранении, способность порошков течь подобно жидкостям и несмачивание твердых частиц аэрозолей жидкостью (известно, что дым может проходить через воду, причем частицы дисперсной фазы не остаются в воде). В некоторых работах приводились даже данные, характеризующие количество воздуха, адсорбированного аэрозолем, причем объем адсорбированного газа обычно во много раз превышал объем адсорбировавшей его дисперсной фазы. Однако в последние десятилетия появились работы, в которых опровергается возможность адсорбции аэрозолями больших количеств газа, и поэтому считают, что образование вокруг их частиц диффузных газовых оболочек невозможно.
Вне всякого сомнения, что поверхность твердых частиц аэрозолей может быть покрыта пленкой жидкости. Например, у обычного дыма такая пленка может состоять из жидких продуктов перегонки топлива и из сконденсированной влаги. Однако стабилизующее действие жидкостных адсорбционных оболочек, на которое указывалось в некоторых работах, более чем сомнительно. Поскольку частицы аэрозоля окружены газом, а не жидкостью, расклинивающее давление не может проявиться. Кроме того, поверхностное натяжение на границе раздела жидкость — газ остается всегда достаточно большим для того, чтобы обеспечить понижение свободной энергии системы при слипании частиц.
Рассматривая влияние влажности на коагуляцию дымов, необходимо упомянуть о наблюдениях Далавала и Орра. Эти~исследо — ватели нашли, что скорость седиментации аэрозолей MgO и, особенно, NH4CI, значительно повышается во влажной атмосфере. Микроскопическое исследование показало, что агрегаты частиц становятся при этом более компактными. По всей вероятности это вызвано стягиванием агрегатов конденсированной водной пленкой-.- Таким образом, аэрозоли, обладая при высокой дисперсности достаточной седиментационной устойчивостью, обычно являются весьма агрегатнвно неустойчивьімц_сисіемами и в них всегда идет процесс кодсуляции. Этим объясняется сравнительно—небольшой" срок жизни любогд аэрозоля. Существенно, что максимальную неустойчивость проявляют аэрозоли с наиболее крупными и наиболее мелкими частицами. Первые системы неустойчивы из-за большой скорости оседания их частиц, вторые не могут долго существовать вследствие интенсивного броуновского движения, приводящего к стрлкновению частиц и образованию агрегатов.
Коагуляция аэрозолей, являющаяся, как правило, процессом быстрой коагуляции, обычно протекает значительно быстрее, чем коагуляция лиозолей, из-за более^интенсивносо броуновского движения ju»Јlma2LCJ^^BM^cnepcH0HH0ft средой? Расчеты пока-* зывают, что скорость коагуляцШГ чрезвычайно сильно возрастает с увеличением ,численной коыцен. тдахшд..аэрозоле — Ниже приведены данные, характеризующие скорость коагуляции аэрозолей в зависимости от концентрации:
Начальная численная
Концентрация в 1 см3 1012 Ю10 108 108
Время, требующееся для уменьшения численной концентрации
На два порядка. . . Доля 15—30 с 30 мин Несколь — секунды ко суток
Из этих данных следует, что независимо от начальной концентрации аэрозоля через несколько минут после его получения численная: концентрация в 1 см3 не может быть выше 10®— 106. Это примерно1 в 108 раз меньше численной концентрации лиозолей (например, обычный золь золота содержит около 1015 частиц в 1 см3). Таким
•образом, как в природе, так и в производственных условиях мы почти всегда имеем дело с весьма сильно разбавленными аэрозолями.
Приведенные данные характеризуют скорость коагуляции аэрозолей только в первом приближении. На скорость разрушения систем с газовой дисперсионной средой, помимо частоты столкновения частиц, влияют и другие факторы Так,-коагуляции аэрозолей способствует полидисперсность и анизодиаметрическая форма частиц. Разрушение аэрозолей ускоряется" при наличии в них противоположно заряженных частиц. Наоборот, если частицы аэрозоля обладают одинаковым по знаку и достаточно большим по величине зарядом, то наблюдается рассеяние частиц.
Весьма интересно поведение аэрозолей, содержащих частицы жидкости с высоким давлением пара. Частицы таких аэрозолей могут упруго отскакивать друг от друга при столкновениях. Причина этого, как установили Б В. Дерягин и П С. Прохоров, заключается в испарении жидкости с поверхности капелек и образовании вследствие этого диффузно — конвекционного газового потока, препятствующего коалесценции капель Расчеты подтвердили, что давление пара, возникающее в результате такого испарения, вполне достаточно, чтобы неограниченно долго препятствовать слиянию двух капелек жидкости, находящихся в непосредственной близости (при условии пополнения испаряющейся жидкости). Интересно, что если предотвратить испарение, например путем насыщения окружающего воздуха парами той же жидкости, то капли тотчас коалесцируют Повышения агрегативной устойчивости эмульсий и суспензий вследствие растворения дисперсной фазы в дисперсионной среде никогда не наблюдается; очевидно, это можно объяснить тем, что диффузия в жидкой среде протекает с очень малой скоростью.
На скорость коагуляции аэрозоля, конечно, влияют конвекционные потоки, механическое перемешивание, ультразвуковые колебания, поскольку все эти воздействия увеличивают вероятности столкновения частиц друг с другом.
В заключение отметим, что в аэрозолях, как и лиозолях, могут изменяться размеры частиц не только за счет явления коалесценции и агрегации, но и вследствие изотермической перегонки дисперсной фазы, что приводит к укрупнению больших частиц за счет испарения более мелких. Испарение капелек туманов может при* водить в соответствующих условиях и к переходу аэрозоля в гомогенную систему подобно тому, как растворение дисперсной фазы лиозоля приводит к образованию истинного раствора,
Зависимость свойств аэрозолей от радиуса их частиц. На
Рис. XI, 1 наглядно представлена зависимость основных свойств аэрозолей от их дисперсности. Нетрудно видеть, что зависимость многих свойств и особенно молекулярно-кинетических от радиуса частицу аэрозолей выражена ярче, чем у лиозолей.
 1 ноября, 2012
1 ноября, 2012  admin
admin 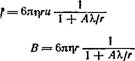
 Опубликовано в рубрике
Опубликовано в рубрике 