Пример, демонстрирующий диффузионную тео])ию адгезии, схематично представлен на рис. G.3. Два материала, обозначенные как.-1 гг Н. находятся в тесном контакте. Если оба материала взаимно растворимы, они образуют раствор. Считают, что в результате диффузии существует не истинная граница раздела, а и первую очередь граница pa. idc. ia, и которой свойст ва материала А постепенно заменяются на снойегва материала И Диффузионное соединение представляет собой предельное адгезионное соединение. В случае «нормального» адгезионного соединении клей и субстрат нерастворимы друг в друге и гг лучшем случае существует микроскопическая морфология (см. раздел 6.5), которая «размывает* границу раздела. В этой «нормальной» ситуации обычно существует определенное несоответствие между свойствами клея и субстрата. Например, контакт между клеем и субстратом ведет себя как нарушение непрерывности, приводящий к концентрации напряжении. Гранина раздела, образованная в диффузионном адгезионном соединении, не приводит к появлению плоскости концентрации напряжений, гак как н данном случае отсу і ствует нарушение непрерывности физических свойств.
1‘ш. 6.3. Коли материалы А и И полностью взаиморасі моримы, они проникают друї н друга
и образуют границу раздела. которая представляет собой раствор материала А в материале В и наоборот. Данный рисунок схематически показывает диффузионное соединение
Ситуации, при которых субстрат и клей взанморап коримы, встречаются довольно jhviko. Следовательно, диффузионная теория адгезии может быть применима только в ряде отдельных случаев. Можно предложи і ь некоторые простые критерии, определяющие взаимную растворимость материалов, в псионе которых заложена теория простых растворов, предложенная Хилдебрандом |(>|. Основным моментом этой теории является энергия когезии материала /:’ у. которая представляет собой величину энергии, необходимой для того, чтобы взять все атомы или молекулы в мате материала и разнести их на бесконечное расстояние. Энергия когезии сама по себе является одним из важных параметров, так как пазволяет понять, насколько сильно атомы или молекулы в твердых телах или жидкостях притягиваются друг к другу. Параметр /: іЛ можно определить, используя следующее уравнение:
RT’ ‘ ‘ <6Э)
где Д/У _ энтальпия испарения; R і. сажая постоянная; Т — абсолютная температура по Кельвину.
Определить величину сил межмолекулярного взаимодействия можно, основываясь на том факте, что изменение энтальпии в результате испарения является основным параметром в уравнении энергии когезии. Требуемся значительно больше энергии для испарения стали, чем для испарения ацетона. Следовательно, паль облачает знач ипглыю более высокой величиной энергии когезии, чем ацетон. Определить плотность когезионной энергии материала можно по уравнению
C. E.D. — ErJV. (6.4)
где C. H.D. плотность энергии когезии; V объем молекулы.
Важным параметром в простой теории растворимости является параметр растворимости. описываемый уравнением
где 5 — параметр растворимся’ і и; 6 плотность энергии когезии.
В растворе, к котором отсутствуют характерные химические взаимодействия, энтальпия раствора описываемая как
где 6 параметр расі воримости /-то компонента: О мольная доля /-то комисшен га.
Это интересное уравнение показываем, что не существует экзотермических рас — твс>|Юв и в действительности лучший раствор, который может быть приготовлен. НС
165
обладает эндотермическими свойствами. Есть много растворов, которые являются экзотермическими, однако нужно помнить, что ранее была допущена ситуация, при которой отсутствуют характерные химические взаимодействия. В данном случае для растворов не характерно экзотермическое поведение. Критерием для самопроизвольного образования расі вора являются знак и величина свободной энергии смешения Гиббса, представленные выражением
Дб^-дЯ^-ГД*^. (6.7)
где Л0‘1я — изменение величины свободной энергии смешения Гиббса: Л//, . — энтальпия раствора: Т абсолютная температура по Кельвину: ДЛ _Ч изменение величины энтропии в системе.
Для регулярных растворов, как показано в приведенном выше уравнении, энтальпия раствора или положительна, или равна нулю. Для того чтобы получить отрицательное значение свободной энергии смешения Гиббса, можно обратиться к изменению энтропии. Для случая низкомолекулярных материалов величина изменения энтропии всегда имеет положительный знак и обычно большое значение из — за увеличения неупорядоченности в системе мри смешении двух материалов. Однако в случае полимерных материалов изменение энтропии обычно очень мало, так как число состояний, в которых может существовать полимер, ограничено его высокой молекулярной массой. Другими словами, все отдельные сегменты полимера связаны друг е другом и число возможных конфигурационных состояний является ограниченным. Так как изменение энтропии незначительно и изменение энтальпии равно нулю или имеет положительную величину, высокомолекулярные полимеры вероятно нерастворимы друг в друге. Установлено, что такое поведение характерно для большинства (если не для всех) полимерных систем. 11ары полимеров, которые взаимно растворимы, демонстрируют некоторую величину энтальпии смешения. Например, пол и метил метакрилат растворим в полининнлиленфгорнле. Считают, что такая растворимость объясняется экзотермической кислотно-щелочной реакцией, при которой основной метакрилатный эфир взаимодействует с кислотной винилидеифторидной группой.
Приведенные выше рассуждения позволяют установить один из критериев досі ижения удовлетворительной силы адгезии. В ситуации, когда один из полимеров растворяется в другом, получают предельную силу адгезии. Критерием определения растворимости одного полимера в другом является параметр растворимости. Самое высокое значение параметра ДII и, которое можно получить, равно 0 или находится в точке, в которой параметр растворимости двух материалов одинаков. Таким образом, одним из критериев для получения удовлетвори гелыюй силы адгезии являются одинаковые значения параметров растворимости клея и субстрата.
Существует множество примеров, в которых данное представление находит применение. Ийенгэр и Эриксон [7] выполнили серию простых экспериментов, в процессе которых был использован ряд клеев между слоями полиэтилснтсрсфталата (ПЭТ) при изготовлении образцов для испытания при расслаивании. Параметры растворимости клеев известны. Параметр растворимости ПЭТ составляет около
10.3. На рис. 6.4 представлен график, аналогичный графику, построенному Имен* гэром и Эриксоном. На рис. 6.4 построен график зависимости прочности при рас
![]()
спаивании от параметра растворимости использованных клеен. Существует строгая зависимость практической адгезии от параметра растворимости клея. Если параметр растворимости клея соответствует параметру растворимости субстрата, характер разрушения меняется от очевидного адгезионного разрушения до когезионного разрушения по субстрату.
Понятие диффузионного соединения не является новым подходом для специалистов, работающих в области склеивания пластмасс. Для соединения ряда пластмасс может быть использована сварка растворителем. Растворитель наносят на поверхности обоих субстратов и соединяют их. Когда растворитель присутствует на поверхности, молекулы полимера в деталях могут взаимно диффундировать. После испарения растворителя собранный элемент конструкции по-существу является исключительно полиме|х>м. Пластмассы и растворители должны быть тщательно полобраны для того, чтобы исключить неблагоприятные воздействия, например, образования микротрещин в объеме пластика в результате испарения растворителя. Пластики могут быть сварены растворителем в результате воздействия теплоты или ультразвука. В расплавленном состоянии молекулы полимера могут переплетаться и образовывать соединение в конечном изделии.* В данном случае также необходимо обращать особое внимание на выбор материалов, так как при наїрсвс многие
|
[*ис. 6.4. Диаграмма, показывающая особенности эксперимента Ийенгора и Эриксона дли ПЭТ (полиэтилентерефгалата). соединенного с ПЭТ с помощью различных клеев. Установлено, что максимальное значение прочности клеевого соединения находится и такой точке, п которой параметр растворимости клея соответствует параметру растворимости ПЭТ (рисунок нз работы Мйснгэра и Эриксона) |
‘ О механизме сварки в расплаве см. Г. В. Комаров. Соединения деталей из полимерных материалов: Учеб, пособие. — СПб.: Профессия, 2006. — С. 337. Иримсч. иауч. ред.
пластмассовые детали могут существенно деформироваться. Оба рассмотренных варианта диффузионного соединения являются примерами проявления аутогезнн, в результате которой происходит самосцспление полимера.
Типичные поливинилонме клеи представляют собой раствор поливинилхлорида (IIBX) с пластификатором в смеси растворителей — тетрагилрофурана и толуола. Тетрагид|юфуран является превосходным раство])ителс. м для ПВХ и обеспечивает набухание прелназначепиых для склеивания виниловых поверхностей. В тот момент. когда растворитель еще присутствует в соединении, поливинилхлорид, находящийся в клее, диффундирует в субстраты и образует соединение. Такие соединения можно получать даже под водой.
 23 августа, 2015
23 августа, 2015  admin
admin 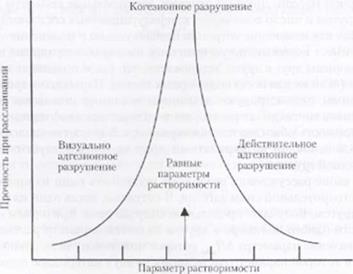
 Опубликовано в рубрике
Опубликовано в рубрике 