Многие ингибиторы претерпевают в электролите или на поверхности электрода химические превращения, и ингибирующее действие могут оказывать уже не первичные продукты, а вторичные. В связи с этам в литературе утвердилось два понятия — «первичное» ингибирование, которое обусловлено действием исходных
|
Рис. 4,14. Влияние соединений с кратными связями иа коррозию железа (порошок) *=24 ч; Г=20 °С: 1 — метилэтинилкетон; 2 — бромэтоксивинилацетилен; 3 — метилэтинилкарбинол; 4 — диме — тилэтинилкарбинол;; 5 —димер циклопентадиена; 6 —амиловый спирт; 7 — акрилонитрилу 8 — акриловая кислота; 9 — сорбиновая кислота; 10 — метакриловая кислота. |
продуктов, и «вторичное», обусловленное действием продуктов превращения. Путилова с сотр. [89], исследуя большое число органических соединений с кратными связями между атомами углерода и азота, установила, что в процессе ингибирования эти соединения претерпевают ряд превращений, приводящих к образованию продуктов гидрирования и неглубокой полимеризации. С возникновением на поверхности металла полимерных пленок и
связывается защита. Функциональные группы —О—Н, уС = 0, —СООН в эффективности защиты у играют второстепенную роль по сравнению с тройными связями. Предполагают, что механизм действия ацетиленовых соединений связан с восстановлением тройной связи выделяющимся в начальной стадии коррозионного процесса водородом.
Был изучен ряд веществ, содержащих двойные или тройные связи между атомами углерода и имеющих в a-положении по отношению к кратной связи различные функциональные группы. Эти соединения обладают относительно высокими защитными свойствами (рис. 4,14).
Была обнаружена относительно большая разница в скоростях растворения, определенных по потере массы и по количеству выделившегося водорода. Водорода всегда выделялось меньше: для 1 % диметилэтинилкарбинола, например в 3,7 раза. Это навело на мысль, что водород участвует в реакции образования защитного слоя. Кроме того, спектроскопические измерения показали, что концентрация непредельных веществ в растворе кислоты значительно убывает: так, содержание спиртовых групп в диметилэтилкарбониле уменьшилось на 25%, а концентрация акрилонитрила.
определенная по группе —CaN, на 65%. В ИК-спектрах появились новые полосы поглощения (2810 см-1 и 2710 см-1), свидетельствующие о химических превращениях акрилонитрила.
Доказательства в пользу «вторичного» ингибирующего эффекта получил Полинг [90], который методом ИК-спектроскопии обнаружил защитные полимерные пленки на поверхности железа после его пребывания в соляной кислоте, содержавшей ацетиленовые соединения: пропаргиловый спирт и этинилциклогексанкарбинол. По мнению автора, реакциями, приводящими к «вторичному» ингибирующему эффекту ацетиленовых соединений, является процесс гидрогенизации ацетиленовых ингибиторов водородом и каталитическое гидрирование ацетиленов при реакции полимеризации карбоксильных соединений:
Fe, неї
НС==СН + Н20 ————— >- Н2С=СНОН ———- Н3С— сно
В подтверждении этой гипотезы в пленках, возникающих на металле, методом ИК-спектроскопии обнаружены насыщенные углеводородные цепи, карбонильные, карбоксильные и гидроксильные группы.
Механизм защитного действия ацетиленовых соединений в соляной кислоте обсуждался также в работе Подобаева с сотр. [91]. Анализируя результаты, полученные при исследовании большого числа ацетиленовых производных, авторы пришли к заключению, что эти соединения действуют по адсорбционно-полимеризационно — му механизму; адсорбция ацетиленовых соединений на железе происходит главным образом по тройной связи; при этом на поверхности железа возникают полимерные пленки ацетиленовых соединений. Полярные группы в ацетиленовых соединениях влияют на я-связи ацетиленовой группы. Те из них, которые ослабляют я-связи, увеличивают вероятность адсорбции и полимеризации, поскольку химическая адсорбция ацетиленовых соединений возникает при разрыве одной из я-связей ацетиленовой группы. По степени ослабления тройной связи в ацетиленовых соединениях полярные группы располагаются в следующий ряд:
/>
ОН > — О — > =S > — СГ > —N= > — С1 (4,74)
Х)Н
При этом воздействие полярных групп на тройную связь максимально тогда, когда они находятся в положении 3 по отношению к тройной связи.
Хаккерман с сотр. [82] исследовал адсорбционные и ингибирующие свойства 4-этилпиридина и поливинилпиридинов с различными степенями полимеризации (от 4 до 10) и также пришел к выводу, что эти свойства обусловлены эффектом полимеризации соединений на поверхности металла.
Другой пример «вторичного» ингибирования дает дибензилсульфоксид. Большинство исследователей сходятся на том, что ин-
гибирующими свойствами в кислотах обладает, не сам сульфоксид, а продукты его восстановления, т. е. дибензилсульфид:
Подробное исследование ингибирующих свойств сульфоксидов с ароматическими и алифатическими цепями было выполнено Тра — банелли и Караситти с сотр. [62]. Авторы установили, что ингибирующие свойства соединений этого класса изменяются в следующей последовательности: дибензилсульфоксид>ди-н-бутил-
сульфоксид > ди-/г-толлилеульфоксид > дифенилсульфоксид > >тетраметиленсульфоксид>диметилсульфоксид. Электрохимические исследования указывают на то, что в данном случае наблюдается «вторичное» ингибирование, обусловленное соответствующими сульфидами, образующимися при восстановлении сульфоксидов. «Вторичное» ингибирование более сильно выражено у соединений с большей электронной плотностью на атоме серы (ди — н-бутилсульфоксид, дибензилсульфоксид).
Ароматические сульфоксиды (дифенил-, ди-н-толилсульфокси — ды) также обладают защитными свойствами, несмотря на то, что электронная плотность на атоме серы у них меньше из-за сопряжения. Защита в этом случае обусловлена низкой растворимостью образующихся при восстановлении сульфидов, которая способствует их концентрации (адсорбции) на поверхности металла.
 Кроме того, по мнению авторов, адсорбцию может облегчать одна из фенильных групп путем я-электрон — ной связи. (Низкомолекулярные диметил — и тетраметилсульфоксиды не обладают защитными свойствами из-за малой величины углеводородных цепей, которые дают небольшое покрытие, и из-за того, что продукты их восстановления имеют большое давление паров.)
Кроме того, по мнению авторов, адсорбцию может облегчать одна из фенильных групп путем я-электрон — ной связи. (Низкомолекулярные диметил — и тетраметилсульфоксиды не обладают защитными свойствами из-за малой величины углеводородных цепей, которые дают небольшое покрытие, и из-за того, что продукты их восстановления имеют большое давление паров.)
Дибензилсульфоксид, по-видимому, плохо адсорбируется на поверхности железа в кислотах, поэтому он слабо ингибирует коррозию. Однако в начальный момент под влиянием водорода, выделяющегося в результате коррозионного процесса, он может восстанавливаться до бензилсульфоксида, который лучше
адсорбируется и образует на поверхности металла полимолекулярные слои, прекращающие коррозионный процесс.
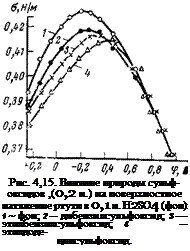
Защитные свойства и адсорбцию сульфоксидов изучал Островский [92], который показал, что сульфоксиды адсорбируются на ртути в широкой области потенциалов. Десорбция происходит лишь при относительно отрицательных потенциалах (—0,7 В для дибензилсульфоксида; —0,6 В для октилбензилсульфоксида; —0,5 В для этилдодецилсульфоксида). Максимум электрокапиллярной кривой тем ниже, чем асимметричнее молекула изученных соединений (рис. 4,15).
Данные ИК-спектров дибензилсульфоксида, полученные Швабе [93], свидетельствуют о том, что на поверхности электрода адсорбируется дибензилсульфид — продукт восстановления дибензилсульфоксида. Карасситти с сотр., исследуя продукты адсорбции дибензилсульфоксида с помощью УФ-спектроскопии, обнаружил полосы поглощения дибензилсульфоксида.
Полинг с сотр. [94] изучал адсорбционные спектры бутилнитрита и выяснил, что последний разлагается с образованием хемосорбированного углеводорода и окиси азота. Отсюда был сделан вывод, что ингибирующее действие бутилнитрита связано с хемосорбцией нейтральных молекул и продуктов их разложения, а также с окисляющим действием окиси азота.
По механизму «вторичного» ингибирования, очевидно, действует и тиокарбамид; как уже указывалось (см. стр. 125), тиокарб — амид и его производные под влиянием выделяющегося на электроде водорода восстанавливаются или окисляются кислородом воздуха с образованием сероводорода, аммиака, ионов серы и органических катионов. Защита в значительной степени обусловлена продуктами превращения тиокарбамида и его производных, в частности, сульфид-ионами, которые облегчают защиту по механизму, рассмотренному выше. Допускают, что в процессе ингибирования принимают участие и невосстановленные молекулы тиокарбамида, которые адсорбируются благодаря образованию электронной связи между атомом серы и атомами железа или никеля. Адсорбция тиокарбамида и его производных возможна также через азот аминогруппы, имеющий пару электронов. Таким образом, эффективность этих ингибиторов коррозии обусловлена наличием двух адсорбционно-активных центров и адсорбцией продуктов их разложения.
Эрмел и Хорнер [95] считают, что по механизму «вторичного» ингибирования подобно дибензилсульфоксиду действуют и четвертичные органические соединения ониевой формы, например производные мышьяка и серы. Однако, по мнению Фишера [96], такие ониевые производные, как трифенилбензилфосфоний и три — фенилбензиларсоний, изменяют скорость коррозии по механизму «первичного» ингибирования, адсорбируясь на электроде в виде ониевых солей.
 28 августа, 2015
28 августа, 2015  admin
admin 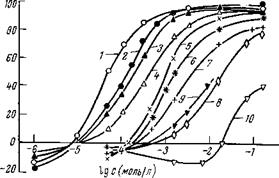
 Опубликовано в рубрике
Опубликовано в рубрике 