Как уже отмечалось, при травлении титановых сплавов, в особенности высокопрочных, может происходить наводороживание, часто приводящее к растрескиванию сплавов. Чтобы избежать этого, можно пойти двумя путями: изыскивать ингибиторы наводоро — живания или подбирать такие электролиты, которые бы не наво — дороживали титановые сплавы. Травление титановых сплавов можно производить в серной, соляной, фтористоводородной, азотной кислотах, а также в смесях их. Первые три кислоты наводо — роживают титан.
Степень наводороживания титана зависит как от концентрации атомного водорода на поверхности металла, определяющейся скоростью катодного процесса восстановления и молизации, так и от растворимости водорода в сплаве. Вследствие более высокой растворимости водорода в {5-титане по сравнению с растворимостью в а-титане сильнее наводороживаютея (а+Р)-сплавы и, особенно, однофазные {5-сплавы.
Выбор электролитов для травления титана, как правило, производится эмпирическим путем, но на основании современных данных электрохимической кинетики можно подбирать их научно обоснованно, принимая во внимание скорости травления и необходимость исключить нежелательный процесс наводороживания.
Общие требования, которым должны удовлетворять электролиты для травления титана, следующие [135].
1. Достаточно положительный стационарный потенциал титана, при котором основным катодным процессом является восстановление добавляемого в электролит окислителя; катодный ток за счет реакции восстановления водорода незначителен или полностью отсутствует, что существенно снижает или исключает наводороживание титана и его сплавов.
2. Достаточно высокая скорость анодного процесса растворения металла при этом потенциале.
При всей простоте идеи возможность ее реализации заранее предсказать трудно, поскольку введение в электролит больших концентраций окислителя может настолько замедлить скорость анодной реакции, что скорость травления уменьшится до значений, неприемлемых для практики (имеется в виду травление со скоростями ~0,1—0,8 мм/ч). Вместе с тем, чрезмерная активация анодного процесса с помощью неокислительной кислоты (НС1, HF) неизбежно приводит к наводороживанию. Поэтому необходимо найти оптимальные отношения пассиватора к активатору. В этом плане представляет особый интерес изучение системы HNO3—HF—Н20. Наиболее приемлемым является следующий метод исследования. Для основных компонентов предполагаемого электролита строятся катодные поляризационные кривые, по которым определяется концентрация окислителя, обеспечивающая необходимую скорость катодного процесса, а следовательно, и травления. Для выбранной скорости травления определяют потенциал травления, а по нему — ожидаемое соотношение скоростей катодного процесса по водороду и окислителю.
В табл. 7,6 представлены данные по травлению сплава ВТ-15 [А1 — 3-f-4; Сг— Юч-11,5 и Мо —7ч-8% (масс.)] в общепринятых водных травильных растворах. Как видно, все указанные электролиты, в том числе содержащие HN03, приводят к сильному наводороживанию сплава.
На рис. 7,3 приведены катодные поляризационные кривые, полученные на хроме, в смеси фтористоводородной и азотной кислот, содержащих постоянную концентрацию HF (20%) и различные концентрации HN03. В электролите без азотной кислоты (кривая 1) наблюдается предельный диффузионный ток в 40— 50 мкА/см2, который, очевидно, определяется растворенным в электролите кислородом. При более высоких плотностях тока начинается выделение Н2. При добавлении в раствор азотной кислоты на катодных кривых 2 и 3 появляется предельный диффузионный ток восстановления азотной кислоты, который выражен менее отчетливо в растворах с высоким содержанием HNO3. При содержании 60—80% HN03 (кривые 6—8) катодным процессом, обеопе-
|
Таблица 7,6. Наводороживание сплава ВТ-15 в различных электролитах
|
|
Рис. 7,3. Катодные поляризационные кривые в растворах [HN03—HF: % (об)] при различных концентрациях HN03: /-20% HF; 2 — 20; 3 — 30; 4 — 40; 5 — 50; 5-60; 7 — 70; 3 — 80% HNO3. |
чивающим достаточно высокие скорости травления титана 0,12 мм/ч, что соответствует 105 мкА/см2, является процесс восстановления азотной кислоты. Следовательно, потенциал травления + 0,2— + 0,4 В, исключающий протекание реакции выделения Н2, обеспечит достаточную скорость травления. Смещение потенциала травления в отрицательную сторону приведет к увеличению скорости катодного процесса, однако вероятность наводорожива — ния сплава при этом увеличится ввиду возможности протекания процесса с водородной деполяризацией.
Для подтверждения правильности предлагаемого метода выбора электролитов для травления и всестороннего изучения влияния отдельных компонентов построили тройную диаграмму системы HN-Оз—HF—Н20, отражающую зависимость потенциала травления сплава ВТ-15 от соотношения компонентов (рис. 7,4).
Как видно, область положительных потенциалов, определенная по катодным поляризационным кривым, располагается в верхнем углу диаграммы, при этом содержание азотной кислоты должно быть не менее 30%.
Из рис. 7,5, отражающего влияние соотношения компонентов системы HN03—HF—Н20 на скорость травления сплава ВТ-15, видно, что в найденной нами области положительных потенциалов наблюдаются достаточно высокие скорости травления сплава.
|
HNOa 0,71 л* |
|
60 МАО о, зб ом /ч% А Л / / ■ л> If. О 0,27 0,ЗГ 0,32 0,32 0,39 „ л Л A A A 7V А О и Ы? SO 0,290,3$ 0,30 0,33^0,ЗГ ^ ии /к………. д-Д -~А~а— . , 60 0,29 0,260,23 0,19 0,210,15 0,27 ^ 70 0 гШдО-О, V — J’iSrpO0,72=f),67 00 пп oJ^yJ*rbG7/ Ч^У 4—4 7 |
|
“Ч ьи *Q А 60 & |
|
mr’p,4y т^- і о М 10 20 30 W 50 60 10 ВО 90 * [н2о]; % |
 |
|
Рис. 7,4. Влияние соотношения концентраций кислот в системе HNO3—HF—Н20
на электродный потенциал титанового сплава ВТ-15.
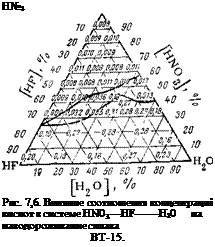
Рис. 7,5. Влияние соотношения концентраций кислот в системе HNO3—HF—Н20
на скорость травления (мм/час) титанового сплава ВТ-15.
Содержание водорода в образцах после травления в смесях системы HNO3—HF—Н2О приведено па диаграмме рис. 7,6, из которой следует, что травление сплава ВТ-15 при отрицательных значениях потенциалов, как и было предсказано, вызывает сильное наводороживание. При положительных же потенциалах травления, очерченных на рис. 7,4, наводороживание незначительно или вообще отсутствует. Однако граница между областями наво — дороживания и ненаводороживания выражена нечетко, что обусловлено факторами, влияющими на характер катодного процесса (перемешивание, температура электролита и т. п.).
Таким образом, полученные результаты показывают, что на основе электрохимических исследований можно научно обоснованно выбирать составы электролитов для травления титановых сплавов без наводороживания. Достаточно по катодным поляризационным кривым определить скорость катодного процесса, обеспечивающего заданную скорость травления, и потенциал, исключающий протекание реакции восстановления иона водорода. Прибавлением к выбранному окислителю (HNO3) активатора (HF) устанавливают соотношение компонентов, обеспечивающее нужный потенциал травления.
Электролиты, пригодные для травления сплава ВТ-15, с некоторым запасом HN03, исключающим возможность случайного попадания в опасную зону потенциалов, судя по диаграмме, должны иметь следующий состав: 50-f70% HN03+30-f50% HF или
30-f42% HN03 + 9-f16°/o HF. На рис. 7,6 эта область составов очерчена.
Один из этих электролитов (36% HNO3+ 16% HF) был изучен более подробно. Травление в таком электролите не только сплава
ВТ-15, но и других титановых сплавов практически исключает их наводороживание (табл. 7,7). В данном электролите можно травить и химически фрезеровать без наводорожи — вания как a-сплавы (ВТ-1, ВТ5-1 и др.), так и а+Р-спла — вы и р-оплавы (ВТ-14, ВТ-15, ВТ-16 и др.).
 Многолетний промышленный опыт травления изделий из высокопрочных титановых сплавов ВТ-14, ВТ-15, ВТ-16 в электролите, содержащем 36% HNO3 и 16% HF, показал, что в нем исключается наводороживание и достигаются приемлемые скорости травления (химическое фрезерование).
Многолетний промышленный опыт травления изделий из высокопрочных титановых сплавов ВТ-14, ВТ-15, ВТ-16 в электролите, содержащем 36% HNO3 и 16% HF, показал, что в нем исключается наводороживание и достигаются приемлемые скорости травления (химическое фрезерование).
В работе [139, с. 226, 230] травление труб из титанового сплава ВТ-14 (а + Р) рекомендуется производить в следующих электролитах: 4—5% HF+40—50% HN03 и 2% HF+8% HN03. Для удаления окалины с титановых труб применяется щелочно-кислотный метод, заключающийся в выдержке в течение 1 ч в щелочном растворе 70—75% NaOH с добавкой 5% NaCl и 20—25% NaN03 при Г—4304-450 °С и последующем травлении в кислом растворе, содержащем 2,0—2,5% HF и 8—10% HN03, в течение 30—40 с.
Брынза с сотр. [139, с. 246] рекомендует для удаления окалины с титана (860°С) раствор, содержащий 40% Н3РО4, 25% H2S04
|
Таблица 7,7. Содержание водорода в различных титановых сплавах после травления в электролите (36% HN03+16% HF)
|
и 5% Na2SiF6. При этом, по утверждению авторов, стадия обработки изделий в щелочном окислительном растворе исключается.
Работники Верхне-Салдинского завода [139, с. 250] испытали большое число травильных растворов на основе серной кислоты и фтористых соединений и пришли к заключению, что по долговечности и экономичности лучшим для снятия окалины с титановых сплавов является раствор, содержащий 20% H2SO4 и 4% NH4F.
 3 сентября, 2015
3 сентября, 2015  admin
admin 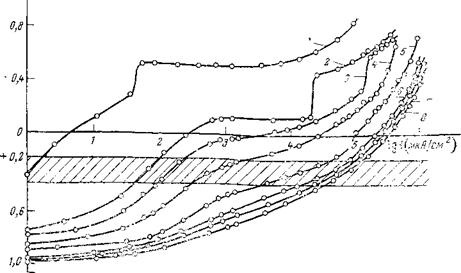
 Опубликовано в рубрике
Опубликовано в рубрике 