Окалина с легированных сплавов удаляется с большим трудом, что связано с наличием в ее составе окиси хрома Сг203 и шпинели Fe0-Cr203, практически не растворяющихся при температурах до
80 °С в минеральных кислотах (H2S04, НС1, HN03). Поэтому приходится прибегать для удаления окалины с таких сплавов к смесям кислот или предварительному разрыхлению окалины. Один из рекомендованных [142] электролитов содержит: 47,5% НС!
(пл. 1,19)+5% HN03 (пл. 1,4) и 47,5% Н20. Режим травления для различных сталей следующий:
|
Сталь |
і, мин |
||
|
рыхление В HNO3 |
траЕление в HCJ или НСИ HNO3 |
пассивирование в HN03 |
|
|
Х13Н4Г9 |
3 |
10—25 |
2-3 |
|
Х18Н9 |
5-20 |
15-50 |
7—12 |
|
1Х18Н9Т |
10-30 |
20—70 |
7—12 |
Рыхление и пассивирование производят в 7,8%-ной HN03 (40—50°С). Травление — в 18%-ной НС1 или 18% НС1 + 5% HN03.
Сообщается [144] также об успешном применении для травления нержавеющих сталей смеси 15% H2SO4+10% Fe2(S04)3. Предполагают, что сульфат трехвалентного железа, являясь сильным окислителем, переводит низшие малорастворимые окислы хрома в высшие окислы (Сг03, СГ2О7), которые хорошо растворимы в кислотах. Однако, судя по данным наших работ [55], не исключено, что сульфат трехвалентного железа выступает в качестве катодного деполяризатора, ускоряющего растворение чистого металла под окалиной. Эффективность этого раствора была проверена Жетвиным с сотр. [142] на стали Х25Н20С2. Оказалось, что потери металла в нем ниже, чем в электролите, содержащем НС1 и HN03 (1,5—1,9% вместо 3%).
|
2. НМ03(пл. 1,4) —8 — 20% HF — 1 — 4% Н20 — до 100% 4. НС1 (пл. 1,19)-25% HN03 (пл. 1,42)—3% Н20 — до 100%* 6. HN03—8 —12% HF — 2 — 5% Н20 — до 100% |
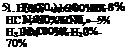 |
Для облегчения удаления окалины с легированных сталей в электролит часто добавляют галогенид-ионы, которые являются активаторами. Вытесняя кислород из окислов, они облегчают их растворение. Для этих целей применяют фториды и хлориды. Кроме того, вводят также селитру NaN03, анион которой в кислых электролитах легко восстанавливается и выступает в качестве сильного катодного деполяризатора. Предложен и ряд других смесей электролитов [ 142]:
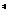 Применяется, когда необходимо получить блестящую поверхность.
Применяется, когда необходимо получить блестящую поверхность.
Для предварительного рыхления окалины рекомендуется кислый электролит следующего состава:
H2S04 (пл. 1,84)—6—8%; НС1 (пл. 1,19)—2—4%; Н20 — до 100%.
Наибольшее распространение в металлургической промышленности для рыхления окалины, возникающей на нержавеющих, жаропрочных я жаростойких сталях, получили растворы щелочи и селитры. Обработка сталей в расплаве каустической соды и селитры (400—520 °С) сильно облегчает последующее удаление окалины кислотами. Значительная часть рыхлой окалины удаляется паром воды при охлаждении стали водой. Для удаления остальной окалины и придания поверхности блестящего вида сталь после обработки в расплаве и охлаждения травят 10—12% НС1 или смесью 15—18% H2SO4+3—5% NaCl (Г=60—70 °С, *=3-г10 мин). После травления сталь пассивируют в 5—8%-ной HN03 (Т = = 50—55°С, t=2-4-3 мин).
По данным [142], 15—18%-ная H2SO4 медленно удаляет окалину после щелочного рыхления. Добавка 3% Nad ускоряет процесс удаления окалины, а качество протравленной поверхности получается таким же, как при травлении в соляной кислоте. Хлористый натрий, кроме того, выступает в роли ингибитора наводо — роживания: количество абсорбированного сталью водорода уменьшается в несколько раз. Объясняется это тем, что хлорид-ионы выступают в качестве сильных ингибиторов коррозии, уменьшая скорость растворения стали после удаления окалины. Это хорошо иллюстрируют данные, приведенные в табл. 7,3.
Добавка хлористого натрия к серной кислоте в то же время ускоряет процесс растворения окалины, что можно видеть из данных, приведенных в табл. 7,4. Таким образом, введение 3—5% Nad в 18% H2S04 ускоряет процесс растворения окалины с хромоникелевых и хромистых сталей и уменьшает коррозионное воздействие кислоты на чистый металл.
|
Таблица 7,3. Влияние NaCl на скорость растворения сталей в 18% H2S04 (Г=70 °С; t= 1 ч) к, г/(м2■ ч) при cNaC1 (в г/л)
|
По данным Богоявленской [139, с. 17], хлористый натрий может облегчить удаление окалины с некоторых котельных трубных сталей (12Х1МФ, 15Х1М1Ф, ЭП756), если его применять и в процессе термической обработки. Рекомендуется перед термической обработкой в полости труб засыпать хлористый натрий из расчета 0,6—0,9 кг/м2. Такая солевая обработка способствует получению более рыхлой окалины, которая частично откалывается при охлаждении труб, остальная удаляется при кислотном травлении.
Исследования, выполненные на заводе «Серп и Молот» [142]. показали, что лучше всего разрыхляет окалину с минимальными потерями металла расплав следующего состава: NaOH (60—65%), NaN03 (ЗО—35%) и NaCl (5%) (7’=400—450°С). Механизм щелочного травления, по данным [139, 142], можно представить в следующем виде:
1) перевод труднорастворимой окиси хрома щелочью в хромит
Сг203 + 2NaOH——- >- 2NaCr02 + Н20 (7,9)
2) окисление хромита азотнокислым натрием до легко растворимого хромата
2NaCr02 3NaNOs + 2NaOH ———- >- 2Na2Cr04 + 2НаО + 3NaN02 (7,10)
3) перевод хромита железа в окиси хрома и железа, а также окислов железа низшей валентности в окислы более высокой валентности
2Fe0-Cr203 + NaN03 ——— v Fe203 + 2Cr203 + NaN02 (7,11)
2FeO + NaN03 ——— >• Fe203 + NaNOa (7,12)
2Fe304 + NaN03 ——— >- 3Fe203 + NaNOa (7,13)
Перевод окислов типа шпинелей (хромита железа), которые практически не растворяются во всех минеральных кислотах, сначала в окислы хрома, а потом в хорошо растворимые хроматы, несомненно, облегчает удаление окалины в кислотах. Что же касается перевода окислов железа низшей валентности (FeO, Fe304)
|
Таблица 7,4. Влияние NaCl в 18% H2S04 на скорость растворения окалины, снятой со стали 2X13
|
Таблица /,5. Оценка качества травления легированных сплавов в различных электролитах [температура комнатная* предварительное рыхление окалины в NaOH (200 г/л) + КМп04 (50 г/л) при 80 °С; / = 30 мин]
|
Сталь |
Оценка качества травления |
|||||||||||
|
« О Г» ос ty Zu, ££ |
о о т}* о X и., XX |
о т w о X X |
о ю 1^ 2и. 03 XX |
о см ^ СІ 2 UhU 05 03 XXX |
о § о С: 00 ^ gbj* ххх |
Ю. о t" О ^ ‘Ю з 8-J? XX X |
ч-vO О Ю о СП х;®22 XXX |
|| Д* сою 9о~ %хх XXX |
с? о У ^ «50 S о ‘— 03 life? 1—’ оо§5 34 К! 33 XXX |
— о <£> "Т w" СІ со „о их XX |
о о С4 о о 00 ю «м -—- "V С4 ЕО £ж |
|
|
ЭИ57 |
У— |
п |
х+ |
У |
У |
У |
У |
У+ |
_ |
______ |
У |
|
|
ЭИ 83 5 |
У— |
У— |
X— |
У |
У |
У |
у+ |
У+ |
— |
У |
У |
п |
|
ЭП750 |
У |
У— |
X— |
п |
У |
У— |
У— |
У— |
У— |
— |
У |
п |
|
ЭП73! |
п |
п |
У— |
п |
X— |
п |
п |
У— |
— |
— |
У— |
п |
|
ХІ8Н9 |
у+ |
п |
У |
У |
п |
X— |
У— |
X— |
У— |
— |
У— |
_ |
|
Х17Н8 |
п |
у+ |
X |
У |
У— |
X— |
У |
X— |
п |
— |
У— |
_ |
|
ЭГ156 |
У— |
У— |
п |
п |
п |
п |
п |
У— |
— |
У |
У— |
У— |
|
XIGH6 |
п |
X |
у+ |
Х2 |
У-Ь |
У— |
у+ |
У |
У |
у+ |
У— |
У— |
|
ЗП699 |
п |
п |
у+ |
У |
п |
У— |
У— |
У— |
У |
X— |
У |
п |
|
ЭП679 |
У |
X |
— |
У+ |
X |
у+ |
X |
у+ |
X |
у+ |
У |
Обозначения: X — Окалина удаляется полностью, поверхность светлая, нет растрава, шлам удаляется струей воды.
У — На поверхности остаются участки неудаленной окалины, легкое растравливание, шлам удаляется с трудом. П — Окалина удаляется не полностью, поверхность растравливается, шлам удаляется с трудом.
* Цифры при формулах — концентрации в г/л.
![]() В ОКИСЛЫ более ВЫСОКОЙ валентности (Fe203), то это вряд ли может облегчить удаление окалины в кислотах, поскольку Fe203 труднее растворяется в кислотах, нежели FeO и Fe304.
В ОКИСЛЫ более ВЫСОКОЙ валентности (Fe203), то это вряд ли может облегчить удаление окалины в кислотах, поскольку Fe203 труднее растворяется в кислотах, нежели FeO и Fe304.
Как предполагают авторы, в процессе высокотемпературного окисления в расплаве окалина, по-видимому, претерпевает объемные и структурные изменения, которые приводят к механическому отслаиванию ее.
Весьма перспективным при удалении окалины является гид — ридный способ, в котором используются восстановительные свойства гидрида натрия. Обработка стали в щелочном расплаве с восстановителем NaH (360—400 °С) приводит к восстановлению труднорастворимых окислов до металла или окислов более низкой степени окисления:
Cr203 + NaH ———— > 2CrO + NaOH (7,14)
Fe304 + 4NaH >- 3Fe + 4NaOH (7,15)
Восстановленный слой металла или окисла легко удаляется водой или кислотой. Гидридный способ удаления окалины является универсальным и высокопроизводительным. Он позволяет удалить окалину с самых разнообразных сплавов и в 5—10 раз производительнее щелочно-кислотного и кислотного методов. К его недостаткам следует отнести сложность аппаратурного оформления.
Изучение большого числа электролитов, предложенных для травления нержавеющих сталей с окалиной, возникающей при термической обработке, проведенное нами совместно с Красноруцкой, Остаповичем [145], показало, что ни один из них не обладает способностью удалять окалину одновременно со многих марок сталей (табл. 7,5). Это создает неудобства на машиностроительных заводах, где, как правило, применяются стали ферритного, полуферритного, мартенситного и аустенитного классов.
В процессе поиска оптимального состава электролита, способного удалять окалину о большинства применяемых в промышленности сплавов без существенного растворения основного металла и образования трудноудаляемого шлама, была всесторонне исследована двухкомпонентная смесь HN03 + HF. После широкой вариации состава было найдено, что наиболее универсальными свойствами обладает раствор HN03 (140-=-150 ry0i)+HF (50-f — — F60 т/л) (температура комнатная). Этот электролит обеспечивает быстрое удаление окалины почти со всех изученных сплавов, не травит основной металл после удаления окалины и не образует трудно удаляемого шлама. Время удаления окалины указано ниже[13]:
Сталь…………………………….. ЭП56 Х18Н9 Х17Н8 ЭП679 ЭП680
![]() *, мин……………………………… 9,5—4 80 70-80 10 3
*, мин……………………………… 9,5—4 80 70-80 10 3
Сталь ………………………………… Х16Н6 ЭП699 ЭП750 ЭП731 ЭП835 ЭП57
t, мин…………………………………… 20 25 40 100 20 20
Растворение металла без
окалины, мкм… — 5,5—7,0 — 0,15 2,4 0,3
Изучение коррозионной стойкости сталей после удаления окалины этим электролитом показало, что он пассивирует поверхность, сталь не наводороживается и не приобретает склонности к коррозиоінному растрескиванию.
 2 сентября, 2015
2 сентября, 2015  admin
admin  Опубликовано в рубрике
Опубликовано в рубрике 