После проделанного анализа можно сформулировать условия безопасности применения ингибиторов: анодные ингибиторы безопасны только в тех случаях, когда скорость коррозии контролируется всецело анодной реакцией. Плотность тока, возникающая на той части электрода, которая осталась по каким-либо причинам в активном состоянии, остается в таких условиях такой же, как и в исходном электролите. При смешанном контроле скорости коррозии анодные ингибиторы в концентрациях, не обеспечивающих полную пассивацию металла, вызывают увеличение интенсивности коррозии. Чем с большей поляризуемостью электрода протекает анодная реакция в исходном электролите, тем ниже интенсивность коррозии в присутствии ингибитора и тем менее опасным является такой ингибитор. Высокая катодная поляризуемость металла в исходном электролите, наоборот, способствует увеличению интенсивности коррозии в электролите, содержащем недостаточную для полной защиты концентрацию анодных ингибиторов.
Применяя анодные ингибиторы, необходимо определить порог концентраций, при котором анодный ингибитор становится опасным, защитную его концентрацию в растворе, а также обеспечить равномерный доступ ингибитора ко всем частям конструкции.
Разумеется, что безопасными должны быть такие анодные ингибиторы, которые тормозят анодную реакцию, не изменяя при этом соотношения между активной и пассивной частями электрода. Самыми опасными при концентрациях, не обеспечивающих полную защиту, являются ингибиторы, вызывающие усиленную анодную поляризацию вследствие частичной пассивации металла и в то же время являющиеся хорошими деполяризаторами катодного процесса.
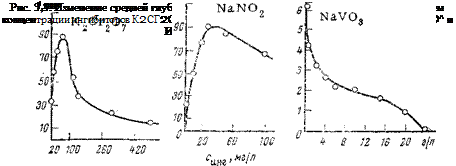
Сформулированные выше закономерности подтверждаются экспериментально. На рис. 3,3 показано, как изменяется глубина коррозионных поражений (интенсивность коррозии) в присутствии нитрита натрия, бихромата калия и метаванадата натрия. Малые концентрации нитрита натрия и бихромата калия, как и следовало ожидать, приводят к увеличению глубины коррозии.
Метаванадат натрия, не пассивирующий частично электрод и не изменяющий в широкой области концентрации соотношение меж-’ ду пассивной и активной частями электрода, не увеличивает глубины коррозии, а, наоборот, непрерывно ее уменьшает (в данном случае она совпадает со скоростью коррозии) по мере увеличения концентрации ингибитора в электролите.
Катодные ингибиторы во всех случаях безопасны, так как в любых концентрациях они уменьшают скорость и интенсивность коррозии.
Смешанные ингибиторы менее опасны, чем чисто анодные, и в ряде случаев могут не приводить к росту интенсивности коррозии. При преимущественном торможении катодного процесса их свой-
ства приближаются к катодным, т. е. они становятся совершенно безопасными.
 Рассмотрим менее изученный случай, обнаруженный в последнее время, когда защита металла осуществляется с помощью нитробензоатов аминов благодаря увеличению эффективности катодного процесса. В тех случаях, когда концентрация ингибитора превышает защитную, металл переводится в пассивное состояние, в случаях же, когда концентрация ингибитора выбрана неправильно, потенциал металла хотя и становится более лоложитель — e f 0 — (/ , , ным, но оказывается еще в обла-
Рассмотрим менее изученный случай, обнаруженный в последнее время, когда защита металла осуществляется с помощью нитробензоатов аминов благодаря увеличению эффективности катодного процесса. В тех случаях, когда концентрация ингибитора превышает защитную, металл переводится в пассивное состояние, в случаях же, когда концентрация ингибитора выбрана неправильно, потенциал металла хотя и становится более лоложитель — e f 0 — (/ , , ным, но оказывается еще в обла-
‘ 4 аиг ы, т^ сти активного растворения. При
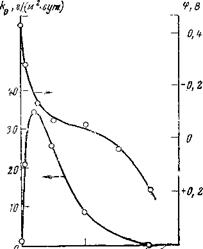
Рис. 3,4. Зависимость скорости общей этом может возрастать не толь — коррозии k0 и электродного потенциа — ко интенсивность коррозии ла <р стали от концентрации динитро — но и суммарный коррозионный бензоата пиперидина в 1 н. Na2S04. эффект /г0 (рис 3,4)
Возможность частичной пассивации металлов анодными ингибиторами не исключает, однако, их успешного применения. Для того чтобы избежать локального развития процесса, необходимо лишь следить за тем, чтобы концентрация ингибитора не снизилась ниже защитной. Контроль осуществляется обычно периодическим анализом электролита на содержание ингибитора. Кроме того, поскольку независимо от природы ингибитора и его защитной концентрации полная пассивация стали достигается при одном и том же значении потенциала (для 0,1 н. NaaS04 фп. п=0,20-г — +0,25 В), полноту защиты можно контролировать по значению потенциала, который необходимо предварительно установить для каждого электролита.
При этом надо различать три случая: 1) ингибитор изменяет лишь окислительно-восстановительный потенциал системы, не изменяя анодной реакции; 2) изменяется окислительно-восстановительный потенциал системы и уменьшается скорость катодной реакции; 3) изменяется окислительно-восстановительный потенциал системы и возможна частичная пассивация электрода.
В первом случае независимо от того, какой реакцией определяется скорость коррозии, коррозионный ток в системе возрастает и скорость процесса будет выше, чем в неингибированном электролите. Во втором случае увеличение скорости коррозии, вызванное изменением эффективности катодного процесса, будет несколько ослаблено замедлением анодной реакции и, в принципе, эти два противоположно действующих фактора могут друг друга уравновесить настолько, что скорость коррозии не изменится. Наиболее
опасным является третий случай, поскольку увеличение эффективности катодного процесса сопровождается частичной пассивацией электрода, а это должно привести к увеличению интенсивности коррозии. Что касается влияния на интенсивность коррозии катодной и анодной поляризуемостей, то при этом будут проявляться те же закономерности, которые рассмотрены выше.
 25 августа, 2015
25 августа, 2015  admin
admin  Опубликовано в рубрике
Опубликовано в рубрике 