Соли бора, и в частности тетраборат натрия Na2B407 (бура), перборат натрия NaB03-4H20, а также борат натрия Na3B03 часто вводят в состав ингибиторных смесей, применяемых для защиты металлов от коррозии. Их эффективность в значительной степени определяется тем, что они обладают большой буферной емкостью и поэтому позволяют регулировать и поддерживать необходимое значение pH. На основе боратного буфера можно создать ряд эффективных смесей, которые дают возможность защищать от коррозии разнообразные сочетания металлов. Например, смесью бората натрия и бензотриазола удается защитить от коррозии системы, состоящие из стали, чугуна, меди и т. д.
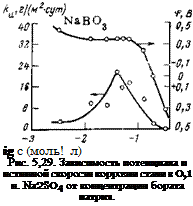
Представление о защитных и пассивирующих свойствах NaB03 можно получить из данных, приведенных на рис. 5.29. Этот ингибитор, как и другие рассмотренные выше, при концентрациях, не достаточных для полной защиты стали от коррозии, увеличивают истинную скорость коррозии, поэтому кривая зависимости скорости коррозии от концентрации проходит через максимум. При концентрации NaB03, равной 0,314 моль/л, коррозия стали в 0,1 н. Na2S04 полностью прекращается. Электродный потенциал при этом изменяется по-другому: в широкой области концентрации он не меняется и лишь при концентрации ингибитора 0,1 моль/л начинается сильное смещение потенциала в положительную сторону. Полная защита достигается при <<р«+0,3 В.
Слабое изменение потенциала в широкой области концентраций NaB03, сопровождающееся увеличением скорости коррозии, требует специального исследования. Оно может наблюдаться в случае, когда ингибитор ускоряет одну из коррозионных электродных реакций или обе сразу в одинаковой степени. Судя по тому, как этот ингибитор частично пассивирует электрод (см. рис. 2,17), эффект от увеличения эффективности обычного катодного процесса восстановления кислорода невелик. Поэтому не исключено, что NaB03 оказывает непосредственное влияние на кинетику катодной реакции, участвуя в процессе деполяризации. При больших концентрациях ингибитора (0,1 моль/л) наступает резкий сдвиг потенциала в анодную сторону, который сопровождается падением скорости коррозии. Это однозначно указывает на замедление ингибитором анодной реакции.
 Такая зависимость скорости коррозии и потенциала от концентрации NaB03 отражается и на характере поляризационной кривой k (<р) (см. рис. 2,17): на участке активного растворения при незначительном смещении потенциала в положительную сторону наблюдается сильный рост скорости коррозии. Однако начиная с потенциала ~—0,35 В отмечается сильное падение скорости растворения. Поскольку пассивная часть электрода при этом не меняется в широкой области концентраций ингибитора, падение скорости коррозии в активно-пассивной области потенциалов обусловлено торможением анодной реакции.
Такая зависимость скорости коррозии и потенциала от концентрации NaB03 отражается и на характере поляризационной кривой k (<р) (см. рис. 2,17): на участке активного растворения при незначительном смещении потенциала в положительную сторону наблюдается сильный рост скорости коррозии. Однако начиная с потенциала ~—0,35 В отмечается сильное падение скорости растворения. Поскольку пассивная часть электрода при этом не меняется в широкой области концентраций ингибитора, падение скорости коррозии в активно-пассивной области потенциалов обусловлено торможением анодной реакции.
 30 августа, 2015
30 августа, 2015  admin
admin  Опубликовано в рубрике
Опубликовано в рубрике 