Адсорбция полимеров имеет свои специфические особенности по сравнению с адсорбцией низкомолекулярных веществ. Независимо от химического состава как аморфные, так и кристаллизующиеся олигомеры и полимеры всегда ассоциированы и образуют надмолекулярные структуры в виде доменов, статистических клубков, пачек, ламелей фибриллярных образований и сплошных сеток, которые ступенчато переходят от первичных к вторичным и далее. Степень ассоциации, т. е. размер, форма и прочность структур в растворах, зависит от молекулярной массы полимера, длины, гибкости и разветвленности цепей, от концентрации его в растворе, термодинамических свойств растворителей, а также от температуры. Значение адсорбции меняется в областях изменения степени (ступеней) ассоциации молекул олигомеров и полимеров.
Синтетические олигомеры и полимеры (пленкообразователи) всегда полидисперсны по молекулярной массе и адсорбцию можно рассматривать как адсорбцию многокомпонентных систем, в которых существенное значение могут иметь эффекты фракционирования. Теплота смачивания твердой поверхности полимерами будет всегда меньше теплоты смачивания мономерами того же химического состава и строения. Высоко структурированные полимеры могут вообще не смачивать твердую поверхность.
В отличие от низкомолекулярных веществ общая теплота адсорбции олигомеров и полимеров ХЗ&дс из концентрированных растворов может бытыиШШщт’льной, так как она является алгебраической суммой положительной теплоты адсорбции полярных групп и неполярных сегментов молекул полимеров Qu отрицательной теплоты десорбции многих молекул ранее адсорбированных на этой поверхности газов, растворителей, мономеров Q2, отрицательной теплоты разрушения межмолекулярных и внутримолекулярных связей в ассоциатах фз и в надмолекулярных структурах полимеров Qi’.
iQw-QI-(Q* + Q»+QA). (3.7)
Отрицательная теплота адсорбции полимеров тем выше, чем больше концентрация их в растворе, а следовательно, чем выше степень структурирования.
Повышение температуры, как правило, не уменьшает, а увеличивает количество адсорбируемых олигомеров и полимеров. На увеличение адсорбции с ростом температуры оказывает влияние и энтропийный фактор, поскольку энтропия полимеров при адсорбции уменьшается.
Термодинамически «хорошие» растворители сольватируют молекулы полимеров, способствуют развертыванию клубков и разрушению других надмолекулярных структур, высвобождая отдельные молекулы, и тем способствуют адсорбции их на твердой поверхности в виде толстого адсорбционного слоя. Это свойство хороших растворителей особенно пропил яется при адсорбции из концентрированных растворов. В «плохом» растворителе молекулы полимеров находятся в свернутом состоянии в виде клубков и при адсорбции образуют более слабо связанный слой. Налипшие шорым и последующими толстыми слоями (аглютинированные) полимерные образования легко отмываются «хорошим» растворителем. Одновременно растворители сами могут адсорбироваться на активных центрах тердой поверхности, конкурируя с большими молекулами полимеров.
При низких (до 2 %) концентрациях полимеров в растворах еще имеются свободные сольватированные большим количеством растворителя молекулы, которые, адсорбируясь параллельно поверхности, образуют тонкий адсорбционный сольватный слой. Большие молекулы закрепляются лишь отдельными сегментами с функциональными группами. Участки цепи при этом направлены в раствор отдельными петлями (рис. 3.5).
С повышением концентрации полимеров в растворе в них образуются первичные, а затем вторичные надмолекулярные структуры, которые и переходят из раствора на твердую поверхность. Статистические клубки, переходя из раствора на поверхность пигментов дают «мономолекулярный» толстый слой из деформированных — сжатых клубков.
При концентрациях выше 35—50 % (для разных пленкообразовате — лей), называемых критическими, образуются вторичные сетчатые фибриллярные структуры. Вязкость растворов при этом резко возрастает, а адсорбция полимера становится затруднительной; адсорбируется преимущественно растворитель. Концентрация полимера в растворе при этом
|
Рис. 3.5. Схема состояния адсорбированных молекул полимеров на твердой поверхности: / — горизонтальная ориентация; 2 — вертикальная ориентация; 3 — адсорбция клубка, 4 адсорбция пачки, 5 — петлеобразное состояние; б — асспцииты клубков |
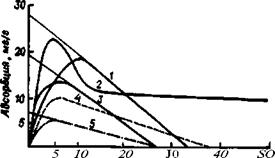
Рис. 3.6. Изотермы адсорбции олигомеров на поверхности диоксида титана из растворов в различных растворителях при 20 °С и <р = 20%: алЛсид ПФ-060; эпо-
![]()
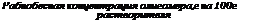
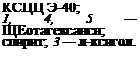 |
возрастает — «отрицательная» адсорбция (область // на рис. 3.4). Поэтому изотермы адсорбции полимеров из растворов в отличие от классических изотерм Ланг-
мюра в большинстве случаев имеют экстремальный характер (рис. 3.6).
Количество низкомолекулярных веществ, в том числе и ПАВ, адсорбируемых из растворов на твердой поверхности, обычно определяют по разности концентраций растворенного вещества до начала адсорбции С и после ее проведения Сг. Отнеся это количество к массе G или площади поверхности пигмента S, получают кажущуюся адсорбцию Акаж,’
![]() ЛКаж=(С,-С2) tn/G,
ЛКаж=(С,-С2) tn/G,
где т — общая масса раствора полимера.
Лишь в случаях, когда концентрация растворенного вещества очень мала и растворитель совершенно не адсорбируется, Акаж = Гадс и изотерма адсорбции будет лангмюровской (см. рис. 3.3).
Обычно изотермы адсорбции из растворов пленкообразователей с пигментами имеют максимумы в области концентраций растворов 2— 5 % (масс), соответствующей началу образования в растворах ассоциа — тов. Именно при этой концентрации отмечается наибольшая теплота смачивания и наибольшая поверхностная активность полярных молекул олигомеров и полимеров.
Переход в адсорбционный слой сольватированных молекул и их ассо- циатов, удерживающих растворители в количестве, превышающем их собственную массу в 5—10 раз, изменяет как состав, так и массу равно — весного раствора после адсорбции. Поэтому адсорбционные слои следует называть адсорбционно-сольватными, а в формуле расчета адсорбции (3.8) величины Сг и га должны быть скорректированы. По экспериментально найденным изотермам с максимумом можно определить значение неопределенным изотермам с максимумом можно определить значение истинной адсорбции полимера А, экстраполируя прямолинейный участок изотермы до оси ординат, как показано на рис. 3.6. Определение количества адсорбированного вещества методом сжигания дает хорошо совпадающие результаты.
Величина насыщения поверхности пигмента Гмакс определяется из уравнения
г — кме (3-9)
где К — константа, характеризующая способность данных веществ к адсорбции; М — масса адсорбируемых молекул полимера; а — коэффициент, характеризующий состояние молекул в адсорбционном слое.
Если а**0, имеет место горизонтальное расположение молекул (см. /Л§фНс *<Г)Ь В этом случае количество адсорбированного вещества
не зависит от молекулярной массы. Если qt = l, имеет место вертикальная ориентация (см. 2 на рис. 3.5), и количество адсорбированного вещества пропорционально его молекулярной массе, если 0 < а < 1 (на практике а = 1/э-г Уг). то молекулы адсорбируются, петлями (см. 5 на рис. 3.5). Отдельные сегменты проявляют «якорный эффект», закрепляя на поверхности макромолекулы. О расположении адсорбированных молекул судят также по поверхности занимаемой одной молекулой в адсорбционном слое, но в этом случае не учитывается реальная рабочая поверхность и расположение активных центров поверхности пигментов, и расчет ведется на общую геометрическую поверхность, что справедливо только в случае физической адсорбции. Адсорбция макромолекул отдельными сегментами или определенными активными центрами уменьшает фактическую плотность упаковки в адсорбционных слоях и вызывает их разрыхленность.
Характерной особенностью адсорбции полимеров является ее необратимость, за исключением случаев физической адсорбции молекул с вертикальной ориентацией (см. 2 на рис. 3.5). Однако необратимость адсорбции полимеров далеко не во всех случаях является доказательством хемосорбции. Необратимость объясняется многоточечностью закрепления при одновременном взаимодействии с твердой поверхностью многими сегментами макромолекулы (см. /, 3, 5 на рис. 3.5). Энергия физической связи каждого адсорбционного контакта составляет 8,4—12,5 кДж/моль, и при большом числе контактов общая энергия связи макромолекул становится соизмеримой с энергией химической связи, поэтому удалить такие молекулы промывкой растворителями не всегда удается.
Полимеры, адсорбированные из плохих растворителей, адсорбируются в виде свернутых клубков — глобул и под влиянием силового поля твердой поверхности могут деглобулизироваться, развертываясь вдоль поверхности и увеличивая число связей (см 3 и / на рис. 3.5), что сопровождается вытеснением одной макромолекулой большого числа ранее адсорбированных малых молекул в раствор.
Механизм формирования адсорбционно-сольватных слоев. Адсорбционное равновесие между пигментами и пленкообразователями устанавливается, проходя через последовательно протекающие процессы адсорбции диффузионно подвижных низкомолекулярных компонентов и последующего их вытеснения более высокомолекулярными соединениями. Большие молекулы, изменяя свою конформацию, мигрируют отдельными сегментами от одних активных центров твердой поверхности к другим и закрепляются, находя положения, отвечающие минимуму поверхностной энергии Гиббса. Закрепление происходит несколькими функциональными группами. При этом в раствор вытесняется большое количество ранее адсорбированных малых молекул. Такой механизм формирования адсорбционных слоев пленкообразователеЙ на пигментах доказан методом жидкостной хроматографии. Изменение состава раствора пленкообразователя, прошедшего через хроматографическую колонку, заполненную пигментом, показано на рис. 3.7. В раствор могут вытесняться вещества, не только физически адсорбированные, но и хемосорбированные, например жирные кислоты вытесняются более сильной фталевой кислотой.
В результате избирательной адсорбции поверхностью пигментов состав пленкообразователя до установления адсорбционного равновесия заметно изменяется: уменьшается содержание больших молекул с функциональны — ми группами адсорбируемыми активными центрами поверхности пигментов.
По объему раствора, удерживаемого пигментом до установления равновесия по всем показателям, V = Vi — V отнесенному к массе пиг-
|
мента в колонке G, можно наиболее точно определить минимально необходимое количество пленкообразователя для диспергирования:
i4 = 100(Va-Vi)/G. (3.10)
Ориентация и конформация молекул пленкообразователя могут изменяться не только при непосредственном контакте с твердой поверхностью, но и в прилежащих к ней слоях молекул, расположенных на расстоянии нескольких микрометров от поверхности. Под влиянием силового поля твердой поверхности молекулы теряют подвижность. Поверх относительно малоподвижного слоя, прилежащего непосредственно к твердой поверхности, создается более толстый и рыхлый слой с повышенной вязкостью. На его образование значительное влияние оказывает межмолекулярное взаимодействие. Однако в результате ограничения сегментной подвижности плотность упаковки макромолекул в адсорбционном слое ниже, чем в объеме полимера. Ограничение твердой поверхностью подвижности больших молекул, т. е. обеднение конформационного набора, связано с энтропийным фактором и объясняет слабую зависимость строения адсорбционных слоев от химической природы и жесткости цепей макромолекул пленкообразователей.
Кинетические закономерности адсорбции. Кинетика адсорбции определяется не только скоростью диффузии молекул пленкообразователя, но более медленными процессами разрушения надмолекулярных структур и изменением ориентации и конформации молекул в адсорбционном слое. Ускорение этих процессов достигается повышением температуры и, в меньшей мере, механическим путем — изменением скорости сдвига. Как было показано ранее, суммарный тепловой эффект адсорбции полимеров чаще бывает отрицательным, и для ускорения адсорбции требуется приток теплоты извне. Нагревание лакокрасочной системы до 50—55 °С, когда разрушаются водородные связи, не только ускоряет установление адсорбционного равновесия, но необходимо для формирования межфазного адсорбционно-сольватного слоя. Так, для установления адсорбционного равновесия в динамических условиях в системе пентафталевый лак ПФ-060 — диоксид титана Р-02 (1 : 1) в зависимости от температуры необходимо следующее время:
При более высоких температурах происходят нежелательные процессы испарения растворителей и преждевременного пленкообразования.
Изотермы адсорбции при 10 и 20 °С в начальный период, до установления адсорбционного равновесия, имеют максимумы и ступени. При 50—55 °С ступени на изотермах исчезают, максимумы сглаживаются. На изотермах, отвечающих разбавленным (ниже 18 %) растворам пентафта — левого лака ПФ-060 имеется лишь незначительный максимум. Все это свидетельствует о наличии вторичных процессов перераспределения и изменения конформации макромолекул и их отдельных сегментов в адсорбционном слое после перехода в него из раствора ассоциатов и надмолекулярных структур олигомеров.
В общем виде скорость установления адсорбционного равновесия при адсорбции олигомеров и полимеров из растворов может быть описана следующим уравнением:
u==/(f(1-6), (З. П)
где К — константа для данной системы; / — функция, характеризующая гибкость цепей полимера 9 — доля, поверхности пигмента, занятая молекулами полимера или олигомера
Время установления истинного адсорбционного равновесия — время «созревания» красочных систем — имеет большое практическое значение, так как определяет необходимый объем смесителей для составления эмалей.
3.3. ВЛИЯНИЕ ПИГМЕНТОВ НА СТРУКТУРУ И СВОЙСТВА ЛАКОКРАСОЧНЫХ ПОКРЫТИЙ
 3 сентября, 2015
3 сентября, 2015  admin
admin 
 Опубликовано в рубрике
Опубликовано в рубрике 