Прокаливание осажденного сернистого кадмия. Прокаливание сернистого кадмия приводит к значительному улучшению его свойств, При этом процессе удаляется адсорбированная вода, разрушаются основные соли, выгорает свободная сера, а главное, резко уменьшаются реакционная способность и поверхностная активность. И, действительно, сернистый кадмий после прокаливания теряет свою способность вступать в реакцию обменного разложения с солями тяжелых металлов, в частности меди. При прокаливании также улучшается и светостойкость пигмента.
Оптимальной температурой прокаливания сернистого кадмия является 550—600°. При более высокой температуре, а именно при 650—700° начинается окисление сернистого кадмия кислородом воздуха в окись и отчасти в сернокислый кадмий. Температура воспламенения сернистого кадмия 730—740°.
Сернистый кадмий, получаемый при прокаливании, обладает золотисто-желтым цветом. Изменение соотношения между реагентами и условия прокаливания не влияют заметным образом на цвет CdS, поэтому сернистый кадмий иных оттенков — лимонного, светло-желтого и оранжевого — по данному методу получать не удается.
Оказалось, однако, что прокаливание в присутствии сернистого цинка способствует значительному посветлению CdS и при этом удается получать пигменты более светлых оттенков, вплоть до лимонного. Обычно применяют ZnS в количестве 0,2 моля при получении светлого и 0,5 моля — лимонного кадмия на моль CdS. Более светлая окраска в присутствии сернистого цинка объясняется не только его разбеливающим действием, но и специфическим влиянием в процессе реакции на свойства сернистого кадмия.
По литературным данным, яркость и интенсивность кадмиевых пигментов улучшаются при прокаливании с гидратом окиси алюминия.
Сернистый кадмий для прокаливания получают взаимодействием водорастворимой соли кадмия (CdS04, CdCl2) с сернистым натрием, сернистым барием или гипосульфитом.
. ‘При работе по гипосульфитному методу операции осаждения и прокаливания сернистого кадмия могут быть совмещены таким образом, что гипосульфит расплавляют в его кристаллизационной воде при нагреве до 60—80°, добавляют в расплав размолотый сернокислый кадмий или его смесь с ZnO и размешивают при той же температуре для получения однородной массы и частичного упаривания раствора.
Загустевшую массу затем прокаливают, промывают и сушат. Для получения светлых оттенков в состав реакционной массы вводят не водорастворимые соли цинка, а окись цинка или углекислый цинк, которые нейтрализуют выделяющуюся при реакции серную кислоту и переходят в сернокислый цинк. Последний затем реагирует с гипосульфитом аналогично сернокислому кадмию:
Zn0 + H2S04 —У ZnS04~fH20
ZnS04 + 2Na2S208 —► ZnS + S02-f S +2Na3S04
Обычно для получения светло-желтого кадмия добавляют 20—24% ZnO по отношению к соли кадмия (считая на CdO), а для получения лимонного кадмия добавляют 34—40% ZnO [48, 53].
При работе с расплавом процесс получения пигмента значительно упрощается благодаря исключению ряда промежуточных операций, а вследствие применения избытка гипосульфита прокаливание происходит в восстановительной среде.
Прокаливание окиси или легко диссоциирующих солей кадмия с серой. При прокаливании окиси кадмия с серой образуется сернистый кадмий. Окись кадмия вначале восстанавливается до
металла, который затем реагирует с серой с образованием сернистого кадмия:
2CdO — ф S —». S02 + 2Cd 2Cd + 2S —► 2CdS 2CdO + 3S —S02-f 2CdS
Вместо окиси кадмия целесообразнее брать углекислый или щавелевокислый кадмий, диссоциирующие при прокаливании на окись кадмия и углекислый газ:
CdC03 "рокалнвзнно CdO + C02; CdC204 CdO — j — C02 + CO
При этом окись кадмия получается в более активном, реакционноспособном состоянии, а выделяющийся углекислый газ предупреждает преждевременное выгорание серы за счет кислорода воздуха.
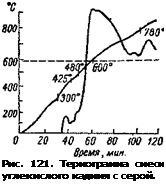 На рис. 121 приведена термограмма смеси углекислого кадмия с серой (65% CdC03 + 35% S). Температурные эффекты имеют место при 300, 425, 480 и 600°; они вызваны разложением углекислого кадмия, образованием сернистого кадмия и его окислением под действием кислорода воздуха [49].
На рис. 121 приведена термограмма смеси углекислого кадмия с серой (65% CdC03 + 35% S). Температурные эффекты имеют место при 300, 425, 480 и 600°; они вызваны разложением углекислого кадмия, образованием сернистого кадмия и его окислением под действием кислорода воздуха [49].
Серу обычно вводят в шихту в значительно большем количестве, чем это следует из расчета, так как часть ее сгорает в кислороде воздуха. Прокаливание производят при 500—600°. Цвет получаемого пигмента золотистожелтый. Для получения светлых оттенков к смеси добавляют окись цинка, которая также реагирует с серой с образованием сернистого цинка по реакции:
2ZnO-f3S —► 2ZnS +S02
Сернистый кадмий наиболее светлого оттенка образуется при введении в шихту окиси цинка в количестве —45% к количеству окиси кадмия. Получается светло-желтый кадмий примерного состава CdS*0,25 ZnS. Добиться еще более светлого оттенка за счет увеличения количества окиси цинка не удается. Темно-желтые и оранжевые оттенки при работе по этому методу достигаются путем добавления к смеси углекислого кадмия и серы небольших количеств селена.
Причина многоцветности сернистого кадмия, т. е. способности к различной окраске при постоянном химическом составе не выяснена в достаточной степени до настоящего времени. Различную окраску сернистого кадмия раньше объясняли неодинаковой степенью полимеризации молекул, причем сернистый кадмий лимон-
ного цвета рассматривали как мономер CdS, а оранжевый — как полимер:
Cd—S—Cd—S—Cd
S—Cd—S—Cd—S
Однако в дальнейшем не удалось обнаружить такую связь между цветом и степенью полимеризации сернистого кадмия. Поскольку сернистый кадмий полиморфен, можно было бы объяснить многоцветность различной окраски той или иной модификации, но на практике это также не подтверждается. По-видимому, основным фактором, обусловливающим цвет сернистого кадмия, является физическое состояние частиц: их величина, характер поверхности, агрегация и т. д. Сернистый кадмий темно-желтого и оранжевого цвета состоит из более крупных частиц, чем светлый и лимонный. Однако одной лишь величиной частиц нельзя объяснить все известные различия цвета и оттенков, так как большие кристаллы гринокита окрашены в желтый, а не в темно — или оранжево-желтый цвет [42].
Технологический процесс
Существуют многочисленные методы получения желтых кадмиевых пигментов с применением различных солей кадмия (CdSO. i, CdCI2, CdC03, CdC204 и др.), соединений, содержащих серу (S, H2S, Na2S, BaS, Na2S203, CS2 и др.), и добавок. При этом могут видоизменяться и условия осаждения и прокаливания. Наибольшее значение имеют методы осаждения сернокислого или хлористого кадмия сернистым натрием, сернистым барием или гипосульфитом с последующим прокаливанием полученного осадка, а также метод прокаливания смеси углекислого кадмия с серой. При этом учитываются особенности каждого метода, а именно: легкость получения светлых сортов при работе с гипосульфитом, золотисто-желтых (средне-желтых) и оранжевых сортов при применении сернистого натрия, золотисто-желтого при прокаливании смеси углекислого кадмия с серой и кадмопонов при осаждении сернистым барием.
Осаждение желтого кадмия производят в деревянных, фарфоровых или эмалированных баках, прокаливание — в муфельных или вращающихся печах.
Сырье, применяемое для производства кадмиевых пигментов (как желтых, так и красных), должно быть химически чистым, так как даже небольшие примеси тяжелых металлов: никеля, свинца, меди, железа и других — значительно ухудшают цвет пигментов.
 27 августа, 2015
27 августа, 2015  admin
admin  Опубликовано в рубрике
Опубликовано в рубрике 