Лакокрасочная промышленность выпускает пигментированные лакокрасочные материалы различных цветов и оттенков. Наиболее распространенными являются пигменты светлых оттенков. Обычно материалы светлых оттенков готовят на основе смесей пигментов; при этом содержание белых пигментов в смеси составляет до 80% (масс.). Таким образом, белые пигменты используют для изготовления не только белых, но и цветных лакокрасочных материалов.
В соответствии с классификацией группа белых пигментов представлена двумя классами химических соединений: оксидами и солями. Оксиды представлены двумя основными белыми пигментами— диоксидом титана и оксидом цинка (цинковыми белилами), на долю которых приходится подавляющая масса всех выпускаемых промышленностью пигментов. Из солей применение находят сульфид цинка, который чаще используется в виде литопона (ZnS+BaS04), и карбонат свинца (свинцовые белила). Литопон хотя по свойствам сильно уступает диоксиду титана и цинковым белилам, но зато значительно дешевле, что позволяет широко его использовать для получения строительных красок. Свинцовые белила находят ограниченное применение из-за исключительно высокой токсичности.
Диоксид титана
Свойства. Диоксид титана ТіОг может кристаллизоваться в тетрагональной и ромбической сингониях. В тетрагональной синго — нии диоксид титана имеет две модификации: анатаз и рутил, а в ромбической одну модификацию — б р у к и т. Последняя модификация не обладает пигментными свойствами, поэтому практического применения не находит.
Свойства анатаза и рутила различаются:
TOC o "1-3" h z Анатаз Рутил
Плотность, кг/м3 3700—3900 3700—4200
Твердость по Моосу, усл. ед. 5,5—6,0 6,0—6,5
Показатель преломления По10 2,55 2,70
Укрывистость, т/и2 35—45 30—40
Удельная поверхность, мг/г 9—15 7—20
Разбеливающая способность, усл. ед. 1150 1500
Спектры отражения рутила и анатаза характеризуются высоким отражением во всей видимой области и различаются в коротковолновой (менее 0,430 мкм) области, в которой рутил отражает примерно вдвое меньше, чем анатаз, поэтому он кажется желтее анатазной модификации. Белизна пигмента зависит и от степени дисперсности. С ее повышением пигмент кажется более белым, так как мелкие частицы повышают рассеивающую способность в коротковолновой части спектра и уменьшают в длинноволновой части. Повышению белизны диоксида титана Способствуют также добавки флуоресцирующих красителей (оптических отбеливателей).
Диоксид титана способен образовывать с оксидами переходных металлов твердые растворы. При этом искажается кристаллическая решетка, и пигмент приобретает цветовой оттенок. Рутил более чувствителен к действию примесей, чем анатаз, поскольку легче образует с ними твердые растворы.
Для диоксида титана характерны явления фототропии и фотохимической активности. Фототропия проявляется в потемнении образцов диоксида титана, загрязненных примесями Fe, Сг, Ni, Мп и др. При освещении такие образцы становятся коричневыми, а в темноте вновь белеют. Объясняется это окислением находящихся в пигменте примесей в высшие оксиды. В темноте высшие оксиды вновь переходят в низшие.
Фотохимическая активность диоксида титана проявляется в ускоренном разрушении покрытий, в которых он содержится. Это обусловлено тем, что титан в диоксиде координационно не насыщен и катализирует окислительную деструкцию пленкообразователя. Пигмент при этом обнажается и может быть легко удален с поверхности покрытия. Происходит меление, которое проявляется тем в большей степени, чем более склонен к окислительной деструкции олигомер. Для снижения фотохимической ^активности пигмент подвергают модификации путем осаждения «а поверхности частиц соединений Al, Si, Zn и др.
Недостатком диоксида титана (особенно анатазной модификации) является и его гигроскопичность. Это приводит к замедлению отверждения покрытий, а также к снижению их водопроницаемости. Для уменьшения гигроскопичности используют поверхностное модифицирование пигмента.
Диоксид титана химически инертен. Он не растворяется в Большинстве органических и неорганических кислот (кроме концентрированной серной кислоты при нагревании и плавиковой), — слабо растворяется в щелочах.
Получение. Диоксид титана получают в промышленности двумя методами: сульф атным и хлорид ным. Сырьем являются титансодержащие руды, из которых наиболее ценными являются ильменит и рутил. Кроме того, могут использоваться высокопроцентные титановые шлаки, содержащие большое количество титана (до 75—80% ТЮ2).
Сульфатный метод. В отечественной промышленности наиболее широко используется сульфатный метод получения диоксида титана. Ильменитовый концентрат, являющийся основным сырьем этого метода, состоит из титаната железа FeO-ТЮг. Содержание ТЮ2 в концентрате в зависимости от месторождения колеблется в пределах 44—60% (масс.), а содержание FeO — в пределах 18—35%. Кроме того, в состав концентрата входит до 18% Fe203 и в значительно меньшем количестве Si02, А1203, MgO, СаО, Сг203 и другие оксиды. Содержание хрома и тяжелых металлов в сырье не должно превышать 0,3%.
Технологический процесс включает четыре основные стадии: получение растворов сульфата титана; получение продукта гидролиза; термическую обработку продукта гидролиза; поверхностную обработку диоксида титана. Таким образом, производство пигментного диоксида титана осуществляется по комбинированному (осадочно-прокалочному) способу. Весь технологический цикл включает большое число операций. Это один из самых сложных многостадийных производственных процессов получения пигментов.
Получение растворов сульфата титана включает в себя несколько операций: разложение титан? одержащего сырья; выщелачивание плава; восстановление Fe3+ в Fe2+; очистку раствора от шлама; выделение FeS0,r7H20; концентрирование раствора.
Разложением называется операция обработки титансодержа — щего сырья серной кислотой. Скорость и степень разложения зависят от состава сырья и степени его измельчения, концентрации и количества серной кислоты, а также от температуры обработки. Обычно используется серная кислота концентрацией 85—89%. Количество ее должно быть достаточным для образования сульфатов всех металлов, входящих в состав сырья.
При взаимодействии концентрата с серной кислотой протекают следующие реакции:
ТЮ2 + H2S04 — Ti0S04 + Н20; FeO + H2S04 — FeS04 + H20; Fe203 + 3H2S04 — Fe2(S04)3 + 3H20.
Сульфаты других металлов, входящих в состав сырья, образуются аналогично.
Разложение проводят в специальном аппарате с коническим днищем, футерованном кислотоупорным материалом. В него заливают концентрированную (92—93%-ную) серную кислоту и затем при постоянном перемешивании сжатым воздухом загружают предварительно высушенный н измельченный концентрат. В зимнее время смесь подогревается паром до 80—90 °С, который подается через коническое днище аппарата. При конденсации пара происходит разбавление серной кислоты до концентрации 85—89% (масс.). В летнее время разбавление кислоты до этой концентрации проводят подачей в аппарат холодной воды.
Процесс разложения титансодержащего сырья протекает с выделением тепла, за счет которого реакционная масса нагревается до 180—220 °С с бурным выделением большого количества газов и паров воды. Реакционная масса вспенивается и увеличивается в объеме. Иногда даже происходит ее выброс из аппарата. По окончании бурной реакции, которая длится несколько минут, масса начинает затвердевать. Степень разложения сырья при этом составляет 85—87%. Для получения пористого плава через массу пропускают сжатый воздух. После этого происходит «вызревание» и охлаждение массы в течение 2—3 ч. Степень разложения концентрата в период вызревания возрастает до 95—97%.
Охлажденный до 8.0—90 °С плав подвергают выщелачиванию водой. При этом сульфаты титана, железа и других металлов переходят в раствор.
Полученный после выщелачивания плава раствор направляют на операции восстановления Fe3+ в Fe2+. При этом часть Ti4+ переходит в Ті3+ (до 3—5 г/л). Наличие в растворе некоторого количества Ті3+ препятствует обратному окислению Fe2+ в Fe3+. Операцию восстановления проводят при 70— 75 °С в присутствии железных опилок, стружек или нарезанных отходов листового черного металла.
Раствор после восстановления освобождают от шлама, который представляет собой в основном неразложившнйся концентрат и диоксид кремния. Предварительно проводят коагуляцию тонкодисперсных частиц шлама, образующих в растворе неоседающую взвесь. В качестве коагулянтов используют различные поверхностно-активные вещества (поливиниловый спирт, сульфа — нол, альбумин, некаль и др.).
Осветленный раствор поступает на вакуум-кристаллизацию для выделения кристаллического продукта FeS04-7H20. Кристаллизация железного купороса достигается охлаждением раствора до 10—15 °С за счет испарения воды в вакууме. Кристаллы железного купороса отделяют центрифугированием, а очищенный раствор сульфата титана упаривают. Полученный раствор называется предгидролизньм. Раствор имеет сильнокислую реакцию. Содержание серной кислоты в нем характеризуется величиной кислотного фактора, т. е. отношением содержания активной кислоты (свободной и связанной с титаном) к содержанию солей титана в пересчете на ТЮ2. Для предгидролиз — ного раствора величина кислотного фактора составляет 1,9—2,1.
Получение продукта гидролиза состоит из следующих операций: приготовление зародышей; гидролиз раствора сульфата титана; отмывка н отбелка продукта гидролиза; его солевая обработка.
Растворы сульфата титана гидролизуют при нагревании с выделением в осадок нерастворимого гидроксида титана. Процесс этот значительно ускоряется в присутствии так называемых зародышей. Последние представляют собой тонкодисперсную взвесь гидроксида титана в воде. Частички взвеси могут иметь как анатазную, так и рутильную структуру. Введением в пред — гидролизный раствор зародышей определенной структуры можно вести направленный синтез пигмента необходимой кристаллической модификации.
Анатазные зародыши получают из растворов сульфата титана (до упаривания) разбавлением их водой н нейтрализацией раствором NaOH. Полученную суспензию выдерживают для вызревания при 60 °С в течение нескольких часов, а затем охлаждают. Концентрация готовых зародышей — около 25 г/л ТЮ2.
Рутильные зародыши готовят из отбеленного продукта гидролиза обработкой его концентрированным раствором гидроксида натрия при нагревании и повышенном давлении. Полученную суспензию отмывают от избытка щелочи, нейтрализуют хлороводородной кислотой, кипятит в присутствии, ТіС14 и разбавляют до концентрации около 50 г/л ТЮг.
Гидролиз растворов сульфата титана проводят в стальных аппаратах, футерованных кислотоупорными плитками н снабженных освинцованными мешалками и змеевиками для нагрева н охлаждения реакционной смеси. Предгидролизный раствор нагревают до 60 °С, вводят зародыши в количестве 0,2—0,5% (в пересчете на ТЮ2) и доводят до кипения (107—110 °С), При достижении степени гидролиза 70—75% к суспензии добавляют воду в количестве 35—40% по отношению к начальному объему раствора. Разбавлением снижают концентрацию кислоты в конце гидролиза и этим способствуют повышению степени гидролиза, так как высокий кислотный фактор замедляет скорость процесса. В результате гидролиза 95—97% титана переходит в осадок. Серная кислота и соли Fe2+ и других металлов обычно остаются в растворе.
Продукт гидролиза представляет собой гидратнрованный диоксид титана ТіОг-пНгО, который обладает значительной адсорбционной способностью. Кроме того, в продукте гидролиза содержится значительное количество сульфатных ионов.
По окончании гидролиза суспензию охлаждают и фильтруют для отделения осадка. Получаемая при этом гидролизная сернаи кислота имеет концентрацию 20—25%. Ее направляют на утилизацию. Осадок отмывают водой и затем очищают от возможных примесей соединений железа и других металлов. Поскольку от результата этой операции зависит белизна готового пигмента, ее называют отбелкой. Для проведения отбелки суспензию, содержащую около 300 г/л ТЮ2, обрабатывают 5—10%-ной чистой серной кислотой с добавлением цинковой пыли и нагревают до 90—95 °С. Отбелку ведут до появлення в растворе Ti2(S04)3 в количестве около 0,5 г/л. При этом присутствующие примеси металлов (Fe, Сг, V) восстанавливаются и переходят в раствор. Их отмывают от осадка водой.
Отбеленная суспензия подвергается солеобработке, которая проводится по-разному в зависимости от того, какой модификации должен быть получен продукт. При получении анатаза к суспензии добавляют K2SO4 (нли К2СО3) и фосфорную кислоту. Добавка фосфорной кислоты (0,5—0,6%) при последующей термической обработке продукта гидролиза способствует сохранению анатазной структуры. Кроме того, при этом улучшается формирование частиц пигмента, тормозится их чрезмерный рост и ускоряется выделение S03. Добавка K2SO4 (0,5—1,0%) способствует росту частиц и ускорению выделения С03.
После солеобработки высушенный продукт гидролиза подвергают термической обработке для получения диоксида титана. Прн этом происходят обезвоживание продукта гидролиза, удаление S03 и процессы структурооб — разовання. Вода удаляется при 200—300 °С; прн более высоких температурах (до 1000 °С) протекают все остальные процессы, на которые в значительной
Степени влияют добавки, введенные при солеобработке. Обычно анатаз получают при температуре около 900 °С, а рутил — при температуре около 850 °С. На качество диоксида титана в значительной степени влияют условия прокаливания, поэтому этот процесс контролируется по цвету ТЮ2 и его интенсивности.
Продукт после прокаливания охлаждают и направляют на измельчение и поверхностную обработку. Измельчение можно проводить сухим способом или мокрым в присутствии жидкого стекла и гидроксида натрия.
Поверхностная обработка (модификация) проводится с целью улучшения пигментных свойств диоксида тнтана путем осаждения на частицах соединений алюминия и цинка, а также органических веществ.
Отходами производства диоксида титана сульфатным методом являются значительные количества гидролизной кислоты (2 т 10%-ной H2S04 на 1 т ТЮ2) и железного купороса (3,5— 4,5 т на 1 т ТіОг).
Некоторое количество гидролизной кислоты используется при разложении сырья и выщелачивании плава. Основная же масса ее подвергается выпариванию в аппаратах с погружными нагревателями. Упаренная кислота (75%-ная) используется для травления железа и в производстве удобрений. Разбавленные кислотные стоки, которые образуются при промывках, нейтрализуют известью. Железный купорос применяют в производстве же- лезооксидных пигментов.
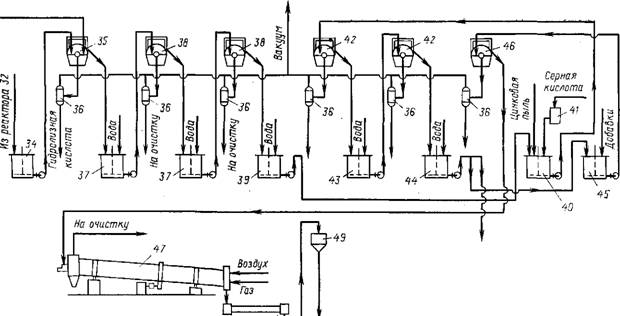
Технологическая схема производства пигментного диоксида титана сульфатным методом приведена на рис. 5.14.
Разложение концентрата проводят в аппарате 1, куда его подают из бункера 2, через питатель 3 шнеком 4. Серную кислоту заливают из мерника 5. Воду подают в аппарат через жидкостный счетчик 6. Восстановление Fe3+ в Fe2+ проводится в двух последовательно установленных аппаратах 7, снабженных мешалками и змеевиками для обогрева. Металлическую стружку или опилки загружают в первый аппарат 7 из бункера 8. Коагуляция и отстаивание примесей проводятся в отстойнике непрерывного действия 9. Шлам из него сливают в емкость 11, снабженную мешалкой и змеевиком для обогрева. Осветленный раствор собирают в емкости 12, откуда подают на вакуум-кристаллизаторы 13. Выпавший осадок железного купороса отделяют от раствора в отстойнике 15 и центрифуге 16. Чистый раствор подвергают контрольной фильтрации на фильтре 18 и собирают в емкости 19. Для упаривания этого раствора используются два аппарата 20. Анатазиые зародыши готовят в аппарате 23, в который подается раствор сульфата титана из емкости 19 и раствор NaOH из мерника 24. Рутильные зародыши готовят в аппарате 25, в который ТіС14, НС1 и раствор NaOH подают из мерников 26—28, А суспензию — из емкости 44.
Гидролиз растворов титана проводят в реакторе 32, снабженном мешалкой и змеевиком для подачи пара или воды. Зародыши дозируются в реактор мерниками 30 и 31. Предгидролизный раствор поступает из емкости 22, А вода—через жидкостной счетчик 33. По окончании гидролиза полученную суспензию сливают в емкость 34, откуда ее подают на вакуум-фильтр 35 С намывным слоем для отделения гидролизной кислоты, которую затем направляют иа утилизацию, а продукт гидролиза подают в репульпатор 37, где его отмывают водой. Из репульпатора 37 суспензия поступает на вакуум — фильтр 38. Вторая отмывка продукта гидролиза проводится аналогично. Отмытый продукт разбавляют водой в емкости 39 и подают на отбелку в аппарат 40. Сюда же подают серную кислоту из меринка 41 и цинковую пыль,
После отбелки суспензию фильтруют на вакуум-фильтре 42, репульпируюг для отмывки от солей в репульпаторе 43 и вновь фильтруют. В емкости 4T Отбеленную суспензию вновь разбавляют водой и подают на солевую обработку в аппарат 45. Затем после отделения на вакуум-фильтре 46 воды от продукта его подают на термообработку во вращающуюся трубчатую печь 47. Готовый продукт охлаждают в барабане 48 и через бункер 49 подают на сухое или мокрое измельчение.
Основными недостатками сернокислотного метода производства диоксида являются многостадийность и сложность процесса, а также значительный расход серной кислоты. К достоинствам этого метода можно отнести возможность использования сравнительно бедного титансодержащего сырья.
Хлоридный метод. При этом методе в качестве основного сырья используют рутиловые концентраты и титанистые шлаки с высоким содержанием титана. По этому методу технологический процесс включает следующие основные стадии: хлорирование сырья с целью получения тетрахлорида титана; очистку тетрахлорида титана; перевод тетрахлорида в диоксид титана; последующую обработку диоксида титана.
Тетрахлорид титана — бесцветная или слабоокрашениая жидкость, дымящая на воздухе вследствие образования твердых продуктов гидролиза с влагой. Химически активное вещество. Получают ТіСЦ хлорированием титансодержащего сырья при 700—1000 °С в присутствии восстановителей! (обычно кокса). При этом протекают реакции:
ТЮ2 + 2С + 2С12 — ТІС!4 + 2СО;
ТЮ2 + С + 2С12 — TiCt4 + С02.
При хлорировании образуются не только ТіС14, но и хлориды примесей, содержащихся в исходном сырье. Очистка тетрахлорида титана от примесей является сложным процессом. Он включает отделение от ТіС14 твердых и растворимых примесей и ступенчатую ректификацию. Процесс сложен и в аппаратурном оформлении вследствие высокой реакционной способности ТіС1« и необходимости полной герметизации аппаратуры.
Диоксид титана из ТІСЦ может быть получен тремя способами: гидролизом водного раствора, парофазным гидролизом и сжиганием в кислороде.
Способ гидролиза водных растворов TiCU практического значения не имеет, так как отходом его является хлороводородная кислота с концентрацией 10—15%, которая не находит применения. Кроме того, рутильный диоксид титана, полученный этим способом, значительно уступает по свойствам рутилу из сернокислых растворов.
|
18* |
Парофазный гидролиз протекает с одновременным обезвоживанием продуктов гидролиза при 300—400 или 900—1100 °С. Этим способом можно получить диоксид титана с высокими пигментными показателями как анатазной, так и рутильной модификации. Однако и этот способ практического значения не имеет.
|
Сухой, измельченный кон |
|
Церн а я кислота |
|
Коагулянт
|
|
В аппарат 25 |
|
Рис. 5.14. Технологическая схема производства пигментного диоксида титана сульфатным методом: |
|
Ю -j |
|
На измельчение и дополнительную обработку |
Намывной слой (гидролизная кислота + древесная мука)
1 — аппарат для разложения концентрата; 2, 8, 49— бункера; 3— питатель; 4 — шнек; 5, 10, 21, 24, 26—28, 30, 31, 41 — мерники: 6, 33 — Жидкостные счетчики; 7 — аппарат для восстановления оксида железа; 9, 15 — отстойники; 11, 12, 14, 17, 19, 22, 34, 39 и 44 — емкости; 13 — вакуум-кристаллизатор; 16 — центрифуга; 18 — фильтр; 20 — ваиуум-вьшарные аппараты; 23—аппарат для приготовления анатазных зародышей; 25— аппарат для приготовления рутильных зародышей; 29 — поглотительная колонна; 32 — реактор; 35, 38, 42, 46 — вакуум- фильтры; 36 — гидравлический затвор: 37, 43 — репульпаторы; 40 — аппарат для отбелки; 45 —аппарат для солеобработки; 47 — трубчатая печь; 43 — охладительный барабан
Наибольшее применение имеет способ сжигания ТіСЦ в кислороде:
ТіСІ4 + 02- ТІ02 + 2СІ2.
Эта реакция необратима. Ее проводят в присутствии избытка кислорода, причем последний предварительно осушают во избежание образования НС1. Выделяющийся при этом хлор вновь используют при получении ТіСЦ из титансодержащего сырья. Использование хлора в замкнутом технологическом процессе является большим преимуществом этого способа, поскольку дает возможность резко сократить количество отходов. Сжиганием ТіСЦ в кислороде можно получать диоксид титана как анатаз — ной, так и рутильной модификации. Первый получается при температурах 1000—1100 °С, а второй —при 1300 °С.
Процесс получения пигмента сжиганием ТіСЦ в кислороде очень сложен, так как вследствие высокой скорости реакции возможно образование ТЮ2 с дефектной кристаллической решеткой и большой поверхностной активностью. При высокой температуре образующиеся частицы пигмента склонны к агрегации и спеканию. Для облегчения регулирования процесса можно разбавлять кислород азотом, но это диктует необходимость регенерации хлора на его смеси с азотом.
Из-за сильного корродирующего действия ТіСЦ и хлора аппаратурное оформление процесса также оказывается сложным. Основными видами аппаратуры являются испарители ТіСЦ, перегреватели паров ТіСЦ и кислорода,, горелки, реакционные аппараты и улавливающие устройства.
В настоящее время в качестве источников нагревания наибольшее значение имеют плазмотроны. Для получения плазмы используется вольтова дуга или индукционный способ нагрева. Применение плазмотронов дает возможность исключить использование перегревателей кислорода, что значительно’ упрощает аппаратурное оформление процесса. Кроме того, при использовании плазмотрона можно варьировать в широких пределах температурные условия процесса и, следовательно, свойства пигмента.
Отходами производства диоксида титана описанным способом являются сточные воды газоочистки. Они представляют собой 10%-ную хлороводородную кислоту и раствор гипохлорита кальция. Количество этих вод составляет менее 1 т на 1 т готового продукта.
Применение. Пигментный диоксид титана применяется при изготовлении пластических масс, резины, бумаги и т. п. Используется он также в текстильной, радиоэлектронной, металлургической, стекольной и других отраслях промышленности. Однако основная масса диоксида титана (около 60%) используется для пигментирования лакокрасочных материалов, в том числе и водоэмульсионных.
В зависимости от назначения выпускают различные марки пигментного диоксида титана с поверхностной обработкой (модификацией) или без нее. Например, анатазный диоксид титана марки А-1 без поверхностной обработки применяют для покры-
Тий внутри помещений, а диоксид титана марки А-01, обработанный соединениями А1 и Si,—для покрытий кожи. Рутильный диоксид титана марки Р-1 без поверхностной обработки предназначен для «неответственных» наружных покрытий; марки Р-01, обработанный соединениями А1 и Si,— для покрытий средней атмосферостойкости; марки Р-01, обработанный соединениями А1, Si и Zn,— для наружных покрытий с высокой атмосферостой — костью.
Цинковые белила
Свойства. Цинковые белила по химическому составу представляют собой оксид цинка, содержание которого в зависимости от способа получения может составлять от 91 до 99,7%. Основными примесями являются оксиды Cd и РЬ, а также водорастворимые соли. Цвет цинковых белил с максимальным содержанием ZnO — чисто-белый. Примеси придают им желтоватый оттенок. При нагревании белый цвет переходит в желтый, а при охлаждении — вновь восстанавливается.
Цинковые белила растворяются в щелочах и кислотах. На воздухе они поглощают диоксид углерода, образуя карбонат цинка. Реагируют цинковые белила и со свободными жирными кислотами маслосодержащих пленкообразующих веществ, образуя мыла, которые улучшают защитные свойства лакокрасочного покрытия. Срок службы такого покрытия удлиняется также за счет того, что оксид цинка взаимодействует и с низкомолекулярными кислотами — продуктами деструкции пленкообразующего вещества. Способность образовывать цинковые мыла приводит к улучшению смачиваемости пигмента, облегчает диспергирование его в пленкообразующих веществах и способствует образованию пространственных структур в красках, что повышает их стабильность.
Из-за химической активности цинковые белила не могут применяться для пигментирования пленкообразующих веществ с повышенными кислотными числами, поскольку в этом случае может произойти загустевание краски.
Укрывистость цинковых белил 110—140 г/м2, маслоемкость 12—16; показатель преломления 1,95—2,05; плотность 5500 кг/м3.
Форма и размер частиц цинковых белил зависят от способа получения. В свою очередь форма и размер частиц сильно влияют на свойства пигментов. Белила с очень высокой степенью дисперсности обладают повышенной фотохимической активностью, которая обусловливает меление покрытий. Оптимальный размер частиц цинковых белил, применяемых в лакокрасочной промышленности,— 0,4—0,6 мкм. При такой дисперсности меление покрытия проходит в незначительной степени. Игольчатая Форма частиц также способствует повышению атмосферостОйш — сти покрытий.
Свойства цинковых белил во многом зависят от способа их получения. Подробнее об этом будет сказано ниже.
Цинковые белила нетоксичны, однако попадение их в организм человека не безвредно.
Получение. Сырьем для получения цинковых белил служат либо металлический цинк, либо цинксодержащие руды (смитсо — нит) и различные отходы, содержащие до 30—50% оксида цинка. В зависимости от вида исходного сырья различаются и методы получения пигмента.
Получение цинковых белил из металлического цинка сводится к плавлению и испарению цинка с последующим окислением паров кислородом.
Одновременно происходит и окисление паров содержащихся в металлическом цинке примесей Cd и РЬ. Присутствие этих примесей приводит к ухудшению цвета и других свойств пигмента. Поэтому в качестве исходного сырья необходимо использовать металлический цинк очень высокой степени чистоты. Обычно ЭТО Электролитический цинк с содержанием основного вещества от 99,95—99,98%. Иногда используется цинк меньшей степени чистоты с содержанием цинка 98,7%.
Плавление и испарение цинка проводятся либо в муфелях, либо во вращающихся барабанных печах.
Муфель представляет собой полый цилиндр из огнеупорного материала. С одной стороны ои закрыт крышкой, с другой — имеет отверстие для загрузки металлического циика и выхода его паров. Иногда используются муфели другой формы (овальные, с плоским днищем). Муфели устанавливаются в специальные печи в одни или два ряда. Число муфелей в одной печи может достигать 28. Нагревают муфели продуктами сгорания топлива (чаще всего природного газа) с температурой 1300—1500 °С. Топливо сжигают в горелках, расположенных, как правило, с обоих торцов печи. Металлический циик в виде слитков (чушек) вручную загружается в муфели через камеру, расположенную в передней части печи. Эта камера иосит название окислительной («окислительный колодец»), поскольку в ией происходит окисление паров цинка кислородом воздуха, который попадает в камеру за счет подсоса.
Преимуществом муфельных печей является то, что пары циика и оксид цинка не соприкасаются с продуктами сгорания топлива, вследствие чего получаются белила высокой степени чистоты (до 99,0—99,7% ZnO). К недостаткам муфельных печей можно отнести: невозможность регулировать процессы окисления и испарения, ручные операции загрузки циика, низкий тепловой коэффициент полезного действия печи и др.
Вращающаяся барабанная печь (внутренний диаметр барабана 0,8—1,1 м, длина 1,7—2,5 м) изготавливается из стали и футеруется огнеупорным кирпичом. Барабан приводят во вращение с частотой 0,5— 1,0 об/мии специальным приводом. В торцовых крышках барабана имеются отверстия. В одно из иих загружается металлический циик, в другое — поступают продукты сгорания топлива. Пары циика выходят из барабана и попадают в окислительную камеру, расположенную со стороны загрузки циика. В барабане иа поверхности расплавленного циика образуется пленка оксида,.
Которая затрудняет его испарение; при вращении барабана эта пленка разрушается. Кроме того, при вращении расплавленный циик растекается, что увеличивает поверхность (зеркало) испарения. Это в свою очередь обусловливает увеличение производительности печи.
Загрузка цинка в барабан может проводиться вручную или механическим способом с помощью автоматической штаиги и вертикального пульсирующего конвейера. Были также предприняты попытки загружать циик в предварительно расплавленном виде. К недостаткам барабаииой печи следует отнести то, что иа ее футеровке постепенно откладывается плотный слой шлака, состоящий главным образом из оксида циика. Обычно раз в смеиу или сутки стенки печи очищают от этой «шубы» вручную с помощью скребка. Однако этот слой накапливается с течением времени, что приводит к уменьшению рабочего пространства печи и утяжелению ее. В свою очередь это обусловливает повышенный расход электроэнергии на вращение печи. Поэтому через каждые 5—8 сут. (иногда раз в месяц) печь останавливают и очищают с помощью пиевмоинструмента или фрезы. При чистке печи топку и окислительную камеру отводят в стороны. Для этой цели топка делается откатной или подвесной, а окислительная камера—откатиой.
Несмотря иа то что по качеству печные белила несколько уступают муфельным, процесс производства во вращающихся печах является более прогрессивным из-за непрерывности испарения циика и возможности управления процессами окисления, что обусловливает стабильность свойств получаемого продукта; при этом обеспечивается механизация загрузки металлического цинка в печь. Кроме того, значительно снижается расход топлива и улучшаются условия труда обслуживающего персонала.
Образовавшаяся в окислительных камерах суспензия цинковых белил попадает далее в сложную уловительиую систему. Непосредственно после окислительной камеры суспензия поступает в уравнительную (расширительную) камеру, где осаждаются грубодисперсные частицы. Осевшие в бункерах этой камеры частицы цинковых белил накапливаются и периодически выгружаются. Этот промежуточный продукт («камерные белила») может использоваться самостоятельно или добавляться к готовому продукту. В уравнительной камере взвесь белил охлаждается до 800 °С и затем поступает по белилопро — воду в систему фильтров. Белилопровод имеет достаточно большую длину (250—350 м) для обеспечения охлаждения суспензии до 100 °С. По ходу белилопровода могут быть установлены шиберы для подсасывания наружного холодного воздуха. В том случае, когда температура суспензии белил превысит 100 °С, возможно загорание тканей уловительиых фильтров.
Охлажденная взвесь цинковых белил попадает в систему рукавных фильтров с автоматическим встряхиванием. Белила оседают иа фильтрующей перегородке, а воздух проходит через иее и выбрасывается в атмосферу, предварительно пройдя циклон и фильтр для дополнительной очистки от твердых частиц. Белила из указанных фильтров системой шиеков и элеваторов подаются иа автоматизированную упаковочную машину.
Цинковые белила, полученные в барабаииых вращающихся печах, имеют меньшую степень дисперсности, чем белила, полученные в муфельных печах, однако вследствие игольчатой формы частиц печных белил они обладают меньшей фотохимической активностью. Поскольку продукты сгорания топлива соприкасаются в печи с расплавленным цинком и его парами, печные белила имеют несколько худшие показатели по химическому составу, чем муфельные. Так, содержание оксида циика в печных белилах 98—99%, соединений свинца (в пересчете на РЬО) —0,1—0,3%, водорастворимых солей-0,4-0,5%.
Отходами производства цинковых белил, как муфельных, так и печных, являются серый оксид циика и поддувальные шлаки. По химическому составу это в основном оксид циика с примесями металлического циика и других металлов. Эти отходы используются в производстве литопона,
|
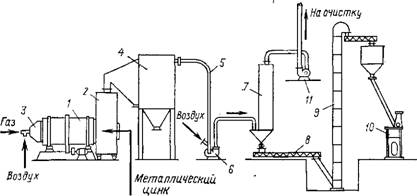
Рис. 5.15. Технологическая схема производства цинковых белил во вращающихся барабанных печах: 1 — вращающаяся барабанная печь; 2 — окислительная камера; 3 — топка; 4 — уравнительная камера; 5—белилопровод; 6 — воздуходувка; 7 — рукавный фильтр; 8 — шнек; 9 — элеватор; 10— упаковочная машииа; 11 — вытяжной вентилятор |
На рис. 5.15 приведена технологическая схема производства цинковых белил во вращающихся барабанных печах.
Металлический цинк загружается в барабан вращающейся печи 1 через окислительную камеру 2. Природный газ сжигается в топке 3 и поступает в рабочее пространство печи. Суспензия оксида цинка из окислительной камеры 2 поступает в уравнительную камеру 4 и затем — в белилопровод 5. Улавливание белил осуществляется в рукавных фильтрах 7. Готовый продукт шнеком 8 и элеватором 9 подается в упаковочную машину 10. Движение- суспензии белил в уловительной системе обеспечивается воздуходувкой 6 и вытяжным вентилятором И.
Получение цинковых белил из цинкосодержащего сырья предусматривает прокаливание сырья в смеси с углем при температуре около 1300 °С. При этом происходит восстановление цинка до металлического, его плавление и испарение. После этого пары цинка окисляются кислородом воздуха, и образовавшийся оксид цинка улавливают по рассмотренной уже выше схеме.
Для восстановления, плавления и испарения цинка в настоящее время используют печи непрерывного действия с движущейся колосниковой решеткой. Поскольку процесс протекает в твердой фазе, исходное сырье и уголь тщательно измельчают, смешивают в необходимой пропорции и затем вновь измельчают. Для снижения пыления, потерь сырья и улучшения условий труда подготовленная шихта брикетируется или гранулируется. Эти брикеты или гранулы подаются на непрерывно движущуюся колосниковую решетку со слоем раскаленного до 1250—1300 °С угля (также брикетированного или гранулированного) в рабочей камере печи, где и происходит восстановление, плавление и испарение цинка. Часть этих паров окисляется в рабочей камере
Кислородом воздуха, который подают через дутьевые короба. Образующаяся суспензия поступает затем в окислительную камеру, где оставшиеся пары цинка доокисляются.
Вместо угля в качестве восстановителя в производстве цинковых белил из цинкосодержащего сырья могут быть использованы продукты сгорания природного газа. Метод этот перспективен, так как позволяет получать белила высокой степени дисперсности с содержанием оксида цинка 98—99%.
Известны и другие способы получения цинковых белил из цинксодержащего сырья, в том числе и гидрометаллургические способы. Последние в перспективе могут найти промышленное применение, поскольку сырьем в них служат отходы цветной металлургии.
Литопон
Литопон представляет собой механическую смесь сульфида цинка и сульфата бария ZnS+BaS04. Если эти компоненты находятся в эквимольном соотношении, литопон называют «нормальным». Литопон же с большим количеством ZnS носит название «высокопроцентного», а с меньшим — «низкопроцентного».
Свойства. Пигментные свойства литопона зависят от содержания в нем ZnS: чем оно выше, тем лучше свойства пигмента. Ниже приводятся свойства нормального литопона: плотность 4300 кг/м3, показатель преломления 2,0; маслоемкость 11—15; укрывистость 110 г/м2; размер частиц 0,5—1,0 мкм. Литопон ще — лочестоек, но не стоек к действию неорганических кислот, которые разлагают его с выделением H2S.
Основным недостатком литопона является его чувствительность к действию света. В присутствии ZnO, влаги и водорастворимых солей при коротковолновом облучении пигмент темнеет в результате восстановления цинка до металлического состояния.
Преимуществом литопона является то, что он содержит значительно меньше цинка, чем цинковые белила, и потому дешевле.
Получение. Сырьем для получения литопона служат цинксо — держащие отходы (обожженные цинковые концентраты, отходы переработки лома цветных металлов, производства цинковых белил и др.), природный сульфат бария (тяжелый шпат, или барит), уголь и серная кислота.
Литопон получают комбинированным осадочно-прокалочным способом. Технологический процесс состоит из трех основных стадий: получение растворов сульфида бария; получение растворов сульфата цинка; осаждение литопона-полуфабриката и переработка его в готовый продукт.
Сульфид бария получают восстановлением природного сульфата бария {тяжелого шпата, или барита) в присутствии угля в трубчатых вращающих — ся печах при 900—1000 "С:
BaS04 + 2С — BaS + 2С02.
Полученный после восстановления плав содержит кроме основного вещества (75—77%) другие соединения бария (ВаСОз, BaSi03 и др.), некоторые количества невосстановленного барита, кремнезем, уголь и др. Плав подвергают мокрому измельчению в шаровой мельнице и выщелачиванию водой, в результате чего BaS переходит в раствор. Механические примесн отделяют от раствора отстаиванием и фильтрованием, а раствор сульфида бария (содержание BaS составляет 140—150 г/л) поступает на осаждение лнтопоиа — полуфабриката.
Для получения раствора сульфата цинка используется цинксодержащее сырье, которое включает соединения цинка (в пересчете на металлический цинк) до 70—80%, а также примеси (Fe, Al, Mn, Cd, №, Си н др.). Это сырье обрабатывается раствором серной кислоты с концентрацией 180— 200 г/л. При этом в раствор переходят сульфаты Zn, Fe, Mn, Cd, №, Си. Если в сырье присутствует свинец, он образует сульфат свинца, нерастворимый в растворе серной кислоты и остающийся в осадке. Оксиды олова не взаимодействуют с серной кислотой. В осадке остаются и другие нерастворимые прнмеси сырья. Этот осадок отфильтровывают и направляют на заводы цветной металлургии.
Осветленный раствор сульфата цинка освобождают далее от примесей других металлов. Примеси железа выводят из раствора в виде осадка Fe(OH)3. Для этого железо предварительно переводят из двух — в трехвалентное состояние. В качестве окислителей могут использоваться кислород воздуха, перманганат калия, белильная известь, гипохлорит натрия. Чаще всего применяют гипохлорит натрия, который получают из белильной извести непосредственно в цехе.
Одновременно с удалением железа раствор сульфата цинка очищается и от соединений марганца. Выпадающий при этом осадок, являющийся отходом производства, отфильтровывают.
От примесей солей Cd, Ni и Си раствор сульфата цинка очищают восстановлением их до металлов. Для этого к раствору добавляют цинковую пыль. Образовавшийся осадок отфильтровывают и направляют на переработку на заводы цветной металлургии. Очищенный же раствор подвергают контрольной очистке от следов железа и марганца.
К готовому раствору цинкового купороса (содержание ZnSO.» 300— 350 г/л) добавляют небольшое количество сульфата кобальта, который способствует образованию светостойкого литопона.
Кроме описанного способа получения раствора цинкового купороса, известен еще способ его получения хлорирующим обжигом. В качестве цннк — содержащего сырья в этом случае используются колчеданные огарки, получающиеся при производстве серной кислоты. Эти огарки, тщательно измельченные и смешанные с хлоридом натрия, подвергают обжигу. В результате образуется плав, содержащий сульфат цинка, хлорид цинка и сульфат натрия. Плав выщелачивают водой и освобождают от примесей сульфата натрия и тяжелых металлов. Полученный раствор, содержащий ZnS04 и ZnCl2, используют для получения литопона с высоким содержанием ZnS. Выделенный прн очистке раствора сульфат натрня используют для получения высококачественного наполнителя — бланфикса, по составу представляющего собой сульфат бария. Другим осадителем является хлорид бария, образующийся как побочный продукт при осаждении «высокопроцентного» литопона. В нашей стране метод хлорирующего обжига не нашел применения, однако он представляет интерес, так как при его применении обеспечивается комплексное использование сырьи.
Литопон-полуфабрикат получают при сливании двух исходных растворов BaS и ZnSO*. При этом протекает обменная реакция:
BaS + ZnS04 — ZnS + BaS04.
Кроме этой основной реакции протекают еще и побочные, приводящие к. получению ZnO.
Для осаждения «высокопроцентного» лнтопона чаще всего к раствору цинкового купороса добавляют хлорид цинка:
ZnS04 + 2 BaS + ZnCI2 — 2ZnS + BaS04 + BaCI2.
«Низкопроцентный» литопон получают добавлением к цинковому купоросу сульфата натрия:
ZnS04 + Na2S04 + 2BaS — ZnS + 2BaS04 + Na2S.
Свойства литопона в значительной степени зависят от величины рН среды при осаждении полуфабриката. Так, при рН<5 (при избытке цинкового купороса) получается осадок, который плохо осаждается и плохо фильтруется, а при прокаливании спекается с образованием пигмента невысокого качества. Такой продукт Характеризуется повышенным содержанием оксида цинка. При рН 7,5—8,3 (при небольшом избытке сульфида бария) образуется хорошо отстаивающийся и фильтрующийся продукт, который после прокаливания переходит в пигмент, содержащий десятые доли процента оксида — цинка.
Осадок литопона-полуфабриката после высушивания подвергается термической обработке для перевода сульфида цинка из кубической в более светостойкую гексагональную кристаллическую сиигонию. Этому процессу способствуют примеси солей кобальта, введенные до осаждения в цинковый купорос. В результате термообработки литопон приобретает пигментные свойства. Температура термической обработки, проводимой в трубчатых муфельных печах непрерывного действия, составляет 650—700 °С. В таких печах литопон не соприкасается с продуктами сгорания топлива, что предотвращает его загрязнение и окисление сульфида цинка в оксид.
После прокаливания литопон быстро охлаждается водой (гашение), поскольку при медленном охлаждении он может вновь перейти в кубическую сингоиию. Далее продукт подвергают измельчению мокрым способом с классификацией частиц по размерам. Высушенный после этого литопон измельчают сухим способом и упаковывают.
Применение. Литопон применяют для получения масляных и Эмалевых красок для внутренних работ, водоэмульсионных красок, а также в производстве резины, пластмасс, клеенки, линолеума и др.
Свинцовые белила
Существует несколько типов свинцовых белил: карбонатные свинцовые белила 2РЬС03-РЬ(0Н)2, белила Паттисона РЬСЬХ ХРЬ(ОН)2, суперайт 2PbS04-Pb(0H)2 и др. Наибольшее распространение имеют карбонатные свинцовые белила, которые и будут рассмотрены ниже.
Свойства белил зависят от их химического состава. Так, при приближении состава к среднему карбонату свинца РЬСОз пигментные свойства ухудшаются, а сам средний карбонат свинца вообще не обладает пигментными свойствами.
Плотность свинцовых белил 6400—6800 кг/м3; коэффициент преломления 1,94—2,09, укрывистость 160—200 г/м2, маслоем — кость 9—12; размер частиц 0,5—1,25 мкм; интенсивность невысокая.
Свинцовые белила растворяются в азотной и концентрированной уксусной кислотах, при нагревании — в разбавленной хлороводородной кислоте. Серная и концентрированная хлороводородная кислоты разлагают белила; растворяются свинцовые белила также в растворах щелочей.
Свинцовые белила легко взаимодействуют с жирными кислотами, образуя свинцовые мыла. Именно этим обстоятельством объясняется высокая атмосферостойкость покрытий, изготовленных на основе маслосодержащих пленкообразующих веществ, пигментированных свинцовыми белилами.
В присутствии серы или ее соединений свинцовые белила темнеют из-за образования черного сульфида свинца. По этой причине белила нельзя смешивать с пигментами, содержащими сульфиды металлов (литопон, желтый и красный кадмий, ультрамарин и др.), а также применять для изготовления покрытий, эксплуатирующихся в промышленных районах, где в воздухе содержится значительное количество сернистых газов.
Свинцовые белила высокотоксичны. Попадание их в пищеварительный тракт представляет большую опасность, так как они легко растворяются в желудочном соке. Во избежание отравлений персонала технологический процесс получения белил должен быть максимально механизирован, а аппаратура тщательно герметизирована.
Получение. Методы получения свинцовых белил могут быть «сухими» и «мокрыми». Сухие методы заключаются в окислении и карбонизации металлического свинца в присутствии уксусной кислоты. В настоящее время эти методы не применяются в промышленности из-за малой производительности и повышенной опасности свинцового отравления. Мокрые методы, или методы осаждения, заключаются в карбонизации растворов различных солей свинца. При этом в качестве сырья используют глет, уксусную кислоту и диоксид углерода.
Из глета растворением в разбавленной уксусной кислоте готовят при 50—80 °С раствор основного ацетата свинца:
ЗРЬО + 2СН3СООН + Н20 — РЬ(СН3СОО)2-2РЬ(ОН)2.
Из полученного раствора удаляют отстаиванием механические примеси (непрореагировавший РЬО, металлический РЬ), а очищенный раствор карбонизируют пропусканием через него диоксида углерода:
7[РЬ(СН3СОО)2-2РЬ(ОН)2] + 8,4 С02- — 7[Pb(CH3COO)2-0,2Pb(OH)2] + 4,2[2PbC03-РЬ(ОН)2] + + 8,4 Н20.
Свойства свинцовых белил в значительной степени зависят от условий осаждения (карбонизации), а именно от концентрации исходного раствора, исходной и конечной величины рН, расхода СОг, а также от температуры. Белила хорошего качества можно получить только в том случае, когда к концу карбонизации рН раствора составит не менее 6,5—7,0.
Полученную в результате карбонизации суспензию белил уплотняют. Осветленный маточный раствор снова используют на начальных стадиях производства с периодической очисткой, главным образом для удаления железа.
Поскольку свинцовые белила токсичны, их выпускают, как правило, не в сухом виде, а в виде водных паст или паст в пленкообразующих веществах. Это позволяет избежать проведения операций сушки и измельчения пигмента, которые связаны со значительным пылением (ПДК свинцовых белил в воздухе рабочей зоны составляет 0,01 мг/м3).
Для получения пасты белил в пленкообразующем веществе пульпу после отделения маточного раствора смешивают при нагревании с льняным маслом или олифой. Пигмент избирательно смачивается последними, в результате чего выделяется из пульпы в виде пасты. Отработанный раствор ацетата свинца сливается и направляется вновь на производство.
Кроме описанного выше существует еще технологический процесс получения свинцовых белил, при котором операция приготовления раствора ацетата свинца отсутствует. Карбонизацию же проводят в 10%-ной суспензии глета в присутствии незначительного количества уксусной кислоты при интенсивном перемешивании и нагревании. Этот способ позволяет значительно сократить продолжительность технологического процесса и почти полностью исключить образование сточных вод.
Известен также электрохимический метод получения свинцовых белил. Однако вследствие значительного расхода электроэнергии, сложности и ряда других причин этот метод не нашел пока практического применения в отечественной промышленности.
Применение. Высокая токсичность пигмента ограничивает масштабы его производства и области применения. В основном он используется для особо ответственных окрасочных работ, например в судостроении. Применяют свинцовые белила и как исходный продукт для получения других свинецсодержащих соединений.
Прочие белые пигменты
Промышленность выпускает кроме рассмотренных выше четырех основных белых пигментов и другие: титанаты магния, бария и цинка; смешанные титанокальциевые пигменты; сурьмяные Sb203, висмутовые Bi(0H)2N03 и циркониевые Zr02 белила; алюминат цинка Zn0-Al203; фосфаты цинка и титана; сульфид цинка и др.
 1 ноября, 2012
1 ноября, 2012  admin
admin 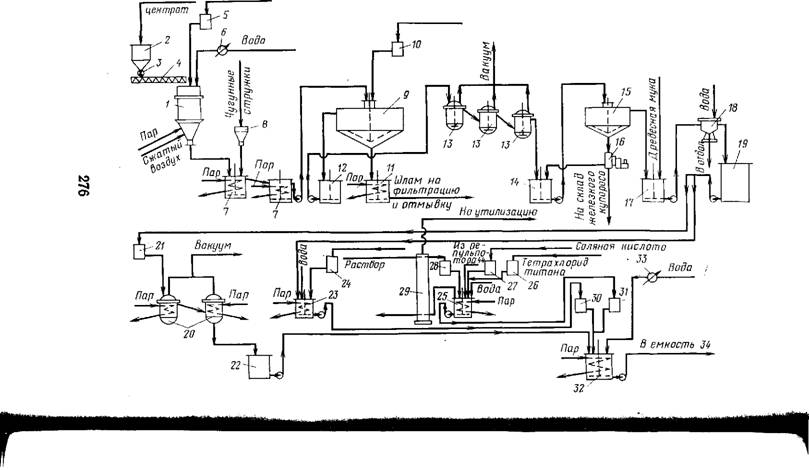
 Опубликовано в рубрике
Опубликовано в рубрике 