Согласно А. И. Рабинерсону и Г. И. Фуксу, структуры, образующиеся в высокодисперсных системах, можно классифицировать по их плотности (числу связей в единице объема). По этой классификации структуры делят на пространственные (рыхлые) и компактные. Первые структуры характерны для дисперсных систем с анизодиаметрическими частицами, вторые структуры часто возникают в системах с изодиаметрическими частицами. Первые структуры при старении и действии коагулирующих факторов могут переходить во вторые.
В последнее время наибольшее распространение получила классификация структур, предложенная П. А. Ребиндером.
Согласно П. А. Ребиндеру, структуры в коллоидных и микрогетерогенных системах можно разделить на коагуляционные (тик — сотропно-обратимые) и конденсационно-кристаллизационные (необратимо-разрушающиеся).
Коагуляционные структуры. К ним относятся структуры, обычно возникающие в результате понижения аі^зегативной устойчивости дисперсных систем. При истинной коагуляции, котда частицы полностью теряют фактор устойчивости (двойной электрический слой, сольватную оболочку и т. д.), они слипаются друг с другом, образуя компактные агрегаты. Достигнув определенного размера, эти агрегаты образуют плотный коагулят (или коагулюм). Если же происходит неполная астабилизация системы, то фактор устойчивости будет снят только с некоторых участков поверхности частиц, да и то не полностью, и в результате этого частицы, слипаясь по таким местам, образуют пространственную сетку, в петлях которой находится дисперсионная среда. Происходит, как принято говорить, гелеобразование [24] или образование лиогеля. Вид струк
туры, получаемой в результате гелеобразования, схематически изображен на рис. X, 1.
При достаточно сильной астабилизации прослойки дисперсионной среды, находящиеся между частицами, в местах их соприкосновения полностью вытесняются, и благодаря этому осуществляется непосредственный контакт частиц друг с другом. Это отвечает образованию наиболее прочных, но одновременно и наиболее хрупких коагуляционных структур. Однако весьма часто при более слабой астабилизации-в месте контакта между частицами
Остаются достаточно толстые слои дисперсионной среды. Иначе говоря, между частицами наблюдается дальнодействие, причины которого рассмотрены в гл. IX. Наличие тонкой жидкостной прослойки между частицами обусловливает меньшую прочность структуры, но зато придает ей пластичность, а в некоторых случаях и эластичность. Чем толще прослойка среды между частицами, тем меньше сказывается действие молекулярных сил, обусловливающих сцепление частиц, тем менее прочна структура и тем жидкообразней система.
На гелеобразование может влиять ряд факторов. * Концентрация дисперсной фазы сильно сказывается на скорости образования геля и его прочности, так как с повышением численной концентрации число контактов, приходящихся на единицу объема системы, и скорость установления контактов возрастают.
Уменьшение размера частиц при постоянной концентрации дисперсной фазы также способствует гелеобразованию. Очень большое значение для гелеобразования имеет форма частиц. Образование лиогеля облегчается, если частицы анизодиамётричны и имеют концы, углы и ребра. В этих местах двойныё электрические слои или сольватиые оболочки наименее развиты, так что слипание астабилизован — ных частиц происходит именно по этим участкам. Кроме того, для образования структуры требуется гораздо меньше дисперсной фазы, представляющей собой палочкообразные или пластинчатые частицы, чем дисперсной фазы, состоящей из сферических частиц.
|
Рис. X, 1. Строение пространственных структур, образующихся в лиозоле При астабилизации: 1—частицы дисперсной фазы; 2—участки поверхности частиц, лишившиеся фактора устойчивости после астабилизации; 3—участки поверхности частнц, сохранившие фактор устойчивости, 4—петли структуры, заполненные дисперсионной средой. |
На скорость образования и свойства полученного геля весьма сильно влияет температура. Время образования геля по тем же причинам, что и время коагуляции, при повышении температуры уменьшается. Однако с повышением температуры в результате увеличения интенсивности броуновского движения лиофобные гели — могут переходить в структурированную жидкость, а затем, при еще
более высоких температурах, становиться даже неструктурированными жидкостями.
— Механическое воздействие, например перемешивание, обычно препятствует образованию геля. Однако в некоторых случаях время образования геля из агрегативно неустойчивых золей с сильно анизодиаметрическими частицами (например, золя V2O5) можно значительно сократить, если сосуд, содержащий золь, медленно вращать. Это явление, открытое Фрейндлихом, получило название реопексии (греч. — образование геля при движении). Причину реопексии некоторые исследователи видят в том, что параллельная ориентация вытянутых частиц при течении благоприятствует установлению Между ними контактов и, следовательно, способствует образованию геля. Другие исследователи считают, что причиной реопексии является возникновение при движении системы слабой турбулентности, ускоряющей установление контакта между частицами.
Специфическим свойством коагуляционных структур является Тиксотропия (от греч. — тиксо — прикосновение, тропе — поворот, изменение) — способность структур после их разрушения в результате какого-нибудь механического воздействия самопроизвольно восстанавливаться во времени. Иначе говоря, тиксотропия представляет собой способность к изотермическому обратимому превращению золя в гель. Сущность тиксотропии заключается в том, что связи, которые были разрушены при механическом воздействии, восстанавливаются в результате случайных удачных соударений частиц, находящихся в броуновском движении. Такое постепенное восстановление структуры и, следовательно, нарастание ее прочности происходит не только, когда система находится в покое, но и при течении системы со скоростью меньшей той, которая обусловила данную степень разрушения первоначальной структуры. Существенно, что при переходе от одного режима течения к другому с большей скоростью обычно, но не всегда, наблюдается дополнительное разрушение структуры, что понижает эффективную вязкость и прочность структуры. Наоборот, при переходе от установившегося режима течения к течению с меньшей скоростью, как правило, происходит некоторое восстановление структуры и, соответственно, эффективная вязкость и прочность системы увеличиваются. х
Явление тиксотропии часто встречается в природе. Тиксотроп — ные свойства проявляют некоторые грунты («плывуны»). Для протоплазмы в клетках живых организмов также характерна тиксотропия. Гели миозина обладают сильно выраженными тиксотроп — ными свойствами, что свидетельствует о роли тиксотропии в работе мускулов.
Способность дисперсных систем проявлять тиксотропию часто используют в технике. Например, при бурении нефтяных скважин глинистые растворы прокачивают через скважину — промывают ее для удаления из нее частиц измельченной выбуренной горной породы. Благодаря тиксотропным свойствам этих растворов предупреждается оседание частиц породы в скважине и заклинивание этим самым бурового инструмента при временной остановке бурения.
Другим примером тиксотропних систем, имеющих практическое применение, могут служить обычные масляные краски, представляющие собой взвесь минеральных пигментов в олифе. Благодаря тиксотропным свойствам красок их можно наносить на вертикальные поверхности в виде жидкости после их механического перемешивания, при этом нанесенная краска не стекает в результате быстро наступающего структурирования. Для повышения тиксо — тропных свойств в краски иногда вводят специальные добавки, например полиамиды, бентониты. Характерные реологические свойства, включая тиксотропию таких красок, в том числе и типографских, исследовали А. А. Трапезников с сотр. с помощью разработанных ими методов определения предела прочности и вязкости в широком интервале скоростей деформации. Было показано, что тиксотропия может выражаться как в разрушении и образовании сплошной сетки (прочностная тиксотропия), так и в разрушении и восстановлении агрегатов частиц (вязкостная4 тиксотропия).
Явлением, противоположным тиксотропия, является дилатансия, проявляющаяся в небольшом сопротивлении системы при низком напряжении сдвига и высоком сопротивлении при большом сдвиговом усилии. Дилатансия характерна для очень концентрированных агрегативно устойчивых суспензий, у которых нет постоянного контакта между частицами. Рейнольде, открывший это явление в 1885 г., объяснил его тем, что движение системы возможно только при малых напряжениях сдвига и малом изменении относительного положения частиц При больших напряжениях сдвига происходит местное сближение частиц и соответственно уменьшается свободное пространство для течения, в результате чего движение жидкости сильно затрудняется ули даже приостанавливается.
К тиксотропным системам близко примыкают тактоиды и слои Шиллера. Под тактоидамн подразумевают дисперсии, имеющие участки с хорошо выраженной периодичностью в расположении параллельно ориентированных относительно друг друга анизоднаметрнческих частиц. Явление анизотропной ориентации частиц было обнаружено на золях Fe(OH)3, на ряде других неорганических к органических дисперсий, а также на биоколлоидах — колониях вирусов и бактерий. Причиной образования анизотропных областей в таких системах является равновесие между молекулярными силами притяжения и электростатическими силами отталкивания, действующими между частицами, являющимися обычно диполями.
Слои Шиллера представляют собой коллоидные осадки, состоящие из пластинчатых частиц, которые расположены в горизонтальных плоскостях, обычно отделенных друг от друга расстояниями в несколько тысяч ангстрем. Характерное строение слоев "Шиллера определяется соотношением силы электростатического отталкивания заряженных частиц и силы тяжести Структуры, близкие к слоям Шиллера, могут возникать под действием и других внешних полей —• центробежных, электрических и магнитных.
Доказательством того, что периодические структуры образуются в результате электростатического отталкивания при перекрытии ионных атмосфер, служит закономерное уменьшение расстояний между соседними частицами при увеличении концентрации электролита. Количественная теория периодических коллоидных структур была развита И. Ф. Ефремовым и С. В. Нерпиным и в некоторых отношениях уточнена С. С. Духиным и др. При этом каждая частица рассматривается как фиксированная в потенциальной яме, образуемой совокупным действием ее соседей.
Известным аналогом периодических коллоидных структур может служить кристалл монтимориллокитовой глины при его вну — трикристаллическом набухании в водных растворах. При внутри — кристаллическом набухании кристаллические плоскости толщиной каждая около 10 А раздвигаются и между ними образуются жидкие прослойки. Условием набухания является насыщение кристалла ионами Н+, Li+ или Na+. При очень низких концентрациях внутрикристаллические прослойки достигают толщины в 300 А. Одинаковость всех прослоек сохраняет периодическую структуру системы и позволяет по дифракции рентгеновских лучей измерять толщины прослоек. Полученные данные согласуются с теорией ДЛФО. Такой набухший кристалл служит хорошей моделью других периодических структур. С помощью этой модели можно также, как показал О. Г. Усьяров, обнаружить существование ближней и дальней потенциальной ям, энергетического барьера и влияние валентности ионов на закономерности набухания.
Если концентрация достаточно монодисперсной коллоидной системы, защищенной от коагуляции в ближней потенциальной яме высоким барьером, становится высокой, то часто в результате сближения частицы образуют квазикристаллическую решетку, в которой они расположены на равных расстояниях друг от друга. При высокой дисперсности системы можно заметить (как частицы совершают колебательное броуновское движение около своих положений равновесия.
Периодические коллоидные структуры образуют многие вирусы, бактерии, монодисперсные золи металлов, золи пятиокиси ванадия, латексы.
Образование периодических структур означает, что расстояние каждой частицы от соседних соответствует дальней потенциальной йме в тех случаях, когда система граничит со свободной дисперсионной средой и, следовательно, не подвергается внешнему давлению. В этом случае расстояния между частицами уменьшаются при добавлении электролита и увеличиваются при разбавлении системы.
Чаще встречаются периодические коллоидные структуры, занимающие весь объем жидкой среды и ограниченные со всех сторон стенками или поверхностью раздела с воздухом В этом случае потенциальная яма, в которой удерживается каждая частица, образуется в результате сложения сил отталкивания со стороны соседних частиц. Поэтому соответственные расстояния могут быть меньше, чем абсциссы дальних потенциальных ям, — система, как принято говорить, находится в «стенсненном» состоянии. При еще большем «сжатии», когда средние расстояния между соседними частицами будут меньше абсцисс потенциальных барьеров, произойдет нарушение равновесия, часть частиц слипнется при попадании в ближние потенциальные ямы, оставшиеся же частицы смогут сохранить периодическое расположение.
Однако и до такого «сжатия» периодическая коллоидная структура обычно находится в состоянии только временного равновесия. Время от времени то одна, то другая частица перескакивает из положения равновесия в узле квазикристаллической решетки в ближайшую потенциальную яму. Возникающие дефекты квазикристаллической решетки множатся необратимо и не могут «залечиваться». Таким образом, в отличие от кристаллов, периодические коллоидные структуры находятся часто ие в состоянии термодинамического равновесия, а устойчивы кинетически. Иными словами, их существование обусловливается медленностью перехода в равновесное состояние
Однако принципиально нельзя исключать возможность равновесных периодических структур, если ближний минимум отсутствует Возможно, что к этой категории принадлежит ряд вирусов, как, например, вирус табачной мозаики.
Современное состояние проблемы, равно как и собственные исследования периодических коллоидных структур, изложены в монографии И. Ф. Ефремова [25].
Системы с коагуляционными структурами обладают, как правило, небольшой прочностью, известной пластичностью, а также некоторой эластичностью. Эластические свойства коагуляционных структур, согласно П. А. Ребиндеру, можно объяснить изменением энтропии системы в результате переориентации образующих систему структурных элементов, сопутствующей изменению ее формы. Такими структурными элементами служат отдельные коллоидные частицы (в отличие от высокомолекулярных соединений, где эластическая деформация связана с изменением взаимной ориентации звеньев молекулярных цепей). Системы с коагуляционными структурами проявляют также ползучесть, т. е. способность при лечении к медленному развитию значительных остаточных деформаций практически без заметного разрушения пространственной сетки. Ползучесть системы определяется высокой, хотя и вполне доступной~измерению вязкостью в области весьма малых скоростей течения. Только при больших скоростях течения в таких системах происходит значительное разрушение структуры, так как связи между частицами не успевают восстанавливаться и скорость разрушения становится больше скорости восстановления.
Системам с коагуляционными структурами очень часто присуще явление „Синерезиса. Под синерезисом понимают самопроизвольное уменьшение размеров геля с одновременным выделением из него дисперсионной среды, содержавшейся в петлях геля. Причина синерезиса заключается в том, что при гелеобразовании между элементами структуры образуется сравнительно малое число контактов, не отвечающее предельно уплотненному состоянию структуры. Затем в результате перегруппировки частиц, обусловленной их тепловым движением, число этих контактов увеличивается, что неизбежно приводит к сжатию геля и к выпрессовыва — нию из него дисперсионной среды. Явление синерезиса схематически представлено на рис. X, 2. Как можно видеть, число палочкообразных частиц, образующих гель, остается тем же самым, но число точек соприкосновения их после синерезиса резко увеличивается.
Синерезису благоприятствуют все факторы, способствующие коагуляции, а именно, увеличение концентрации электролита, повышение температуры, введение в систему десольватирующих агентов и т. д. Синерезису способствует также гибкость и подвижность элементов коагуляционной структуры. Поэтому особенно значи
тельный синерезис наблюдается у студней высокомолекулярных веществ, состоящих из гибких макромолекул.
Системы с коагулядионной структурой, из которых высушиванием удалена дисперсионная среда, способны в той или иной степени поглощать эту среду при контакте с ней. Поглощение среды сухим гелем — к, серогелем (от греч. ксерос — сухой) может обусловливаться как простым капиллярным всасыванием, так и раздвижением элементов структуры геля вследствие возникновения расклинивающего давления и заполнения образовавшихся промежутков средой. В последнем случае говорят о набухании«
А 5
Рис. X, 2. Схематическое изображение сннерезиса: а —система до синерезиса, б —система после сииерезиса.
Ксерогеля. Совершенно очевидно, что набухание является процессом обратным синерезису. Однако вследствие того, что при образовании пространственной структуры лиофобных систем места контакта закрепляются обычно довольно прочно, лиофобные ксеро — гели набухают сравнительно незначительно. Наоборот, студни высокомолекулярных веществ могут очень сильно набухать. Поглощение среды сухим гелем или предельно прочной коагуляционной структурой приводит к пластификации, т. е. к резкому понижению прочности, сопровождающемуся, однако, возрастанием пластических и эластических свойств данного тела.
Более подробно явления синерезиса и набухания рассмотрены в гл. XIV.
Кондеисациоино-кристаллизациониые структуры. К этому типу принадлежат структуры, у которых связи между частицами образованы за счет химических сил. Эти структуры возникают либо в результате образования прочных химических связей между частицами (конденсационные структуры), либо вследствие сращивания кристалликов в процессе выкристаллизовывания новой фазы (кристаллизационные структуры).
Структуры с таким характером связей между частицами не могут проявлять тиксотропии, пластичности и эластичности, а должны, наоборот, проявлять упруго-хрупкие свойства. Прочность их обычно значительно выше прочности коагуляционных структур. Совершенно очевидно, что системы с такого рода
Структурами не могут в сколько-нибудь заметной степени сине — резировать или набухать.
Типичный конденсационной структурой является гель кремневой кислоты. Кристаллизационное структурообразование имеет существенное значение для твердения минеральных вяжущих средств в строительных материалах на основе цементов, гипса или извести.
На образование связей, а следовательно, и на свойствах этих структур может сильно сказываться присутствие в системе модифицирующих добавок поверхностно-активных веществ, изменяющих форму и размеры образующихся кристаллов, а также условия их срастания.
Необходимо хотя бы кратко, остановиться на дисперсных системах, в которых структура в обычном смысле этого слова отсутствует, но у которых наблюдаются некоторые общие свойства с настоящими структурированными системами. К таким системам относятся, например, высркоконцентрированные стабилизованные суспензии (пасты), а также осадки, образующиеся в результате седиментации.
В агрегативно устойчивых суспензиях, частицы которых достаточно сольва — тированы, при предельно высокой концентрации дисперсной фазы (когда частицы разделены весьма тонкой пленкой жидкости) почти вся дисперсионйая среда может быть сольватно связана с дисперсной фазой. В результате этого вязкость систем обычно весьма высока
Механическая прочность подобных систем может резко возрастать при введении в них поверхностно-активных веществ, молекулы которых, адсорби — руясь и ориентируясь на поверхности частиц, способствуют, согласно Б В. Де — рягину, развитию и взаимодействию граничных сольватных слоев Мїханические свойства концентрированной суспензии можно повысить также введением в нее высокомолекулярных веществ, обычно адсорбирующихся на поверхности частиц и вызывающих застудневание жидкой среды При этом застудеванию способствуют частицы дисперсной фазы, играющие роль «активного наполнителя».
Механические свойства концентрированных систем, в которых частицы дисперсной фазы имеют сольватные оболочки, все же обычно значительно ниже механических свойств систем с коагуляционными и конденсационно-кристаллиза — ционными структурами. Кроме того, благодаря образованию сольватных оболочек у частиц система пластифицируется, понижается ее прочность и у нее появляются пластично-вязкие свойства, тогда как при возникновении пространственных структур повышаются упруго-хрупкие свойства системы.
Рассмотрим два возможных случая образования осадков в результате оседания частиц седиментационно неустойчивых суспензий.
1.Оседание агрегативно неустойчивых суспензий происходит быстро из-за образования агрегатов; осевший осадок занимает большой объему так как частицы сохраняют то случайное — взаимное расположение, в котором они оказались при соприкосновении. Совершенно очевидно, что подобные системы, образующиеся при оседании суспензий, довольно близки по строению и свойствам к рассмотренным выше коагуляционным структурам.
2. Оседание агрегат и. в но устойчивых суспензий, если частицы достаточно малы, происходит медленно и частицы, осевшие на дно сосуда, остаются разделенными друг от друга под влиянием тех же сил, которые препятствуют их агрегации. Вследствие этого частицы, скользя друг по другу, занимают положение, отвечающее минимальной потенциальной энергии н характеризующееся максимальной компактностью укладки. Полученный таким образом осадок, если он достаточно плотен, может обладать всеми механическими свой» ствами, присущими концентрированным суспензиям.
Из сказанного следует, что объем осадка может служить показателем степени агрегатнвной устойчивости седиментнрующей суспензии. Это можно видеть
из следующего примера. Если 40 г порошка кварца с диаметром частиц от 1 до
5 мкм размешать в 25 мл воды, то образуется агрегативно устойчивая суспензия, устойчивость которой обусловлена возникновением вокруг частиц гндратных оболочек или двойных электрических слоев за счет ионизации кремневой кислоты, образовавшейся прн взаимодействии Si02 н Н20. В этой суспензии за
6 ч оседания образуется всего 8,5 мм осадка, содержащего, однако, 54 объемн % кварца.
Если то же количество порошка кварца распределить в том же объеме четыреххлорнстого углерода, не способного образовывать на частицах сольват — ные оболочки н исключающего возможность возникновения двойного электрического слоя, то получается агрегатнвно. неустойчивая суспензия В этой суспензии уже за 15 мнн оседання слой осадка достигает предельной толщины в 53 мм, причем он состоит всего нз 7 объемн. % кварца.
Наконец, если 40 г кварцевого порошка поместить в 25 мл четыреххлорнстого углерода, в который предварительно было введено небольшое количество олеиновой кислоты, то при оседаннн суспензнн снова образуется малое количество осадка большой плотности. Это следует объяснить тем, что молекулы олеиновой кислоты, адсорбнруясь на кварце полярными группами, гндрофобизуют поверхность частнц, делают их агрегатнвно устойчивыми в четыреххлористом углероде н тем самым способствуют компактной укладке частнц в осадке.
 1 ноября, 2012
1 ноября, 2012  admin
admin 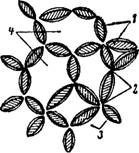
 Опубликовано в рубрике
Опубликовано в рубрике 