|
|
|
Рис. IV, 2. Изотерма адсорбции в логарифмических координатах- |
Взаимодействие молекул адсорбтива с поверхностью адсорбента при физической адсорбции может обусловливаться различными причинами. Рассмотрим кратко эти причины, так как Подробное рассмотрение адсорбционных сил выходит за рамки коллоидной химии и сведения о них можно найти в специальных монографиях, посвященных адсорбции, или в фундаментальных курсах физической химии [4].
Наиболее простым случаем является адсорбция неполярной молекулы, также неполярным адсорбентом, когда действуют только дисперсионные силы притяжения и борновские силы отталкивания.
Потенциал 0, определяющий взаимодействие одной молекулы адсорбента с одним атомом неполярного адсорбтива, приближенно можно выразить, например, уравнением Леннарда — Джонса:
6 — — Сг_6 + Br~12 (IV, 4)
Где г — расстояние между центрами частиц; С — константа дисперсионного притяжения, В — константа, характеризующая энергию сил отталкивания.
Константа С для многоэлектронных атомов может быть выражена через электрические и магнитные свойства взаимодействующих молекул с помощью различных уравнений, основанных иа квантовомеханических представлениях, которые здесь не будут рассматриваться. Существенно, что, как это показывается в физической химии, не только энергия дисперсионных, но и индукционных, и ориентационных сил притяжения зависят от расстояния г одинаковым образом, а именно — обратно пропорционально шестой степени расстояния.
Выражение Вг~12 введено в уравнение (IV,4) как удачное эмпирическое приближение. Совершенно очевидно, что на сравнительно далеких расстояниях должны превалировать силы притяжения, а на весьма малых расстояниях — силы отталкивания. Ясно также, что на определенном расстоянии эти силы должны быть равны, так как это соответствует минимуму свободной энергии системы.
Однако поскольку при адсорбции дисперсионные силы действуют одновременно между каждой неполярной частицей, например атомами аргона, и всеми близлежащими атомами адсорбента, суммарный потенциал Ф адсорбционных сил приближенно может быть получен суммированием потенциала парных взаимодействий атома аргона с каждым отдельным атомом адсорбента по всем его атомам с учетом потенциала сил отталкивания:
Ф=Хе*=-сЕгг6+я Хт12 (IV,5)
В этом уравнении — С X Т6 — суммарный потенциал дисперсионных сил притяжения В Z Т12 — суммарный потенциал сил отталкивания, а г і— расстояния от центра атома аргона до центров различных атомов адсорбента. Поскольку энергия взаимодейСтвия частиц быстро убывает с расстоянием, то практически достаточно произвести суммирование по 100—200 ближайшим атомам адсорбента. Существенно, что при адсорбции сложных неполярных молекул потенциальную энергию взаимодействия можно приближенно вычислить как сумму потенциальных энергий адсорбции ее звеньев (силовых центров).
Если адсорбент состоит не из атомов, а из ионов, то к действию дисперсионных сил добавляется действие индукционных сил притяжения диполя, индуцированного в молекуле адсорбтива электрическим полем, создаваемым ионами решетки адсорбента. При этом доля индукционных сил в адсорбционном взаимодействии пропорциональна поляризуемости молекулы адсорбтива и квадрату напряженности электростатического поля над поверхностью адсорбента.
Если на неполярном адсорбенте адсорбируются полярные молекулы адсорбтива, то постоянные диполи молекул адсорбтива поляризуют атомы адсорбента, т. е. индуцируют в них электрические моменты. Вследствие этого возникает индукционное притяжение, которое добавляется к дисперсионному. Индукционное взаимодействие обычно невелико и в зависимости от диполя молекулы адсорбтива и поляризуемости адсорбента может достигать не более нескольких ккал/моль.
Наконец, если полярные молекулы адсорбируются на адсорбенте, имеющем на поверхности ионы или диполи, то возникает взаимодействие ионов или диполей адсорбтива с электростатическим полем адсорбента. При этом молекулы адсорбтива могут ориентироваться в электростатическом поле адсорбента, т. е. происходит ориентационное кулоновское взаимодействие.
Следует заметить, что если суммарное дисперсионное >взаимо — действие молекулы адсорбтива с адсорбентом всегда больше взаимодействия ее с одним активным центром адсорбента, то суммарное электростатическое взаимодействие молекулы адсорбтива может быть и меньше ее электростатического взаимодействия с одним центром адсорбента. Такое явление можно объяснить тем, что отрицательный полюс диполя молекулы адсорбтива, притягиваемый катионом решетки адсорбента, одновременно испытывает отталкивание со стороны соседних с этим катионом анионов, образующих вместе с катионами знакопеременную поверхность адсорбента.
Обычно энергии индукционного и ориентационного взаимодействия гораздо меньше энергии дисперсионного взаимодействия, и поэтому часто принимают, что энергия межмолекулярного притяжения определяется энергией дисперсионного притяжения.
Причиной адсорбции, близкой к физической, может быть также образование водородной связи. В частности, такая связь везникает при адсорбции на адсорбентах, содержащих на поверхности гидроксильные группы таких молекул, как молекулы воды, спиртов, аммиака и аминов. Например, при адсорбции воды на тидроксилированнои поверхности снликагеля водородная связь может возникать по следующей схеме:
О
Н н н н
{ S
—Si—о—Si—+ Н20 —► —Si—О—Si—
II II
При образовании водородной связи энергия взаимодействия адсорбтива с адсорбентом довольно велика, и поэтому теплота, выделяющаяся при такой адсорбции, обычно значительно больше теплоты адсорбции веществ, сходных по геометрической форме и размеру молекул, но не образующих водородной связи.
Существенный вклад в раскрытие сущности адсорбционных явлений дало использование для их изучения инфракрасной спектроскопии. В частности, А. Н. Терениным было показано, что при адсорбции на поверхности кремнезема происходит возмущение гидроксильных групп, причем в инфракрасном спектре это проявляется в виде смещения частоты валентных колебаний гидроксильных групп поверхности в более длинноволновую область спектра. Это смещение оказалось не одинаковым для различных адсорбированных поверхностью молекул.
 1 ноября, 2012
1 ноября, 2012  admin
admin 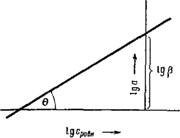
 Опубликовано в рубрике
Опубликовано в рубрике 