При растворении полимеров и олигомеров в органических растворителях образуются термодинамически равновесные однофазные системы с молекулярно-дисперсными компонентами (истинные растворы). Содержание растворителей в них может изменяться в широких пределах — от 10 до 90% (масс.).
Пленкообразующие системы этого типа имеют ряд достоинств. Они могут быть легко приготовлены из подавляющего большинства пленкообразующих веществ, причем технология их изготовления очень проста. Такие системы, как правило, имеют очень хорошую способность растекаться по поверхности (так называемый «розлив»), что обусловлено низким поверхностным натяжением органических растворителей. Последние в процессе формирования покрытия довольно легко улетучиваются из пленки, поскольку теплота их парообразования невысока.
Вместе с тем эти системы имеют и существенные недостатки. Они пожароопасны и токсичны, и, кроме того, при применении этих материалов в процессе отверждения (сушки) покрытий происходят безвозвратные потери растворителей, которые часто составляют 50—60% (и даже более) от массы лакокрасочного материала. Поэтому в последнее время появилась тенденция увеличивать содержание основного вещества (пленкообразующего) в лакокрасочных материалах (материалы с высоким содержанием основного вещества).
Выбор растворителей для пленкообразующих систем проводится с учетом растворяющей способности и скорости испарения органических жидкостей, технологических свойств лакокрасочного материала, экономических факторов, а также требований техники безопасности (взрыво — и пожароопасность, токсичность) и экологии.
Основы подбора растворителей для полимеров по их растворяющей способности до сих пор имеют полуколичественный характер. Хорошо известно эмпирическое правило, что химическое и структурное сходство полимера и органической жидкости облегчают растворение («подобное растворяется в подобном»). Были сделаны попытки количественной оценки растворяющей способности органических жидкостей по отношению к тому или иному полимеру с помощью понятия «плотность энергии когезии» Бк. Энергия когезии Ек — это энергия, необходимая для
Разрушения всех межмолекулярных контактов и отнесенная к одному молю вещества — кДж/моль. Для растворителей Ек равна энергии испарения. Отнеся ее к единице мольного объема (М3/мОЛь), получим величину ПЛОТНОСТИ энергии когезии £>к = =£к/Ум (кДж/м3).
Для практической оценки взаимной растворимости веществ» в том числе полимеров и органических жидкостей, используют не плотность энергии когезии, а производную от этой величины, названную параметром растворимости 6, который равен б= = (£>к) 1/2.
Параметр растворимости органических жидкостей определяют обычно по теплоте испарения:
6=[ (АН — КГ)/ЩЧ (1.125>
Где АН — энтальпия испарения, кДж/моль.
Поскольку полимер нельзя испарить, параметр его растворимости определяют косвенными методами, например по набуханию или растворению полимера в жидкостях с известными параметрами растворимости, или рассчитывают по суммарной энергии когезии атомных групп полимера.
Для этого можно использовать уравнение:
Б=(Рт)/М, (1.126)
Где р — плотность полимера, кг/м3; /•’г — вклад отдельных групп в энергию когезии, (МДж/м3) ,/2/моль; М — масса повторяющегося звена полимера» кг/моль.
Растворение полимеров будет происходить при любом соотношении компонентов при условии, что молярная энтальпия смешения ДН близка к нулю. Ее можно подсчитать по уравнению
ДЯ= (61 — б2) 2У<р, ф2> где б], 62 — параметры растворимости; фь <ря — объемные доли компонентов.
Величина Р=(б1—62)2 называется параметром совместимости. Чем она меньше (чем ближе значение параметров растворимости), тем лучше совместимость компонентов.
Органические жидкости, имеющие величины б, близкие к соответствующим величинам отдельных полимеров (при сходстве химического строения), действительно являются их хорошими растворителями. Так, поливинилхлорид (6=19,1) растворяется в дихлорэтане (6=19,6) и о-дихлорбензоле (6=20,6). Полиолефины (полиэтилен, полипропилен — соответственно 6=15,9 и 16,2) растворяются в алифатических углеводородах (гексане и октане, имеющих соответствующие величины 6=14,6 и 15,1), полистирол (6=18,2)—в бензоле и толуоле (6=18,2). Хорошими растворителями эпоксидных олигомеров (6=19,8) являются ацетон (6 = 20,0) и диоксан (6=20,0). В то же время
При полном несходстве химического строения органической жидкости н полимера даже при хорошем совпадении их величин 6 полимер не растворяется. Так, полистирол (6=18,2) не растворяется в кетонах (для метилэтилкетона 6=18,6, ацетона — 6 = 20,0). Такие отклонения в растворимости полимеров связаны с наличием в системе сильных специфических взаимодействий полимер — растворитель, которые не учтены при выборе критерия растворимости полимера по сходству параметров растворимости. К специфическим взаимодействиям относят водородные и координационные связи, образующиеся при участии функциональных групп в полимере и растворителе, в частности гидроксильной, карбоксильной, сложноэфирной, эпоксидной, урета- 5говои, аминной, амидной и др. Для таких систем плотность энергии когезии не всегда может служить критерием растворимости.
Попытки количественного учета межмолекулярных взаимодействий различного характера привели к появлению так называемого трехмерного параметра растворимости, который можно представить в виде векторной суммы величин трех частных параметров:
6s=62d+62p+ц2„, (1.127)
Где бd — параметр, учитывающий дисперсионные взаимодействия; бр — параметр, учитывающий дипольные и индукционные взаимодействия, характерные для полярных молекул; 6н — параметр, учитывающий взаимодействия, обусловленные водородными связями.
Расчет соответствующих величин 6 в этом случае возможен только с использованием эмпирических уравнений.
Трехмерный параметр может быть использован для определения области растворимости полимеров. Несмотря на то что параметр растворимости можно рассчитать, область растворимости обычно определяют только экспериментально — по растворимости данного полимера в различных растворителях. Нагляднее всего это можно проиллюстрировать, используя тройную диаграмму на плоскости (треугольник Гиббса). Перевод тройных параметров в координаты на этой диаграмме осуществляют, находя доли частных параметров от их суммы:
6 6 6 fi => 100 ~2бТ" ; fp=> 100 ; fh — 100 . (1.128)
Выраженные таким образом параметры дисперсионного, До — дярного и водородного взаимодействия в сумме дают 100. Каждый растворитель может быть изображен на площади треугольника точкой с координатами, соответствующими его величинам:
U, fP и fh-
С помощью тройной диаграммы может быть выбрана и оптимальная смесь растворителей для каждого олигомера. Пара-
![]()
|
Метр растворимости для смеси растворителей бсм — величина аддитивная и может быть рассчитан по уравнению |
![]()
|
Где VI — мольный объем 1-го компонента; XI — мольная доля 1-го компонента; х,= (С;/М;)/2 (С;/7И;); ЗДвСЬ С; — КОНЦвНТраЦИЯ КОМПОНеНТЭ, %(МЭСС.). |
![]()
|
(1.129) |
![]() Практически, например, для расчета состава бинарной смеси растворителей, выбранных с учетом технологических, экономических и других факторов, на диаграмму наносят точки, соответствующие их параметрам растворимости. Соединяя эти точки прямой линией, находят на ней точку, расположенную в наибольшей близости к точке олигомера, а затем по координатам этой точки определяют оптимальный состав смеси.
Практически, например, для расчета состава бинарной смеси растворителей, выбранных с учетом технологических, экономических и других факторов, на диаграмму наносят точки, соответствующие их параметрам растворимости. Соединяя эти точки прямой линией, находят на ней точку, расположенную в наибольшей близости к точке олигомера, а затем по координатам этой точки определяют оптимальный состав смеси.
В состав растворителей могут входить и органические жидкости, не растворяющие олигомеры, координаты которых расположены вне области их растворимости. Их обычно называют разбавителями.
Пара «растворитель — разбавитель» должна выбираться с таким расчетом, чтобы прямая, соединяющая точки с координатами растворителя и разбавителя, проходила вблизи точки олигомера. Такая смесь является растворяющей только на отрезке, попадающем в область растворимости. Наибольшей растворяющей способностью обладают смеси растворителей, координаты которых расположены с противоположных сторон точки, соответствующей олигомеру.
Растворяющую способность органической жидкости можно количественно оценить и на основе термодинамических соображений.
|
(1.130) |
![]() Вещество В растворяется в жидкости (растворителе), если оно имеет сродство к растворителю (и раствору) большее, чем к своей собственной фазе (к самому себе). Сродство В к данной фазе определяется величиной его химического потенциала рв (парциальной мольной энергией Гиббса, Дж/моль) в этой фазе. Сродство тем выше, чем ниже химический потенциал. Поэтому, если рв— химический потенциал вещества в собственной фазе, а рве — его потенциал в растворе, то вещество В будет обладать более высоким сродством к раствору в том случае* когда разность (р. в—рвэ) имеет положительное значение. Растворяющая сила (способность) йв растворителя вещества В равна (безразмерная величина):
Вещество В растворяется в жидкости (растворителе), если оно имеет сродство к растворителю (и раствору) большее, чем к своей собственной фазе (к самому себе). Сродство В к данной фазе определяется величиной его химического потенциала рв (парциальной мольной энергией Гиббса, Дж/моль) в этой фазе. Сродство тем выше, чем ниже химический потенциал. Поэтому, если рв— химический потенциал вещества в собственной фазе, а рве — его потенциал в растворе, то вещество В будет обладать более высоким сродством к раствору в том случае* когда разность (р. в—рвэ) имеет положительное значение. Растворяющая сила (способность) йв растворителя вещества В равна (безразмерная величина):
— (Р-В Р-вз) / >
Где Я — газовая постоянная, равная 8,315 Дж-К-1-моль-1; Т — абсолютная температура, К.
Химический потенциал раствора рве зависит от объемной доли растворенного вещества и возрастает с ее увеличением.
Если значение с1ъ положительно, то сродство В к растворителю больше, чем к своей фазе, и растворение происходит беспрепятственно. При отрицательном значении растворимость затруднена и может происходить разделение на фазы. При ^в = 0 устанавливается равновесие, и молярная доля растворенного вещества соответствует насыщению раствора.
С позиций термодинамики (1В равна сумме двух величин, имеющих вполне определенный физический смысл:
*гв=—+Д5,/Л — (1.131)
Первый член уравнения Д#< соответствует теплоте, поглощенной системой при переносе одного моля В из своей фазы в раствор. Второй член характеризует соответствующее изменение энтропии системы.
Если вещество В является полимером, содержащим г повторяющихся звеньев, то растворяющую силу для полимера с1р можно представить следующим образом:
(1.132)
Где с1т — растворяющая сила, отнесенная к повторяющемуся звену.
В свою очередь,
<1т=()хт-)хтв)/(т. (1133)
Где |хт и Цтэ — химические потенциалы повторяющегося звена соответственно в собственной фазе (полимере) и в растворе.
Следует отметить, что с1т характеризует растворяющую силу только определенного растворителя по отношению к определенному полимеру (его повторяющемуся звену). Для данного полимера другого типа значение йт может меняться. Например, оно уменьшается при переходе от аморфного к кристаллическому состоянию полимера. При снижении молекулярной массы полимера (1т повышается.
В уравнении (1,132) не учтено влияние концевых групп полимера, которым при достаточно больших молекулярных массах можно пренебречь.
Сравнение методов с использованием параметров растворимости и термодинамического метода показало, что результаты, полученные термодинамическими расчетами, лучше совпадают с экспериментальными данными. Это обусловлено тем, что параметры растворимости не учитывают энтропийных эффектов при растворении.
При подборе растворителей необходимо принимать во внимание некоторые особенности растворов полимеров. Изменение температуры при внешних воздействиях может привести к разделению раствора на фазы. Для систем полимер — растворитель, как и для низкомолекулярных веществ (например, для
Рис. 1.14. Фазовая диаграмма полимер (П) —растворитель (Р). На оси
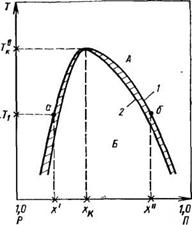 Абсцисс отложен состав (в долях). Объяснение см. в тексте
Абсцисс отложен состав (в долях). Объяснение см. в тексте
Систем жидкость — жидкость), можно построить диаграммы состояния, или фазовые диаграммы, которые характеризуют подчинение данной системы правилу фаз Гиббса. Для двухкомпонентных систем эта диаграмма представляет собой кривую растворимости в координатах температура — состав.
Для двухкомпонентной системы полимер — растворитель фазовые диаграммы могут иметь различный вид. Рассмотрим диаграмму (рис. 1.14) с верхней критической температурой растворения (ВКТР), равной Ткв. Подвижность молекул компонентов смеси влияет на равновесные концентрации сосуществующих фаз. Поэтому кривая растворимости для системы полимер — растворитель сдвигается в ■область низких концентраций полимера, так как подвижность макромолекул значительно меньше, чем у молекул растворителя.
Кривая взаимного растворения (смешения) отделяет (см. рис. 1.14) од — щофазную область неограниченного смешения А от двухфазной области ограниченного смешения В. Переход фазы А в фазу В (и наоборот) совершается при температуре фазового расслоения, в данном случае Ткв (ВКТР). Фаза А представляет собой гомогенный истинный раствор полимера в растворителе. В фазе В при температурах ниже Т,:в происходит расслоение однофазного раствора полимера на две фазы. Для полимерных систем характерно существование пограничной области критического (метастабильного) состояния раствора полимера, образование которой обусловлено полидисперсностью полимера и неодинаковой растворимостью различных полимергомологов. Эта пограничная область существует на грани фазового перехода.
Следовательно, при температуре, равной (или выше) Ткв, существует устойчивый истинный раствор полимера с концентрацией лгк. Кривая 1 (см. рис. 1.14) разделяет области существования однофазного (фаза А) и метастабильного (заштрихованная область) растворов и называется бинодалью. Температуры и концентрации, отвечающие бинодали /, характеризуют те условия, при которых устойчивый истинный раствор полимера переходит в ме — тастабильное состояние и образует коллоидный раствор с зарождающейся в нем новой фазой. Области метастабильного и неустойчивого (фаза В) растворов разделены кривой 2, называемой спинодалью. При температурах <ГКВ начинается расслоение на две фазы, состав которых можно определить, проводя горизонтальные линии, параллельные оси абсцисс и пересекающие кривую 1 на уровне соответствующей температуры. На рис. 1.14 показано, что при Т<ТКВ существуют две фазы (точки а и Ь на бинодали), имеющие составы х’ и х". В практически изученных системах равновесные концентрации полимера в фазе I (концентрация х’) очень малы. Эта фаза является раствором полимера в растворителе. Фаза II (концентрация х")
содержит много полимера и представляет собой как бы раствор растворителя в полимере. Состав фазы II сильно зависит от ее вязкости. Если вязкость невелика, то происходит ее полное отделение от фазы I с расслоением — системы с образованием двух жидких слоев. Чаще всего вязкость фазы II, богатой полимером, настолько велика, что в области расслоения В не наступает полного разделения фаз. Образуется гетерогенная смесь, в которой низковязкая фаза I распределена в высоковязкой устойчивой фазе II. Такие системы относятся к студням.
На основании изложенного можно сделать важный практический вывод о том, что Ткв всегда должна быть ниже температуры эксплуатации (или хранения) лакокрасочного материала, во избежание его расслоения на фазы.
На практике очень редко используют индивидуальные растворители. Это обусловлено как экономическими факторами, так и технологическими требованиями. Разбавители вводят в основном по экономическим соображениям.
Качество образующейся пленки (ее сплошность, глянец, декоративный вид и т. п.) во многом зависит от скорости улетучивания растворителя при пленкообразовании. Слишком быстрое улетучивание растворителя может привести к сильному охлаждению пленки и вследствие этого — к ее помутнению за счет конденсации на поверхности влаги из окружающей среды. Кроме того, в этом случае могут образоваться пористые пленки,, а также пленки с более высокими внутренними напряжениями,, поскольку при большой скорости удаления растворителя не успевают пройти релаксационные процессы. Пористые пленки могут образоваться и при слишком медленном улетучивании растворителя, например при формировании пленок из термореактивных пленкообразующих.
Для обеспечения нормальных условий пленкообразования — наиболее целесообразным оказывается введение в пленкообразующую систему одновременно нескольких растворителей, отличающихся по своей летучести и температуре кипения. В случае применения наряду с растворителями и разбавителей последние должны обладать большей летучестью, чем растворители, во избежание коагуляции полимера при пленкообразовании.
При выборе растворителей и разбавителей для лакокрасочных материалов необходимо учитывать их взрыво — и пожароопасность, а также токсическое действие на организм человека.
Промышленность выпускает большое число разнообразных смесевых растворителей различного назначения. Приводим некоторые составы [% (масс.)]:
1. Растворитель Р-5. Состав: ацетон — 30, бутилаце — тат — 30, ксилол — 40; применение — перхлорвиниловые, эпоксидные, кремнийорганические, полиакрилатные пленкообразова — тели;
2. Растворитель Р-189. Состав: бутилацетат—13, кси — .лол—13, метилэтилкетон — 37, этилгликольацетат — 37; применение — полиуретановые, уралкидные пленкообразователи;
3. Растворитель РС-2. Состав: ксилол — 30, уайт-спирит— 70; применение — тощие и средние пентафталевые, масляные, битумные пленкообразователи.
 31 августа, 2013
31 августа, 2013  admin
admin  Опубликовано в рубрике
Опубликовано в рубрике 