Существующие способы борьбы с коррозией металлов весьма разнообразны. По принципу воздействия на коррозионный процесс различают следующие группы защитных мероприятий:
1) изоляция поверхности металла от коррозионноактивной среды;
2) дезактивирующая обработка среды с целью уменьшения ее активности;
3) поддержание металла в термодинамически неактивном состоянии.
По механизму защитного действия применяемые мероприятия сводятся к трем группам:
1) повышение анодного контроля коррозионной системы — легирование сплавов пассивирующими компонентами, введение в раствор анодных ингибиторов коррозии, применение анодной электрохимической защиты;
2) повышение катодного контроля — уменьшение содержания катодных компонентов в металле, снижение концентрации деполяризаторов катодного процесса, введение в раствор катодных ингибиторов, применение катодной электрохимической защиты;
3) повышение электрического сопротивления системы — коррозионной среды, применяемых защитных покрытий или образующихся на поверхности продуктов коррозии.
Наибольший технический и экономический эффект в борьбе с коррозией достигается при изоляции металлов с помощью различных защитных покрытий — металлических, неорганических неметаллических, органических. Независимо от вида материала покрытия должны иметь хорошую адгезию, быть беспористыми и стойкими в среде, в которой эксплуатируется изделие.
Металлические покрытия подразделяются на катодные (более электроположительные, чем основной металл) и анодные (более электроотрицательные, при этом покрытие защищает основной металл электрохимически). Их наносят горячим способом, погружая изделие в ванну с расплавленным металлом, гальваническим (электроосаждение), термодиффузионным и механотермическим (плакирование) способами.
Неорганические неметаллические покрытия — силикатные, цементные, оксидные, фосфатные, хроматные и другие — применяют или самостоятельно, или в комбинации с лакокрасочными и другими покрытиями обычно в качестве подслоя. Их основное достоинство — повышенная термостойкость.
К Органическим покрытиям относят все виды полимерных покрытий, включая лакокрасочные и наносимые способами экструзии расплавов и плакирования, а также разного рода футеровочные покрытия — обмазки, обкладки тонколистовым материалом, гуммирование резиной. Из органических защитных материалов достаточно широко применяют защитные смазки и пленкообразующие ингибированные нефтяные составы (ПИНС) — разные по консистенции вещества, изготовляемые на основе продуктов переработки нефти, невысыхающих растительных масел, кремнийорганических и других олигомеров.
Уменьшение активности коррозионной среды обычно достигается введением в нее ингибиторов коррозии, а также деаэрацией (удалением растворенных и окклюдированных газов). И в том, и в другом случае достигается торможение электрохимического процесса за счет подавления анодной или катодной реакции либо обеих одновременно.
К способам, снижающим термодинамическую активность металлов, относят их легирование, катодную (наложение внешнего тока) и анодную (пассивация) защиту. Особенно эффективным может явиться более широкое использование металлов, имеющих аморфную структуру, как более устойчивых к внешним воздействиям.
С целью сохранения металлов все шире практикуется их замена при изготовлении изделий, конструкций и механизмов на неметаллические материалы — пластмассы, бетон, керамику, углеграфитные и другие материалы. Однако, когда требуются высокие значения теплопроводности и электрической проводимости в сочетании с хорошей механической прочностью и теплостойкостью, наиболее оправданным является применение металлов. Из способов их защиты особое внимание уделяется лакокрасочным покрытиям и ингибиторам коррозии.
По представлениям, развитым в работах Ю. Эванса, В. А. Каргина, Я. М. Колотыркина, И. Л. Розенфельда, Д. Е. Майна и других ученых, противокоррозионное действие лакокрасочных покрытий обусловливается торможением коррозионных процессов на границе раздела металл — пленка. Это торможение может быть связано с ограниченной скоростью поступления веществ, необходимых для развития коррозионного процесса, повышенным электрическим сопротивлением материала пленки, специфическим влиянием адгезии, химическим или электрохимическим воздействием материала пленки на подложку. Таким образом, факторами, определяющими защитные свойства покрытий, являются: проницаемость, электрическое сопротивление, эффект ингибирования, адгезионное взаимодействие с подложкой.
Влияние проницаемости. По данным Ю. Н. Михайловского, торможение процесса коррозии металла под покрытием Г2 может быть представлено суммой обратных величин: проницаемости Р по отношению к коррозионному агенту, его адсорбции Уадс поверхности металла и скорости анодной реакции уа:
В зависимости от активности среды лимитирующей оказывается та или иная стадия. В случае высокоактивных сред (растворы кислот, другие агрессивные жидкости и газы), когда практически отсутствует торможение анодного процесса ионизации металла, а степень адсорбции коррозионного агента велика, защитная способность покрытий в основном определяется проницаемостью пленки. При этом скорость коррозии укор ориентировочно может быть оценена следующим образом:
Укор = КРАС/6,
Где К — постоянная, зависящая от природы металла; ДС — градиент концентрации коррозионноактивного агента; 6 — толщина покрытия.
В таких условиях все факторы, обусловливающие уменьшение проницаемости покрытий: устранение пористости, кристаллизация и структурирование пленкообразователей, введение наполнителей и компонентов, реагирующих со средой, — благоприятно сказываются на защитной способности покрытий. В частности, в химическом машиностроении оправдало себя применение покрытий на основе химически стойких полимеров с низкой проницаемостью — фторопластов, пентапласта, полиэтилена, полипропилена, поливинилхлорида,
При изоляции труб — битумных покрытий. Вследствие низких коэффициентов диффузии электролитов и достаточно большой толщины покрытий (3 мм и более) нередко обеспечивается эффективная их барьерная защита в самых разных средах, в том числе и агрессивных.
В условиях воздействия слабых электролитов (содержащаяся в воздухе вода, атмосферные осадки) существенное влияние на коррозию оказывает способность электролита инициировать анодную реакцию. При доступе электролита подавление анодной реакции за счет поддержания металла в пассивном состоянии может явиться решающим фактором его защиты. Практика показывает, что тонкие пленки, к которым относится большинство лакокрасочных покрытий, проницаемы по отношению к агентам, вызывающим коррозию, в частности к кислороду воздуха и содержащейся в нем воде. Скорость проникновения воды и кислорода через различные полимерные пленки, по данным И. Л. Розенфельда и Ф. И. Рубинштейн, составляет [в г/(см2 • год)]:
Н20 1,122-1,190 02 0,004-0,050
Необходимое количество этих агентов для протекания коррозии стали со средней скоростью 0,070 г/(см2 • год), согласно реакции
4Бе + 302 + 2Н20 = 2Ре203 • Н20,
Составляет [в г/(см2 • год)]:
Н20 0,011 02 0,030
Сопоставляя эти данные, можно заключить, что в преобладающем числе случаев лакокрасочные покрытия, в том числе и пигментированные, не Представляют серьезного препятствия для диффузии агентов, необходимых для развития коррозионного процесса.
Имеются данные о том, что через год эксплуатации покрытий (масляные, алкидные, эпоксидные) в водных средах содержание Н20 и 02 под пленкой достигает значений, в несколько раз превосходящих их количества, необходимые для эффективного протекания процесса коррозии. Иначе говоря, барьерный принцип защиты тонких покрытий, какие обычно Используются в Лакокрасочной технологии, не является определяющим. Барьерный эффект полимерных покрытий, как показывает опыт, проявляется в большей степени по отношению к продуктам коррозии, чем к агентам, ее вызывающим. Так, проницаемость ионов железа — продуктов анодной реакции — на 1-2 порядка меньше, чем, например, воды, ионов хлора и других анионов. Таким образом, в отношении проницаемости защитные функции полимерных покрытий в Первую очередь Проявляются в Замедлении отвода продуктов коррозии с поверхности металла, поскольку ионная проводимость полимеров, особенно по отношению к катионам металлов, невысока.
Роль электрических свойств покрытий. Электрическое сопротивление покрытий в среде электролитов является суммой двух слагаемых — омического и поляризационного сопротивлений. Первое составляет меньшую долю общего сопротивления, однако оно является основным в защитном действии покрытий. При высоком омическом сопротивлении электрохимический процесс может не наступить. Отмечается определенная зависимость между электрическим сопротивлением пленок и их защитными функциями. В частности, хорошую защиту в морской воде обеспечивают покрытия, имеющие электрическое сопротивление не менее 108 Ом • см2. При погружении пленок в раствор электролита их электрическое сопротивление заметно падает. Так, в 0,5 н. растворе Кта2504 через 15 сут его значение для полимерных пленок составило (в % от исходного):
Эпоксидные 87 Поливинилбутиральные 25
Перхлорвиниловые 55 Нитратцеллюлозные 18
Электрическое сопротивление покрытий в растворах электролитов и в воде неуклонно снижается, хотя и с меньшей скоростью, чем в случае свободных пленок (рис. 5.11). Конечное значение сопротивления зависит от присутствия в пленкообразователе гидрофильных групп, особенно групп, способных к ионному обмену. Например, в растворе хлорида натрия электрическое сопротивление масляных и алкидных пленок вследствие гидролизующего действия электролита падает на 4-5 порядков. В таких условиях роль покрытия как электрического барьера сводится к нулю.
В отличие от гидрофильных пленок, покрытия, образованные гидрофобными пленкообразователями, способны более длительное время сохранять высокое электрическое сопротивление и тем самым в большей степени препятствовать развитию коррозионного процесса. Проводимость таких покрытий, однако, может возникать в результате присутствия сквозных пор, заполняемых электролитом, или появления других дефектов. Поскольку электрическое сопротивление покрытий уменьшается с повышением температуры, их защитная способность также падает.
Таким образом, электрические свойства покрытий, имея важное значение в электрохимических процессах, не являются определяющими при обеспечении защитных свойств покрытий. Нередко покрытия с низкими значениями электрической проводимости и емкости, причем мало изменяющимися во времени, проявляют низкие защитные свойства.
|
|
 Ъ сут 1 А /, А/СМ2
Ъ сут 1 А /, А/СМ2
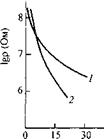
Рис. 5.11. Зависимость электрического сопротивления полиакрилатного покрытия (1) и свободной пленки (2) от продолжительности выдержки в воде при 20 °С
Рис. 5.12. Анодные потенциодинамические кривые стали СтЗ в контакте с водоразбавляемым полиэфируретаном (1) и 0,1 н. раствором Ш2804 (2)
Роль адгезии. Противокоррозионные свойства покрытий в большой степени зависят от адгезии. Благодаря адгезионному взаимодействию достигаются: 1) пассивация поверхности металла, 2) торможение анодной реакции, 3) замедление отвода продуктов коррозии. Если рассматривать коррозию металла как процесс адсорбции молекул коррозионноактивного вещества на вакантных участках его поверхности, то становится очевидным что чем выше адгезия, тем меньше остается таких вакантных участков и соответственно меньше появляется возможностей для развития коррозионного процесса.
При высокой прочности адгезионных связей изменяется и характер энергетического состояния поверхности металла под покрытием: происходит его пассивация, которая обусловлена адсорбционными процессами. Об этом свидетельствует, в частности, сдвиг стационарного потенциала металла в положительную сторону, плотность тока анодной поляризации снижается (рис. 5.12). Особенно благоприятное влияние на повышение стационарного потенциала (пассивацию металла) оказывают пленкообразователи (полиуретаны, карбоксилсодержащие водоразбавляемые и др.), способные при соответствующих условиях химически взаимодействовать с металлом с образованием нерастворимых соединений. Высокая адгезия покрытий может явиться существенным препятствием в развитии коррозионного процесса благодаря замедлению отвода продуктов коррозии. Их объ
ем всегда больше объема прокорродировавшего металла» отвод же вследствие малой диффузионной активности ионов сильно затруднен. Напротив, низкая адгезия является одной из причин нарушения покрытия и появления подпленочной коррозии. Поэтому все факторы, способствующие получению покрытий с высокой и стабильной в условиях эксплуатации адгезионной прочностью, благоприятно сказываются на защитной способности покрытий.
М. И. Карякиной предложена условная классификация покрытий по механизму их защитного действия. При этом выделены три механизма защиты: адгезионный, барьерный и смешанный.
К покрытиям, защищающим по Адгезионному механизму, относят покрытия с высокой адгезией к металлам, причем адгезия в процессе эксплуатации длительно сохраняется или даже возрастает. Это покрытия на основе полиуретанов, эпоксидных, фуриловых, алкидных, феноло — и мочевиноформальдегидных и других пленкообразовате — лей. Для таких покрытий толщина пленки не играет существенной роли. Нередко тонкие, но сплошные покрытия защищают металл так же эффективно, как и толстые. Повышению защиты способствует надлежащая подготовка — химическая модификация, выравнивание знака полярности адгезива и субстрата и др.
Барьерный механизм защиты свойствен покрытиям, получаемым на основе инертных полимерных пленкообразователей: полиолефи — нов, полифторолефинов, пентапласта, полимеров и сополимеров винилхлорида, полиамидов, некоторых полиакрилатов. Вследствие малой прочности адгезионных связей в этом случае возможна адсорбция коррозионноактивных агентов на поверхности металла, приводящая к возникновению подпленочной коррозии. Увеличение толщины таких покрытий, как правило, благоприятно сказывается на их защитной способности.
Смешанный механизм характерен для большинства других покрытий и является наиболее типичным.
Ниже приведены данные по свойствам покрытий из эпоксидного ЭП-524 (I) и фторопластового 32Л лаков (II), позволяющие судить о сравнительной эффективности адгезионного и барьерного механизмов защиты:
I II
TOC o "1-5" h z Адгезия, МПа 30 12
Коэффициент диффузии (водяные пары), см2/с 1 • 10~8 2 • 10~9
Водопоглощение, г/(см3 • Па) 7 • 10~7 7 • 10~8
Время до начала коррозии металла, ч:
В 5 %-м растворе НИОз 198 138
В 3 %-м растворе 1^аС1 252 132
В атмосфере 95 %-й влажности при 40 °С 312 184
Из этих данных видно, что фторопластовое покрытие, несмотря на лучшие по сравнению с эпоксидным изолирующие свойства, уступает последнему по защитной способности. Адгезионный механизм в данном случае превалирует над барьерным.
Эффект ингибирования. Ингибирующие свойства лакокрасочных покрытий обычно обеспечиваются за счет введения в их состав противокоррозионных пигментов и ингибиторов коррозии. Это позволяет получать покрытия с хорошими противокоррозионными свойствами на металлах не только из органорастворимых, но и воднодисперсионных и водоразбавляемых материалов.
Эффект ингибирующего действия проявляется главным образом в электрохимических процессах, происходящих на границе металл — пленка. Поэтому ингибированные покрытия эффективны только тогда, когда они служат первым (грунтовочным) слоем. При контакте ингибированной пленки с металлом могут происходить разные процессы: изменение потенциала анодных и катодных участков, изменение pH среды, образование на металле оксидных пленок и ингибирующих комплексов; присутствие пигментов может влиять и на диффузионные характеристики покрытия (см. гл. 4). Наиболее полно эти процессы проявляются в присутствии электролитов. Поэтому эффективность многих пигментов и ингибиторов как противокоррозионных добавок зависит от их растворимости, а продолжительность действия — от времени, в течение которого они сохраняются в пленке в той концентрации, при которой способны поддерживать металл в пассивном состоянии. При диффузии в покрытии электролит подрастворяет частицы пигмента или ингибитора и переносит их в растворенном или ионном состоянии на поверхность металла, вызывая пассивацию последнего (рис. 5.13). Скорость переноса зависит от диффузионной активности материала пленки, состава и активности электролита по отношению к пигменту, а также pH среды.
Наиболее распространено применение в покрытиях пигментов. В зависимости от механизма действия различают Пигменты-ингибиторы и Пигменты-пассиваторы.
![]()
|
Электролит |
![]() Анодное ингибирование достигается пигментами, обладающими способностью принимать электроны или увеличивать pH среды и вследствие химических процессов окисления или гидратации образовывать на анодных участках защитные пленки. Результатом их
Анодное ингибирование достигается пигментами, обладающими способностью принимать электроны или увеличивать pH среды и вследствие химических процессов окисления или гидратации образовывать на анодных участках защитные пленки. Результатом их
|
II I I I II |
![]() Рис. 5.13. Схема переноса пассиви — Пленка РУЮ1ДИХ ионов пигментированной (ингибированной) пленки на ме — Металл тадл
Рис. 5.13. Схема переноса пассиви — Пленка РУЮ1ДИХ ионов пигментированной (ингибированной) пленки на ме — Металл тадл
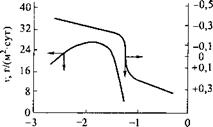
Рис. 5.14. Зависимость скорости коррозии V и потенциала ф стали от концентрации С ионов СгОд" в 0,1 н. растворе Ш2804
 Действия является смещение электродных потенциалов металлов в более положительную сторону, в том числе в область пассивного состояния, в которой коррозии металла не про-
Действия является смещение электродных потенциалов металлов в более положительную сторону, в том числе в область пассивного состояния, в которой коррозии металла не про-
1§ С (моль/л)
Исходит. Приведенные ниже данные показывают сдвиг стационарного потенциала стали в воде под влиянием добавок пигментов:
|
Ф, В +0,08 +0,02 -0,05 -0,04 |
![]()
Ф, В
TOC o "1-5" h z Свинцовый сурик +0,77
Калий-барийхромат +0,59
Цианамид свинца +0,59
Цинковый грунтовочный крон +0,14
Цинковые белила Желтый свинцовый крон Диоксид титана Железный сурик
Как видно из этих данных, противокоррозионное действие пигментов сугубо избирательно. Наиболее эффективными анодными замедлителями являются пигменты-окислители (три — и тетраоксихро — маты цинка, хромат стронция, калий-барийхромат), а также пигменты, обладающие основными свойствами (свинцовый сурик, цинковые белила, фосфат хрома, цианамид свинца).
Эффект действия хроматных пигментов возрастает с увеличением их растворимости в воде, т. е. с ростом степени ионизации. Растворимость хроматов металлов Ъп, Бг, Ва, РЬ соответственно равна 1,1; 0,6; 0,001 и 0,00005 г/л. Таким образом, наиболее ценными в противокоррозионном отношении и вследствие этого самыми распространенными являются хроматы цинка — цинковые крона. При воздействии воды они образуют растворы с pH 7,0-7,6 и концентрацией хромат-ионов 3 • 10-2 моль/л и более. Этой концентрации оказывается достаточно для того, чтобы сместить потенциал железа в нейтральной среде до +0,3+ +0,5 В, при котором наступает его пассивное состояние (рис. 5.14). Механизм действия хроматных пигментов связан с адсорбцией хромат-ионов на поверхности металла, восстановлением хрома из шестивалентного до трехвалентного состояния и образованием нерастворимых сложных комплексных соединений Бе3+ и Сг3+. При этом адсорбируются комплексные ионы, образующиеся при действии воды на хроматные пигменты:
Н, о
|
2пСг04 • 4Н20 |
![]() [2пСг04(0Н)«]8“ + 8Н+.
[2пСг04(0Н)«]8“ + 8Н+.
Пассивирующая способность кронов максимальна в чистой воде. Если покрытие эксплуатируется в электролитах, содержащих агрессивные ионы, например СГ, Б04 , то пассивирующая способность резко падает. Поэтому крона как противокоррозионные пигменты непригодны для защиты металлов от коррозии в сильноагрессивных средах. Хроматные пигменты токсичны, что существенно ограничивает их применение.
Эффективны по своему противокоррозионному действию в покрытиях и фосфатные пигменты — фосфаты цинка, хрома, марганца, гидрофосфат цинка. Их применяют как самостоятельно (фосфат цинка), так и в смеси с хроматными пигментами (фосфат хрома). Главное преимущество этих пигментов перед хроматными — низкая токсичность. Противокоррозионное действие фосфатных пигментов основано на их диссоциации
2п3(Р04)2 • 4Н20 5^ [2пз(Р04)2(0Н)2(Н20)2]2′ + 2Н+. и адсорбции образующихся ионов на анодных участках поверхности; возникающие при этом железо-цинкфосфатные комплексы пассивируют металл. Наиболее распространенный из фосфатных пигментов фосфат цинка, кроме того, обеспечивает экранирующий эффект вследствие пластинчатого строения его частиц.
Фосфатные пигменты применяют в грунтовочных составах преимущественно по черным металлам, а хроматные — по цветным (алюминию, сплавам алюминия и магния).
Пигменты основного характера (оксид цинка и др.) применяют исключительно для защиты черных металлов. Их защитное действие связано с генерированием гидроксильных ионов, способствующих образованию пассивирующего оксида по реакции:
Бе + 20Н~ — 2е —► БеО + Н20.
Свинцовые пигменты благоприятно влияют на защитную способность покрытий в морской воде. Например, свинцовый сурик РЬ304 при гидратации в воде способен образовывать ряд соединений: РЬ(ОН)2, РЬ203 • Н20 и др. Первое, взаимодействуя с сульфатами металлов, имеющих радиус катиона менее 0,12 нм, дает нерастворимые осадки сульфата свинца, отлагающиеся преимущественно на катодных участках поверхности; второе, осаждаясь в виде комплексной соли с железом, экранирует анодные участки. Этот пигмент применяют преимущественно с такими пленкообразователями, как растительные масла, алкиды, хлоркаучук, эпоксидные олигомеры.
Катодное ингибирование (протекторная защита) в нейтральных средах осуществляется в результате использования порошков металлического цинка (цинковой пыли) и магниевых сплавов, в щелочной — порошков металлического свинца. Потенциал цинка в морской воде достигает -0,83 В, а свинца в щелочных средах -0,84 В. Это позволяет применять их в качестве эффективных протекторов по стали и другим металлам, имеющим более положительные электродные потенциалы. Действие этих пигментов, однако, проявляется при высокой степени наполнения, когда достигается контакт между частицами, обеспечивающий хорошую электрическую проводимость пленок. Так, протекторные цинковые покрытия на основе полистирола, этилси — ликата, эпоксидных и других пленкообразователей содержат до 95- 96 % (по массе) металлического порошка.
Алюминиевая пудра из-за наличия на поверхности частиц оксидной пленки и слоя смазки не способна к электрохимической защите. Ее положительное влияние в противокоррозионных покрытиях сводится к обеспечению барьерного эффекта.
В сочетании с пленкообразователями можно применять не только противокоррозионные пигменты, но и вещества непигментного характера — различные Ингибиторы коррозии. При этом достигается нередко более высокий противокоррозионный эффект, чем в случае использования пигментов.
Ингибиторы коррозии — низкомолекулярные, олигомерные и полимерные вещества неорганической и органической природы, способные адсорбироваться из растворов или газовой фазы на поверхности металлов (анодных или катодных участках) и, взаимодействуя с ними, делать металл более устойчивым в коррозионном отношении.
По способу воздействия на металл выделяют ингибиторы контактные и парофазные. Наибольшее применение в лакокрасочных покрытиях получили контактные ингибиторы (их действие проявляется при непосредственном соприкосновении с поверхностью металла), однако известны составы и с парофазными ингибиторами коррозии.
Механизм действия ингибиторов коррозии неоднозначен. Анодные ингибиторы, воздействуя на анодные участки, либо вызывают окисление металла и образование труднорастворимых осадков, либо экранируют их механически вследствие адсорбции. Действие катодных ингибиторов основано на снижении содержания кислорода в растворе, повышении перенапряжения катодного процесса или уменьшении площади катодов. Имеются ингибиторы (преимущественно экранирующего типа), которые замедляют одновременно и катодную, и анодную реакции.
Из неорганических соединений водорастворимого типа распространенными замедлителями коррозии в нейтральных средах являются соли щелочных металлов и азотистой и хромовой кислот. Их применяют в водных составах индивидуально или в смеси с другими ингибиторами — Na2C03, Na3P04, Na2HP04, уротропином, бензоатом аммония и др. При содержании нитрита натрия в воде (0,2 г/л) начальный потенциал стали смещается в положительную сторону более чем на 0,7 В, при этом скорость растворения стали практически сводится к нулю. Действие хроматов и щелочных солей аналогично действию соответствующих пигментов. Такие ингибиторы применяют преимущественно при подготовке поверхности металлов.
Органические ингибиторы — соединения различных классов, в основном относящихся к группе ПАВ (гидрофильно-лиофильный баланс 5-20) адсорбируются на электродных участках, вызывая экранирующий эффект. Наиболее эффективны те из них, которые склонны к хемосорбции, т. е. содержат активные группы — доноры и акцепторы электронов: —CN, —CNS, —CNO, —NH2) =СО, —СНО и др. По адсорбционной способности и соответственно ингибирующему эффекту алифатические соединения располагаются в следующий ряд:
Кислоты > Амины > Спирты > Эфиры.
Повышенной адсорбционной способностью обладают также этиленовые и особенно ацетиленовые производные, вследствие взаимодействия я-электронов с поверхностными атомами металлов.
Для получения ингибированных покрытий нашли применение многие органические соединения, которые подразделяются на Водорастворимые: хроматы гуанидина и циклогексиламина, фосфат гуанидина, таннин, бензотриазол, гексаметиленимин и др.; и Маслорастворимые: соли и комплексы аминов и синтетических жирных, нафтеновых и сульфокислот (ингибиторы МСДА, ПМП, ИФХАН, КИНК, ИКБ-2 и др.), производные морфолина и 8-капролактама (ингибиторы ВНХ-101, ВНХЛ-49), амиды жирных кислот (алкиленсукцинимид карбамида), нитрованные масла, петролатум, церезин (ингибиторы АКОР-1, ИНГА, МНИ-5, МНИ-7), нефтяные сульфонаты кальция и карбамида (ингибиторы КСК и БМП), аддукты малеинового ангидрида и полибутадиенов.
Водорастворимые ингибиторы вводят как в водные, так и в органорастворимые составы, маслорастворимые — преимущественно в материалы, содержащие органические растворители, однако ингибиторы водовытесняющего типа пригодны и в воднодисперсионных составах.
Имеется ряд особенностей получения ингибированных покрытий. В отличие от пигментов, которые можно сочетать с самыми разными пленкообразователями, ингибиторы выбираются индивиду
ально для каждого вида пленкообразующей системы с учетом их химического взаимодействия с ее компонентами (при наличии такого взаимодействия ингибитор берется в избытке). Следует учитывать и избирательное действие ингибиторов по отношению к разным металлам, а также требования по подготовке их поверхности.
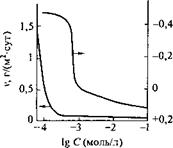
Поскольку адсорбция идет преимущественно по активным центрам поверхности, а они, как правило, имеют разную природу, нередко лучший защитный эффект достигается при использовании смесей двух или нескольких ингибиторов. Концентрация ингибитора выбирается с учетом эффекта его действия. Так, для хромата цикло — гексиламина (СбНпИНгЬНгСгС^, по данным И. Л. Розенфельда и Ф. И. Рубинштейн, минимальная концентрация в водном растворе составляет 1 • 10_3 моль/л. При этой концентрации необратимый электродный потенциал стали смещается в область положительных значений, и коррозия металла становится близкой к нулю (рис. 5.15). Минимальная концентрация хромата циклогексиламина при введении его в алкидный лакокрасочный материал составляет 3 % от массы пленкообразователя.
 Аналогичным образом вызывает пассивацию металла хромат гуанидина ЫН=С(НН2)2*Н2Сг04, будучи введенным в состав масляных и алкидных красок в количестве 3-6 % (рис. 5.16).
Аналогичным образом вызывает пассивацию металла хромат гуанидина ЫН=С(НН2)2*Н2Сг04, будучи введенным в состав масляных и алкидных красок в количестве 3-6 % (рис. 5.16).
|
Ф, в
|
Рис. 5.15. Зависимость скорости коррозии V И потенциала <р Стали от концентрации С хромата циклогексиламина в водном растворе
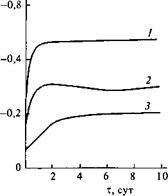
Рис. 5.16. Зависимость потенциала стали от продолжительности испытания в 3 %-м растворе №С1:
1 — неокрашенный металл; 2 — металл, окрашенный масляной краской; 3 — металл, окрашенный масляной краской с 6 % хромата гуанидина
Действие ингибиторов проявляется не только при их введении в состав лакокрасочных материалов, но и при обработке поверхности металлов перед окрашиванием.
Разработаны и нашли промышленное применение содержащие ингибиторы коррозии воднодисперсионные и органорастворимые лакокрасочные материалы: краски и эмали для длительной противокоррозионной защиты (марки ГФ-570, ГФ-570РК, ГФ-750, МС-1181) и составы для временной защиты металлов, в том числе съемные (см. гл. 4) и смываемые (марки ИС-1, ИСМ-3, ИП-27 и др.). Для профилактической и межоперационной защиты металлоизделий наряду с этим широко используются пленкообразующие ингибированные нефтяные составы (ПИНС) мМовильм, "Шасси-Универсал", НГ-216 и др., а также ингибированные восковые составы и смазки. При их нанесении поверх лакокрасочных покрытий достигается особенно высокая противокоррозионная защита.
Использование ингибиторов коррозии наряду с пигментами — один из наиболее действенных путей повышения защитных свойств лакокрасочных покрытий. Это видно хотя бы на таких примерах. Тонкое покрытие из неингибированной олифы защищает сталь в атмосфере 100 %-й влажности примерно 10 сут, такое же покрытие с ингибитором хроматом гуанидина — до 1 года. Длительность защиты съемного неингибированного покрытия из эмали ХВ-114 в атмосферных условиях не более 6 мес, ингибированного (ингибиторы АКОР-1, БМП или МСДА-11) — свыше 3 лет. С использованием ингибиторов коррозии появилась возможность получать многие высокоэффективные противокоррозионные грунтовки на основе водных дисперсий полимеров, а также составы с пониженным содержанием токсичных и дефицитных противокоррозионных пигментов или без них.
 14 апреля, 2013
14 апреля, 2013  editor
editor 
 Опубликовано в рубрике
Опубликовано в рубрике 