В строительной технике часто приходится сталкиваться с явлениями прилипания (удержание слоя краски на поверхности предмета, сцепление штукатурки с кирпичом) и склеивания (облицовка стен плитками, покрытие пола линолеумом). Прилипание двух тел — результат проявления сил адгезии и когезии. Склеивание— это соединение двух тел при помощи третьего (клея)-
Адгезией называется прилипание двух разнородных жидких или твердых тел, обусловленное молекулярной связью, проявляющейся при соприкосновении этих тел. Притяжение частиц (атомов, ионов, молекул) внутри данного тела называется когезией. Прочность клеевой прослойки определяется силами когезии. Сцепление же ее со склеиваемым материалом (или материалами) обусловлено силами адгезии.
Химическая и физическая природа явлений адгезии и когезии едина. Она обусловлена межмолекулярным взаимодействием, т. е. отношением сил притяжения между молекулами, которое в свою очередь зависит от электрической природы веществ и определяется движением электронов и взаимодействием создаваемых ими электрических полей. Распределение электрических зарядов в веществе определяет его полярность. Полярные молекулы ориентируются в массе вещества так, что противоположные по знаку заряда участки притягиваются, создавая устойчивую систему, в которой действуют электростатические силы. Чем более полярны вещества, тем больше величина электростатических сил. Поэтому адгезия полярных веществ к полярным обычно высокая. Как правило, полимеры, содержащие гидроксильные (ОН), карбоксильные (СООН), амидные (NHCO), аминные (NH2) и другие полярные группы, являются хорошими клеями.
Различают несколько видов межмолекулярного взаимодействия (или межмолекулярных сил): электростатическое, индукционное, дисперсионное, водородная связь. Кроме того, для склеивания имеют значение и химические связи (ионные, ковалентные, координационные).
Согласно теории, разработанной Дебаем, энергия Электростатического взаимодействия полярных молекул зависит от температуры, повышение которой нарушает ориентацию заряженных молекул в результате их теплового движения и снижает величину электростатического взаимодействия. Под влиянием электрического поля полярных молекул может произойти поляризация неполярных веществ, находящихся в контакте с полярными. Результатом взаимодействия между молекулами этих веществ является притяжение, подобное притяжению полярных молекул, но более слабое. Возникающие при этом силы называются индукционными. В отличие от электростатических сил они не зависят от температуры, но быстро убывают с расстоянием между частицами.
Наконец, независимо от наличия или отсутствия в молекулах электрических зарядов между ними действуют силы, называемые дисперсионными. Они являются результатом взаимной поляризации молекул, вызываемой непрерывным движением электронов рядом расположенных атомов. Дисперсионное взаимодействие проявляется при расстояниях между частицами до 3—4 А. Так как нагревание тел не оказывает заметного влияния на движение электронов, то величина дисперсионных сил не зависит от температуры.
Согласно современным представлениям максимальное действие этих сил проявляется в микроуглублениях, имеющихся на поверхности твердого тела, так как силовые поля, образуемые противоположными стенками этих углублений, будут накладываться друг на друга и таким образом усиливаться [3].
При склеивании большое значение имеет еще одна разновидность межмолекулярного взаимодействия — водородная связь. По характеру и величине действующих сил она близка к электростатическому взаимодействию и может возникать между непосредственно не связанными группами внутри одной и той же молекулы, между молекулами одного и того же соединения и между молекулами различных соединений, содержащих водород, кислород, азот, хлор. Ее действие проявляется на расстоянии до 2,5—2,8А. Гидрофильность (способность хорошо смачиваться водой) поверхности древесины, имеющая важное значение для склеивания, частично обусловлена образованием водородных связей между молекулами воды и гидроксильными группами молекул целлюлозы. Эту связь можно представить общей для многих веществ схемой (рис. 1).
При склеивании металлов синтетическими клеями образуется так называемая ионно-дипольная связь. Возникает она между ионами металлов и полярными молекулами полимеров, например, содержащих группы CN в феноло-акрилонитрильных клеях или сложно-эфирные
группировки в поливинилацетатном и полиметилмета — крилатном клеях. Эта связь образуется как при взаимодействии клея с поверхностными окисными пленками, так и на границе с чистыми неокисленными поверхностями металлов. Силы ионно-дипольного взаимодействия убывают с увеличением расстояния между частицами слабее, чем водородные связи, и поэтому обеспечивают высокую адгезию.
Иногда при склеивании проявляется действие сил химической связи — ковалентной и координационной. Они
Действуют на значительно меньших расстояниях, чем дисперсионные, индукционные и электростатические. Их энергия в десятки раз превосходит энергию межмолекулярных связей.
Твердого материала с клеем. Заключительной стадией склеивания является переход клея в твердое состояние, т е. его когезионное упрочнение.
На полноту смачивания поверхности и величину сцепления с ней клея влияют форма и размеры микроуглублений на поверхности. Любая поверхность твердого тела представляет собой систему выступов и впадин, т. е. имеет неровности, зависящие от способа обработки. Наиболее распространенные формы углублений схематически изображены на рис. 2. С точки зрения полноты смачива ния более благоприятны коническая (рис. 2, а) и призма тическая (рис. 2, г) формы.
|
Рис. 2. Формы углублений на поверхности твердого тела: О и б — коническая; в — цилиндрическая; в —при Зматическая; д — сферическая |
Следует различать склеивание плотных и пористых тел. Углубления на поверхности плотных тел представляют собой капилляры, которые клей заполняет под влиянием капиллярного давления. При этом находящийся в капиллярах воздух сжимается и препятствует прониканию в них клея. Практически клей не заполняет капилляров полностью, поэтому смачиваемая поверхность всегда меньше свободной поверхности, взятой с учетом всех ее неровностей. При склеивании непористых материалов сжимаемый в капиллярах воздух частично поглощается жидким клеем. В пористых телах воздух, содержащийся в капиллярах, отжимается под влиянием прилагаемого давления и диффундирует в глубь тела, поэтому сцепление клея с поверхностью пористых тел происходит в более благоприятных условиях. Учитывая смачивающую способность клея и прилагаемое давление, глубину заполнения клеем неровностей поверхности непористых тел с углублениями конической формы выражают формулой
|
|
(1.1)
Где H — средняя глубина заполнения капилляра, см; Н — средняя высота микронеровностей, см р — прилагаемое давление, Г/см2; рн — начальное давление воздуха в углублениях, Г/см2; а — поверхностное натяжение жидкого клея, Г/см.
Согласно приведенной формуле глубина заполнения зависит в основном от давления (без учета поглощения воздуха жидким клеем, также зависящего от давления).
Существует несколько теорий склеивания: механическая, адсорбционная, электронная, диффузионная, химическая.
Механическая теория склеивания выдвинута в 30-х годах XX в. Мак-Беном. По этой теории при склеивании образуется механическая связь между клеем и поверхностью склеиваемого материала наподобие шипового или заклепочного соединения. Более поздние исследования показали недостаточность общих представлений механической теории и ограничили применимость ее лишь для частных случаев склеивания, например пористых материалов [50, 77].
Образование клеевого соединения в несколько стадий и преимущественное значение поверхностных явлений в процессе склеивания лежат в основе адсорбционной теории адгезии, выдвинутой Мак-Лареном, Дебройном, Ставерманом [1, 5]. Многие представления этой теории основаны на анализе энергетических состояний при смачивании клеем поверхности твердого тела. Однако попытки оценить адгезию энергией смачивания и связать ее с физико-механическими свойствами соединения осложняются тем, что с момента нанесения клея на твердую поверхность энергия смачивания непрерывно изменяется в результате испарения растворителя, затвердевания расплавленного клея или химической реакции, протекающей при отверждении. Поэтому конечная энергия системы после отверждения не равна энергии в момент смачивания и по величине энергии (или работы) смачивания нельзя судить о прочности адгезионной связи затвердевшего клея к поверхности. Адгезия затвердевшего клея опреде — пяется по механическому отрывающему усилию или по аботе, затрачиваемой на разъединение твердых поверхностей.’ Если величина адгезии при смачивании измеряется в момент равновесного состояния системы, то механическое отделение пленки клея является процессом неравновесным. Сопротивление пленки отрыву зависит от скорости разъединения: чем она больше, тем большая затрачивается работа. Только в том случае, если пленка отрывается очень медленно, так что процесс проходит ряд равновесных и обратимых состояний, полученные данные можно сравнивать с работой смачивания.
Адсорбционная теория объясняет связь между микро — геометрией поверхности и прочностью склеивания следующим образом. При нанесении клей взаимодействует с поверхностью лишь в отдельных точках, которые представляют собой активные адгезионные центры. Остальная часть поверхности не может войти в контакт с клеем из-за наличия на поверхности адсорбированных веществ, сопротивления воздуха в капиллярах и других причин, препятствующих полному смачиванию. Чем более шероховата поверхность, тем больше ее активных центров вступает в контакт с клеем и тем сильнее проявляются силы адгезии. Несмотря на то, что не вся склеиваемая поверхность смачивается клеем, концентрация молекул около активных центров уравнивает неполноту смачивания, так что в целом на единицу площади клеевого шва число молекул, участвующих в сцеплении, достаточно велико. Однако плотность молекулярных цепей с удалением от точек сцепления уменьшается. На основе этого существует представление о трехслойной структуре клеевой прослойки вблизи границы раздела ее со склеиваемым материалом [1]. Согласно этому представлению в клее последовательно образуются три слоя:
1) слой ориентированных молекул, удерживаемых у поверхности твердого тела силами межмолекулярного или химического взаимодействия;
2) промежуточный слой с менее упорядоченным расположением молекул;
3) основной слой с более или менее равномерным пространственным распределением межмолекулярных связей.
Представление о механизме образования трехслойной структуры в значительной степени условно. С точки зрения современных представлений о строении полимеров, оно не охватывает всего многообразия процессов формирования клеевого соединения. Большие размеры и сложное строение молекул полимеров и ограниченные зазоры между склеиваемыми поверхностями исключают в ряде случаев возможность образования многослойной структуры. Расположение функциональных групп в молекулах может ориентировать их не поперек, а вдоль плоскости склеивания (конечно, понятие о плоскости в данном случае весьма условно и принято лишь для схематических представлений). Адсорбционная теория не объясняет возможности склеивания слабополярных материалов — каучука, полиизобутилена и др. Многие ее выводы сделаны на основании опытов с низкомолекулярнымп жидкостями, в то время как для склеивания применяют преимущественно высокомолекулярные соединения.
Проведенные в 1949—1950 гг. Б. В. Дерягиным и его •сотрудниками опыты показали, что при отслаивании полимерных пленок от поверхности твердых тел затрачивается гораздо большая работа, чем это необходимо для преодоления сил межмолекулярного взаимодействия, и что эта работа тем больше, чем выше скорость отслаивания. Адсорбционная теория не объясняет это явление, так как величина межмолекулярных сил не должна зависеть от скорости разделения склеенных поверхностей. Было выдвинуто предположение, что между твердой поверхностью и клеевой пленкой в период отверждения образуется двойной электрический слой (микроконденсатор) [3, 4].
Механизм образования и разрушения двойного электрического слоя в клеевом соединении объясняет электронная теория адгезии, предложенная Н. А. Кротовой и Б. В. Дерягиным. По современным представлениям, двойной электрический слой образуется в результате ориентирования заряженных частиц клея и поверхности, твердого тела с возникновением затем разности потенциалов между ними. Однако в отличие от электростатического взаимодействия при образовании двойного электрического слоя происходит взаимный переход электронов между функциональными группами молекул полимера и
Инятие ими электронов от поверхности твердого тела. Образование двойного электрического слоя при склеива — и подтверждается электронной эмиссией, наблюдаемой 0Хрыве пленок различных полимеров от поверхности стекла, металла и других материалов. Электронная тео — пия не’ объясняет адгезию между неполярными полимерами и возможность склеивания металлов и диэлектрических материалов токопроводящими клеями, наполненными порошками металлов, графитом, сажей.
Диффузионная теория адгезии, разработанная С С. Воюцким [2], объясняет адгезию как результат взаимного проникновения, или диффундирования, линейных макромолекул или их участков с образованием прочного переходного слоя на границе между клеем и склеиваемым веществом. По этой теории, применимой к склеиванию полимеров преимущественно линейного строения,, чем больше гибкость макромолекул, тем больше их’ способность к взаимному проникновению, и чем ближе химическая природа склеиваемых полимеров, тем легче осуществляется взаимное проникновение. Наиболее характерным примером такого взаимного проникновения макромолекул является аутогезия (самослипание) полимеров линейного строения при нагревании или при нанесении на склеиваемые поверхности органического растворителя. Молекулы полимера диффундируют в раствор, а при соприкосновении поверхностей — взаиморастворяются. Связь, образующаяся в результате взаиморастворения, обладает значительной энергией, большей, чем энергия адсорбционных сил. Предполагают, что это обусловлено межмолекулярным взаимодействием, усиленным большим количеством контактов и отчасти механическим заклиниванием макромолекул или их участков, проникших в соседний полимер. Диффузионная теория раскрывает также зависимость работы адгезии от скорости отслаивания. Поскольку между прослойкой клея и склеиваемым веществом образуется переходный слой макромолекул, он подчиняется таким же закономерностям при — разрушении, как и любой полимер, т. е. с увеличением скорости нагружения сопротивление разрушению также увеличивается.
В основе химической теории адгезии, развиваемой в последние годы, лежит представление о том, что — при взаимодействии клея с поверхностью твердого тела образуются ковалентные или координационные связи. Действительно, имеются примеры, показывающие возможность протекания химических реакций между клеем и склеиваемыми материалами [30, 37, 78].
Как видим, единой теории склеивания нет, так как полностью ни одна из теорий не может объяснить все многообразие и специфичность явлений, возникающих на различных стадиях склеивания. Но даже неполные теоретические представления, применимые для частных случаев, оказываются полезными при синтезе новых клеев и конструировании соединений.
 24 декабря, 2012
24 декабря, 2012  admin
admin 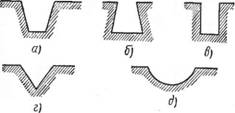
 Опубликовано в рубрике
Опубликовано в рубрике 